
- •Химия окружающей среды Учебное пособие
- •Физико-химические процессы в литосфере Введение
- •1. Строение литосферы и структура земной коры
- •Примеры решения задач
- •2. Минералы и горные породы
- •2.1. Магматические породы
- •2.2. Осадочные породы
- •2.3. Метаморфические горные породы
- •Пример решения задач
- •3. Гипергенез и почвообразование
- •Пример решения задач
- •4. Механический состав почв
- •Примеры решения задач
- •5. Элементный состав почв
- •Примеры решения задач
- •6. Органические вещества почвы
- •6.1. Классификация органических веществ почвы
- •6.2. Неспецифические органические соединения в почвах
- •6.3. Специфические гумусовые вещества почв
- •6.4. Органоминеральные соединения в почвах
- •Примеры решения задач
- •7. Поглотительная способность почв
- •7.1. Катионообменная способность почв
- •7.2. Обменные катионы почв
- •Примеры решения задач
- •8. Щелочность и кислотность почв
- •Примеры решения задач
- •9. Соединения азота в почве
- •Примеры решения задач
- •10. Соединения фосфора в почве
- •Примеры решения задач
- •Контрольные вопросы по теме «Физико-химические процессы в литосфере»
- •Задачи для самостоятельного решения
- •«Физико-химические процессы в литосфере»
- •Вопросы
- •К учебному модулю
- •Задачи к учебному модулю
- •Литература
- •Содержание
- •Учебное издание
Примеры решения задач
Пример 19.
Образец почвы был взят из верхнего
горизонта влажной почвы. Из образца
массой 50 г были экстрагированы 19-нитраты
при помощи 200 мл 2 М КСl.
Измеренная концентрация ионов NO![]() составляла 6 мг/л. Содержание воды во
влажной почве – 26 г/100 г абс. сухой почвы.
Рассчитайте количество ионов NO
составляла 6 мг/л. Содержание воды во
влажной почве – 26 г/100 г абс. сухой почвы.
Рассчитайте количество ионов NO![]() в почве в миллиграммах на килограмм
абс. сухой почвы (мг/кг). Какова концентрация
нитрата в почвенном растворе? Рассчитайте
количество ионов NO
в почве в миллиграммах на килограмм
абс. сухой почвы (мг/кг). Какова концентрация
нитрата в почвенном растворе? Рассчитайте
количество ионов NO![]() в верхнем слое почвы (2500 т/га) в килограммах
на гектар (кг/га).
в верхнем слое почвы (2500 т/га) в килограммах
на гектар (кг/га).
Решение.
В качестве первого шага определим
количество нитратов (mNO![]() ),
которое было экстрагировано:
),
которое было экстрагировано:
mNO![]() =VэС
NO
=VэС
NO![]() ,
,
где Vэ – объем экстрагента, л;
С
NO![]() – изморенная
концентрация нитратов, г/л;
– изморенная
концентрация нитратов, г/л;
mNO![]() = 200 ·
10–3
– 6 ·
10–3
= 1,2 ·
10–3
(г).
= 200 ·
10–3
– 6 ·
10–3
= 1,2 ·
10–3
(г).
Далее пересчитаем взятый образец влажной почвы на абсолютную сухую почву. Исходим из следующей пропорции:
126 г влажной почвы содержит 100 г абс. сухой почвы
50 г влажной почвы содержит X г абс. сухой почвы.
Таким образом, количество абсолютно сухой почвы в 50 г влажной почвы составит:
X
=![]() .
.
В 1кг абс. сухой
почвы будет содержаться ионов NO![]() :
:
![]() .
.
![]() 0,030 (г
0,030 (г
![]() /кг абс. сухой почвы) =
/кг абс. сухой почвы) =
= 30 (мг
![]() /кг абс. сухой почвы).
/кг абс. сухой почвы).
Примем, что объем
почвенного раствора равен объему воды,
присутствующей во влажной почве. Таким
образом, концентрация нитратов в
почвенном растворе (С![]() )
составит:
)
составит:
С![]() =
=![]() ,
,
где ρ – плотность почвенного раствора, для упрощения в этой задаче принятая равной 1 кг/л;
![]() .
.
Общее количество
нитратов М![]() ,
содержащееся на 1 гапочвы,
может быть определено следующим образом:
,
содержащееся на 1 гапочвы,
может быть определено следующим образом:
М![]() =
=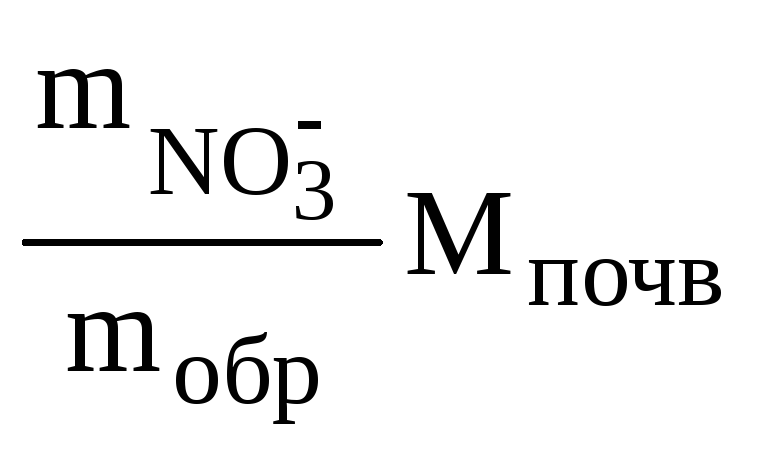 ,
,
где Мпочв – масса почвы на площади 1га;
mобр – масса навески почвы (50г);
m![]() – содержание нитратов в почве;
– содержание нитратов в почве;
М![]() =
=![]()
Ответ:
в 1кг абс. сухой почвы содержится 30 мг
NO![]() ;
содержание NO
;
содержание NO![]() в почвенном растворе – 0,12 г/л; содержание
NO
в почвенном растворе – 0,12 г/л; содержание
NO![]() в верхнем слое почвы – 60 кг/га.
в верхнем слое почвы – 60 кг/га.
10. Соединения фосфора в почве
Общее количество фосфора в верхнем слое почвы в среднем составляет около 1000 кг · га–1. Главный источник его поступления – почвообразующие породы, некоторая незначительная часть поступает с атмосферными осадками. Ежегодно с урожаем сельскохозяйственных растений из почвы выносится от 10 до 40 кг · га–1 фосфора. Поэтому значительные количества его соединений дополнительно вносятся в почву с органическими и минеральными удобрениями. Соединения фосфора в почве содержатся в почвенном растворе, находятся в адсорбированном состоянии на поверхности неорганических компонентов почвы, присутствуют в твердой фазе почв в виде аморфных и кристаллических минералов и входят в состав органических соединений почвы.
В зависимости от вида почв содержание фосфора в органических соединениях изменяется от 10-20% (дерново-подзолистые почвы) до 70-80% (черноземные почвы) от его общего содержания в почвенном слое. Основное количество (до 60%) органических соединений фосфора во многих почвах находится в виде инозитолфосфатов, которые представляют собой эфиры ортофосфорной кислоты и насыщенного шестиатомного циклического спирта – циклогексангексола, или инозита. В результате присоединения к инозиту шести молекул ортофосфорной кислоты образуется 12 – основная инозитгексафосфорная кислота. При неполном фосфорилировании возникают цента-, тетра-, три-, ди- и моноинозитолфосфаты.
В составе гуминовых и фульвокислот может находиться от 2-3 до 50-80% всего фосфора, содержащегося в органической части почв. Его концентрация в гуминовых кислотах колеблется от 0,03-0,05 до 0,3-0,5%. Часть этого фосфора представлена также инозитолфосфатами.
Около 1% фосфора органической части почв сосредоточено в липидах, 2-3% – в нуклеиновых кислотах. Помимо этих соединений в почве идентифицированы фосфопротеины, сахарофосфаты и фосфорилированные карбоновые кислоты. Фосфаты принимают участие и в образовании органоминеральных соединений в почве, в этом случае ортофосфаты, например, могут быть связаны с органическими соединениями через катионные мостики железа, алюминия или кальция.
Минеральная часть твердой фазы почв представлена в основном ортофосфатами, преимущественно минералами апатитовой группы. Кроме них распространены минералы группы плюмбогумита РbАl3Н(ОН)6(РО4)2, на долю которых в некоторых видах почв приходится до 50% от всей массы минерального фосфора, вавеллита Аl(РО4)4(ОН)6 · 5Н2О и вивианита Fe3(PO4)2 · 8H2O. Все встречающиеся в почве ортофосфаты относятся к труднорастворимым соединениям (таблица 10).
Трансформация соединений фосфора в почве связана с протеканием процессов минерализации органических фосфорсодержащих веществ, а также процессов иммобилизации, фиксации и мобилизации его неорганических соединений.
Минерализация – процесс превращения органических соединений фосфора и минеральные. Этот процесс протекает в почве в результате деятельности микроорганизмов. При этом под воздействием различных ферментов, например, фитаз, происходит выделение из органических веществ остатков ортофосфорной кислоты. Последующие их превращения будут определяться свойствами почвенного раствора и составом твердой фазы почв.
Таблица 10. Основные представители ортофосфатов кальция в почвах
|
Вещество |
Формула |
рК = – lg К |
|
Гидрофосфат кальция |
СаНРО4 |
6,66 |
|
Фосфат кальция |
-Са3(РО4)2 |
33,21 |
|
Ортофосфат кальция |
Са3(РО4)23Н2О |
146,9 |
|
Гидроксилапатит |
Са10(РО4)6(ОН)2 |
113,7 |
|
Фторапатит |
Ca10(PО4)6F2 |
18,4 |
Иммобилизация – превращение неорганических соединений фосфора в органические формы в процессе развития живых организмов. При этом фосфор переходит, например, в молекулы фосфолипидов или нуклеиновых кислот микробных клеток и в форме органических фосфорсодержащих соединений становится недоступным для других организмов.
Фиксация фосфора – переход растворимых фосфорных соединений в менее растворимое состояние за счет образования прочных связей с минеральными компонентами почвы. Фиксация протекает в результате образования труднорастворимых минералов и в процессе хемосорбции фосфат-ионов из почвенного раствора. Хемосорбция осуществляется в результате связывания фосфат-ионов с ионами Al, Fe или Са, которые находятся на поверхности минералов. В случае взаимодействия фосфат-ионов с катионами железа, алюминия или кальция, присутствующими в растворе, возможно образование и выпадение малорастворимых соединений.
Мобилизация – увеличение подвижности соединений фосфора, связанное с превращением труднорастворимых соединений в более растворимые, или переход их в почвенный раствор. Для большинства почв главный путь мобилизации связан с переходом соединений кальция из трикальцийфосфата в гидрофосфат или дигидро-фосфат кальция:
Са3(РО4)2 СаНРО4 Са(Н2РО4)2. (28)
Эти превращения протекают в присутствии свободных кислот, образующихся, в частности, при трансформации компонентов почв. Для оценки возможного перехода фосфатов из твердой фазы почв в почвенный раствор на практике часто используют величину фосфатного потенциала почв (ФП). Фосфатный потенциал почв характеризует степень равновесности почвенного раствора по отношению к дигидрофосфату кальция:
ФП = –lg(![]() (29)
или ФП = 0,5р(Са2+)
+ р(Н2РО
(29)
или ФП = 0,5р(Са2+)
+ р(Н2РО![]() ),
(30)
),
(30)
где
р(Са2+)
= – lgaCa2+),
p(H2PO![]() )
= –lg
)
= –lg![]() .
.
Сравнивая величину фосфатного потенциала с отрицательным логарифмом корня квадратного из произведения растворимости дигидрофосфата кальция, можно сделать вывод о вероятном поведении соединений фосфора. Так, если для почв соблюдается неравенство
0,5р(Са2+)
+ р(Н2РО![]() )
> –lg
)
> –lg![]() (31)
(31)
то концентрация фосфат-ионов в растворе контролируется соединениями, более трудно растворимыми, чем Ca(H2PO4)2. Если наблюдается равенство
0,5р(Са2+)
+ р(Н2РО![]() )
= –lg
)
= –lg![]() ,
(32)
,
(32)
то растворяется преимущественно монокальцийфосфат. Чем выше фосфатный потенциал, тем труднее переходит фосфор в почвенный раствор, тем менее благоприятные условия создаются для питания растений фосфором.
