
- •Содержание
- •1. Введение.
- •1.1 Общие закономерности химических процессов. Классификация процессов общей химико-технологических процессов
- •Требования к химическим производствам
- •Компоненты химического производства
- •Разделение на две твердые фазы:
- •Разделение жидкости и твердого вещества:
- •1.2 Промышленный катализ
- •Основные положения теории катализа.
- •1.3. Сырьевая база химической промышленности.
- •Классификация сырья
- •Характеристика минерального сырья
- •Химическое сырье
- •Растительное и животное сырье
- •Характеристика разработок минерального сырья
- •Качество сырья и методы его обработки
- •Способы сортировки:
- •Способы обогащения:
- •Сырьевая база химических производств
- •1.4 Энергетическая база химических производств
- •1.5 Критерии оценки эффективности производства
- •1.5.1. Интегральные уравнения баланса материальных потоков в технологических процессах. Понятие о расходных коэффициентах. Относительный выход продукта
- •1.5.2. Балансы производства
- •1. Материальный баланс
- •2. Энергетический (тепловой) баланс
- •3. Экономический баланс
- •1.5.3. Технологические параметры химико-технологических процессов.
- •1.6.Принципы создания ресурсосберегающих технологий
- •2. Теоретические основы химической технологии
- •2.1. Энергия в химическом производстве. Тепловой эффект реакции в технологических расчетах. Направленность реакции в технологических расчетах
- •2.2 Массообменные процессы. Основные принципы массообменных процессов. Моделирование процессов теплообмена.
- •Молекулярная диффузия. Первый закон Фика
- •Турбулентная диффузия
- •Уравнение массоотдачи
- •Уравнение массопередачи
- •Связь коэффициента массопередачи и коэффициентов массоотдачи (или уравнение аддитивности фазовых сопротивлений)
- •Подобие массобменных процессов
- •3. Химическое производство как сложная система. Иерархическая организация процессов в химическом производстве
- •3.1. Химико-технологические системы (хтс). Элементы хтс. Структура и описание хтс. Методология исследования хтс, синтез и анализ хтс.
- •Методология исследование химико-технологических систем.
- •3.2. Сырьевая и энергетическая подсистема хтс
- •1. Классификация химических реакторов по гидродинамической обстановке.
- •2. Классификация химических реакторов по условиям теплообмена.
- •3. Классификация химических реакторов по фазовому составу реакционной массы.
- •4. Классификация по способу организации процесса.
- •5. Классификация по характеру изменения параметров процесса во времени.
- •6. Классификация по конструктивным характеристикам.
- •3.4. Промышленные химические реакторы. Реакторы для гомогенных процессов, гетерогенных процессов с твердой фазой, гетерогенно-каталитических процессов, гетерофазных процессов.
- •Реакторы для гетерогенных процессов с твердой фазой.
- •Реакторы для гетерогенно-каталитических процессов.
- •4. Основные математические модели процессов в химических реакторах
- •4.1. Идеальные химические реакторы. Непрерывный реактор идеального вытеснения. Непрерывный реактор идеального смешения
- •4.2. Сравнение эффективности проточных реакторов идеального смешения и идеального вытеснения. Обоснование использования каскада реакторов.
- •Каскад реакторов смешения.
- •Влияние степени конверсии.
- •Влияние температуры.
- •5. Применение кинетических моделей для выбора и оптимизации условий проведения процессов
- •5.1. Экономические критерии оптимизации и их применение для оптимизации реакционных узлов.
- •Оптимальные концентрации инициатора и температуры в радикально-цепных реакциях
- •Оптимизация степени конверсии.
- •7. Важнейшие промышленные химические производства
- •7.1 Проблема фиксации атмосферного азота. Синтез аммиака, Физико-химические основы производства и обоснование выбора параметров и типа реакционного узла. Технологическая схема процесса.
- •Синтез аммиака
- •Сырье для синтеза аммиака.
- •Технология процесса.
- •Основные направления в развитии производства аммиака.
- •7.2. Получение азотной кислоты. Физико-химические основы химических стадий процесса, обоснование выбора параметров и типа реакторов. Технологическая схема процесса.
- •Физико-химические основы процесса.
- •Контактное окисление аммиака.
- •Обоснование роли параметров и их выбор.
- •Окисление оксида азота (II) до диоксида.
- •Абсорбция диоксида азота.
- •Технология процесса.
- •7.3. Производство минеральных удобрений. Классификация минеральных удобрений
- •Классификация минеральных удобрений.
- •7.3.1. Азотные удобрения. Физико-химические основы производства нитрата аммония. Устройство реакционного узла. Теоретические основы процесса и его технологическое оформление
- •Производство нитрата аммония.
- •7.3.2. Производство фосфорной кислоты. Физико-химические основы процесса. Технологическая схема
- •Функциональная схема производства эфк.
- •Сернокислотное разложение апатита.
- •7.3.3. Фосфорные удобрения. Физико-химические основы процессов их производства. Типы реакционных узлов.
- •Производство простого суперфосфата.
- •Производство двойного суперфосфата
- •Азотнокислое разложение фосфатов. Получение сложных удобрений
- •Обжиг серосодержащего сырья.
- •Обоснование роли параметров и их выбор.
- •Сжигание серы.
- •Окисление диоксида серы.
- •Обоснование роли параметров и их выбор.
- •Технология контактного окисления so2.
- •Абсорбция триоксида серы.
- •Перспективы развития сернокислотных производств.
- •7.5. Электрохимические производства. Теоретические основы электролиза водных растворов и расплавленных сред. Технология электролиза раствора хлорида натрия.
- •Основные направления применения электрохимических производств
- •Электролиз раствора хлорида натрия
- •Электролиз раствора NaCl с твердым катодом и фильтрующей диафрагмой
- •Электролиз раствора хлорида натрия с ртутным катодом
- •7.6. Промышленный органический синтез
- •Первичная переработка нефти.
- •Каталитический риформинг углеводородов.
- •7.6.2. Производство этилбензола и диэтилбензола. Теоретические основы процесса и обоснование выбора условий процесса. Технология процесса
- •7.6.3. Синтезы на основе оксида углерода. Производство метанола. Теоретические основы процесса.
- •Окисление изопропилбензола (кумола)
- •Технологическая схема получения фенола и ацетона кумольным способом.
- •7.6.5. Биохимические производства. Особенности процессов биотехнологии.
- •7.6.5.1. Производство уксусной кислоты микробиологическим синтезом
- •7.6.5.2. Производство пищевых белков
- •8. Химико-технологические методы защиты окружающей среды
- •8.1. Утилизация и обезвреживание твердых отходов
- •8.2. Утилизация и обезвреживание жидких отходов
- •8.3. Обезвреживание газообразных отходов
1.5.1. Интегральные уравнения баланса материальных потоков в технологических процессах. Понятие о расходных коэффициентах. Относительный выход продукта
К основным показателям ХТП относятся расходные коэффициенты, характеризующие затраты сырья, воды, топлива, электроэнергии, пара на единицу массы целевого продукта. В связи с большим вкладом затрат на реагенты (сырье) в себестоимость продуктов в химической технологии особое значение имеют расходные коэффициенты по реагентам. Различают теоретические и практические расходные коэффициенты.
Теоретический расходный коэффициент стех рассчитывают, пользуясь стехиометрическим уравнением, описывающим химическое превращение:




![]()

где ![]() и
и
![]() - массы реагента и продукта из уравнения
реакции
- массы реагента и продукта из уравнения
реакции
MA и MP - молекулярные массы реагента и продукта
а и р - стехиометрические коэффициенты.
Теоретический расходный коэффициент характеризует минимальный расход сырья на единицу массы продукта.
Практический
расходный коэффициент
отражает реальный расход поступившего
в процесс сырья на единицу массы продукта,
т.е. его рассчитывают как отношение
массы поступившего в процесс сырья
![]() к массе получившегося продукта GР:
к массе получившегося продукта GР:
![]()
Расходные коэффициенты рассчитывают по всем реагентам. Практические расходные коэффициенты всегда больше стехиометрических из-за неполноты превращения сырья, а также из-за расходования сырья на побочные реакции. Данные для расчета практических расходных коэффициентов берут из материального баланса процесса. Практический расходный коэффициент по реагенту можно найти, зная теоретический расходный коэффициент и выход целевого продукта по этому реагенту:

где
![]() - выход Р по реагенту А в долях единицы.
- выход Р по реагенту А в долях единицы.
Выход продукта – отношение количества практически получаемого продукта к теоретически возможному (выход по сырью).
![]()
Gт – определяют из равновесного превращения исходного вещества или по полному превращению исходного сырья в продукт (исключается образование побочных продуктов).
Для простых реакций выход по сырью прямопропорционален общей концентрации.
Для уравнения (1) выходы продукта Р на реагенты А и В выражаются формулами .
![]()
![]()
где
![]() ,
,![]() и
и
![]() количества молей продукта Р, полученное
в реакции (1), и реагентов А и В, введенные
в реакционную систему, соответственно,
а, b
и p –
стехиометрические коэффициенты реакции
(1).
количества молей продукта Р, полученное
в реакции (1), и реагентов А и В, введенные
в реакционную систему, соответственно,
а, b
и p –
стехиометрические коэффициенты реакции
(1).
Определения
выхода для реагента А в двух видах


Выражение
![]() в формуле – это количество молей
реагента А, из которого образуется NP
молей продукта Р в соответствии с
уравнением (1) и т.д.
в формуле – это количество молей
реагента А, из которого образуется NP
молей продукта Р в соответствии с
уравнением (1) и т.д.
Выход можно рассчитывать для каждого из продуктов по любому из реагентов (а если необходимо, то и по всем реагентам основной реакции). Чаще выход рассчитывают для наиболее ценного (целевого) продукта на наиболее дорогой из реагентов.
Пример: синтез метанола из синтез-газа наряду с основной идут побочные реакции.
СО + 2Н2 = СН3ОН основная
2СО + 2Н2 = СН4 + СО2
СО + 3Н2 = СН4 + Н2О
2СН3ОН = СН3ОСН3 + Н2О
Выход метанола (ηCH3OH) в соответствии со стехиометрией уравнения по оксиду углерода(II) рассчитывают по формуле, а по водороду – по формуле.


где
![]() –
полученное количество молей метанола,
–
полученное количество молей метанола,
![]() и
и
![]() –
введенные в систему количества молей
СО и Н2.
–
введенные в систему количества молей
СО и Н2.
Аналогичным образом может быть рассчитан выход по каждому из побочных продуктов. Практический выход не может превышать равновесный выход при условиях проведения процесса.
Для процессов, в которых трудно выделить одну стехиометрическую реакцию образования целевого продукта, и поэтому нельзя рассчитать выход описанным способом, рассчитывают показатель, который также называют выходом или массовым выходом и который представляет собой отношение массы полученного продукта к массе затраченного сырья. Например, выход этилена для процесса пиролиза фракций нефти находят как отношение массы этилена к массе поступившей в реактор фракции нефти.
Пример 1: При термическом разложении не загрязненного примесями карбоната кальция образовалось 8,00 г оксида кальция. Известно, что реакция прошла с выходом 85,0%. Вычислите массу карбоната кальция, взятого для проведения реакции разложения и объем (н.у.) образовавшегося углекислого газа.
Пример 2: Реакция синтеза иодоводорода из простых веществ при определенных условиях проходит с выходом 35,0%. Вычислите, какую массу технического цинка, содержащего 2,50% примесей, нужно обработать избытком соляной кислоты, чтобы из полученного водорода получить, в конечном счете 1,00 л (н.у.) иодоводорода.
Селективность – важнейший показатель сложного ХТП, характеризующий эффективность превращения сырья в целевой продукт. Селективность образования продукта по реагенту (φ) – это отношение количества этого реагента, превратившегося в продукт, к общему количеству превратившегося реагента. В отличие от выхода, селективность не учитывает не превратившийся реагент, поэтому этот показатель более чувствителен к соотношению различных направлений химического превращения. Для реакции (1) селективность образования продукта Р по реагентам А и В выразится формулами, в знаменателе которых, в отличие от формул для выхода, количество превращенного реагента. Символом N обозначены мольные количества веществ или мольные потоки (для открытых систем, работающих в стационарном режиме).
![]() интегральная селективность
интегральная селективность
![]()
Селективность – это отношение количества полученного практически продукта, к количеству этого продукта, которое должно было быть получено из прореагировавшего количества реагента в соответствии со стехиометрией реакции, по которой образуется этот продукт. Если продукт образуется по нескольким реакциям, то селективность, как правило, рассчитать нельзя.
Дифференциальной
селективностью
(![]() )
образования продукта Р по
реагенту А - это отношение скорости
расходования реагента А на образование
продукта Р к суммарной скорости
превращения А. Рассчитывают дифференциальную
селективность как отношение скоростей
образования продукта и расходования
реагента, умноженное на обратное
отношение стехиометрических коэффициентов.
)
образования продукта Р по
реагенту А - это отношение скорости
расходования реагента А на образование
продукта Р к суммарной скорости
превращения А. Рассчитывают дифференциальную
селективность как отношение скоростей
образования продукта и расходования
реагента, умноженное на обратное
отношение стехиометрических коэффициентов.
![]() в уравнении -
скорость расходования А на образование
Р.
в уравнении -
скорость расходования А на образование
Р.
![]()
Пример: для реакции синтеза метанола интегральную селективность образования метанола по СО и по Н2 рассчитывают по формулам:


Взаимосвязь степени превращения реагента, выхода и интегральной селективности образования продукта по этому реагенту получают, перемножив выражения для степени превращения и селективности. Сократив одинаковые члены в числителе и знаменателе, получим:
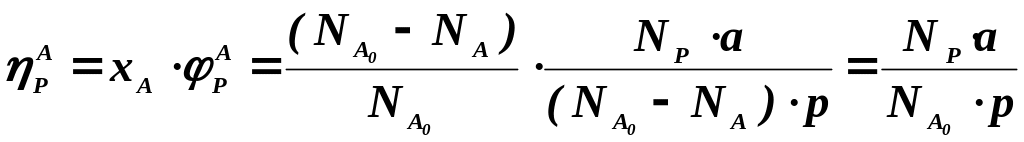
Для простых ХТП селективность равна
единице (100%) для всех продуктов единственной
реакции (стехиометрического уравнения).
В этом случае выход каждого из продуктов
реакции по любому из реагентов равен
степени превращения этого реагента
(![]() ).
).
В случае сложных ХТП для получения высокого выхода необходимо иметь высокие значения и степени превращения, и селективности. Если процесс протекает с полным превращением реагента, то выход продуктов по этому реагенту равен селективности образования каждого из продуктов по данному реагенту.
Например, в контактном окислении аммиака весь поступающий в процесс аммиак реагирует, превращаясь в оксид азота и побочные продукты. Выход оксида азота в этом случае равен селективности образования NO по аммиаку.
Количество готовой продукции – должно удовлетворять требованиям ГОСТ и характеризуется содержанием основного вещества и посторонних примесей и зависит в первую очередь от характера побочных реакций и степени очистки исходных и конечных продуктов.
Производительность аппарата П – количество готового продукта фактически вырабатываемого данным аппаратом в единицу времени при данном расчете процесса производства. Производительность: кг/ч; т/сутки; тыс т./сутки
![]() (кг/ч, т/ч, м3/ч)
(кг/ч, т/ч, м3/ч)
где G – масса (или объем) продукта, полученная за время t
Мощность – максимальная производительность аппаратуры
![]()
Интенсивность работы процесса или аппарата – производительность отнесенная к единице полезного объема или рабочей поверхности аппарата. Обычно производительность относят к объему аппарата V или к площади его сечения S:
![]() (кг/м3ч),
(кг/м3ч),
![]() (кг/м2ч)
(кг/м2ч)
В каталитических процессах рассчитывают интенсивность работы катализатора, для чего массу полученного за единицу времени целевого продукта относят к объему катализатора Vk:
![]() (кг/мk3ч)
(кг/мk3ч)
Производительность труда – количество вырабатываемой продукции в единицу времени на одного рабочего.
увеличение интенсивности труда
увеличение интенсивности процесса:
- рационализация
- введение более совершенных методов
- увеличение количества сырья
- уровень технической культуры
Себестоимость продукции – это сумма затрат в денежном выражении на единицу продуктов в конкретном производстве. (заготовка и хранение сырья и топлива, оплата труда работников, оплата энергии, амортизация оборудования и помещений). Себестоимость тем ниже, чем выше производительность.
