
Техническая термодинамика. Булыгин Ю.А., Кретинин А.В
.pdfЮ.А. БУЛЫГИН, А.В. КРЕТИНИН
ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА
Учебное пособие
Воронеж 2003
Министерство образование Российской Федерации Воронежский государственный технический университет
Ю.А. БУЛЫГИН, А.В. КРЕТИНИН
ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА
Утверждено редакционно-издательский совотом университета в качестве учебного пособия
Воронеж 2003
УДК 621.1.016.7
Ю.А. Булыгин, А.В. Кретинин Техническая термодинамика; Учеб. пособие. Воронеж ; Воронеж. гос. техн. ун-т, 2003, 158 с.
Учебное пособие включает в себя основные сведения технической термодинамики о законах взаимопревращения теплоты и работы и способствует лучшему усвоению изучаемого материала студентами. Издание соответствует рабочей программе и предназначено для специальности 134000 «Ракетные двигатели».
Табл. 10. Ил. 136. Библиогр. 14 назв.
Научный редактор доктор техн. наук, проф. С.Г. Валюхов.
Рецензенты: кафедра математического моделирования Воронежского государственного университете (зав. кафедрой доктор техн. наук, профессор В.А. Костин); главный конструктор КБ химавтоматики, доктор техн. наук, профессор А.Ф. Ефимочкин.
сБулыгин Ю.А., Кретинин А.В., 2003
сОформление. Воронежский государственный технический университет, 2003
3
ВВЕДЕНИЕ
Развитие народного хозяйства требует всѐ более рационального использования тепловых ресурсов нашей страны, создания более экономичных тепловых установок, двигателей, компрессоров и холодильных машин. Решение этого вопроса во многом зависит от глубины знания и понимания основы теории тепловых машин - технической термодинамики инженерами нашей промышленности, создающими и использующими эту технику. Поэтому будущий специалист ещѐ в студенческой аудитории должен быть настроен на оригинальное, поисковое решение научно-технических задач. Этим объясняется и выбор дедуктивного метода изложения материала: от общих идей и закономерностей (показав пути их реализации, достигнутые результаты и оставшиеся возможности) к проблемной информации. Общеэнергетическую направленность и теоретическую основу курса определяет термодинамика - логическая наука, занимающаяся изучением законов взаимопреобразования и передачи энергии. Термодинамика позволяет установить, в каком направлении могут протекать различные физические и химические процессы в тех или иных системах, непосредственно не оперируя какими-либо моделями строения вещества. В основу термодинамики положены два основных начала (закона), установленных опытным путѐм, используя которые можно получить все основные выводы термодинамики.
Слово "термодинамика" греческого происхождения: "терме" означает тепло, жар, огонь, "динамикос" - силу, движение, а всѐ вместе "движущую силу тепла (огня)". Впервые это словосочетание было применено на французском языке Сади Карно в 1824 г. в работе "Размышления о движущей силе огня и машинах, способных развивать эту силу", с которой и началось развитие термодинамики. Таким образом, термодинамика возникла как теория теплового двигателя. Первое упоминание об использовании "движущей силы огня" относится к 1 в. до н. э., когда Герон Александрийский построил различные паровые машины - игрушки, лучшей из которых являлся Эолопил (Эол - бог ветра). Он представлял собой полый металлический шар с впаянными в него на противоположных полушариях открытыми трубками, загибавшимися в разные стороны. В шар наливалась вода и подогревалась до кипения. Образовавшийся пар выбрасывался из трубок, создавая реактивные силы, под действием которых шар вращался в трубчатых опорах. Прообраз реактивно - турбинного двигателя. Впрочем, ещѐ ранее (во 2 в. до н. э.) Филон из Византии демонстрировал прибор, состоящий из шара с водой и сосуда, соединѐнных трубкой. На солнце воздух расширялся и вытеснял воду из шара, а в тени вода из сосуда возвращалась в шар. В 1597 г. в Падуанском университете Галилео Галилей изготовил первый термоскоп. Гениальная идея Галилея - судить об изменениях температуры по другим измеряемым измерениям в телах - позволила в дальнейшем сконструировать различные термометры. О некоторых из них и температурных шкалах мы поговорим позднее. В средние века господствовали идеалистические представления о природе, явления которой объяснялись не движением материи, а перетеканием в ней особых невесомых жидкостей: нагрев и охлаждение тел объяснялись протеканием теплорода, а горение - перетеканием флогистона, электрические явления - перетеканием особой электрической жидкости и т.п. Наука тогда отставала от практики, и прогресс определялся успехами изобретателей - эмпириков. В 1681г. ассистент физика X. Гюйгенса врач и механик Дени Папен изобретает паровой котел, снабжѐнный предохранительным клапаном, позволяющим регулировать давление пара. Гюйгенс взрывал порох на дне цилиндра под поршнем, который возвращался обратно под действием атмосферного явления. Таким образом, родились два принципа - атмосферной паровой машины и двигателя внутреннего сгорания. В 1690 г. Папен заменил порох водой, подогреваемой до образования пара, после чего он конденсировался вследствие обливания цилиндра холодной водой или впрыскиванием еѐ внутрь.
4
Проблема откачки воды из шахт привела к созданию паровытеснительных насосов, не имеющих движущихся частей, англичанином Эдуардом Сомерсетом (в 1698 г. на это изобретение получил патент Томас Сэвери). В 1705-1712 г.г. английский слесарь Томас Ньюкомен разработал паропоршневые насосы, в которых пар приготавливался в отдельном котле, а поршневой двигатель был отделѐн от откачивающего воду поршневого насоса. Система клапанов регулировала поступление пара и воды в цилиндры. Последняя из этих машин была демонтирована в Англии в 1934г. Историки утверждают, что уже в 1717 г. фонтаны Летнего сада в Петербурге приводились в действие паровой (атмосферной) машиной, сконструированной Жаном-Теофилем Дезагюлье по заказу Петра 1. В 1793 г. русский инженер И. И. Ползунов предложил, а к 1766 г. построил универсальную машину, которая работала на угле, холостой ход исключался с помощью двух цилиндров, работавших на общий вал, парораспределение было автоматическим. Изобретатель умер в 38 лет перед пуском машины и она после небольшой поломки была забыта. В 1769 г. англичанин Джеймс Уатт впервые применил такой элемент как конденсатор и использовал в качестве движущей силы давление упругости пара, подаваемого сверху поршня. В 1782 г. Уатт ввел двойное действие (пар поочерѐдно поступал сверху и снизу поршня), золотниковое парораспределение, преобразование поступательновозвратного движения во вращательное, а в 1788 г. - центробежный регулятор оборотов. Схема установки стала почти современной.
Уже к 1775 г. обилие подаваемых заявок на изобретение различных двигателей, в том числе и "вечных", привело к тому, что Парижская Академия наук первой в мире принимает решение их больше не рассматривать.
В 1801 г. француз Ф. Лебон патентует поршневой двигатель, работающий уже на горючих газах от сухой перегонки древесины с зажиганием их электрической свечой и сгоранием внутри цилиндра. В 1805 г. швейцарец И. Риваз предлагает двигатель на водороде. В 1816 г. английский священник Р. Стирлинг получает патент на универсальную тепловую машину, состоящую из цилиндра с двумя по-разному двигающимися поршнями и регенератора-теплообменника и способную работать на разных топливах как двигатель внешнего сгорания, как холодильник и как тепловой насос (отопитель). В настоящее время эта машина перспективна. В 1824 г. основоположник термодинамики С. Карно предсказывает рабочий цикл четырѐхкратного двигателя внутреннего сгорания (ДВС). В 1860 г. французский механик Ж. Ленуар начинает строить и продавать ДВС, работающий на светильном газе, но без предварительного сжатия воздуха, что ограничило их к.п.д. 3-6 % (как у паровых машин).
И только в 1877 г. немецкий изобретатель-коммерсант Н. Отто создаѐт, наконец, четырѐхкратный ДВС с искровым зажиганием и к.п.д. 16-20 %. В 1892-1897 г.г. немецкий инженер Р. Дизель разрабатывает компрессорный с воспламенением от предварительно сильно сжатого в цилиндре воздуха ДВС, оказавшийся самым экономичным. В 1904 г. в России Г.В. Тринклер создаѐт менее громоздкий и ещѐ более экономичный бескомпрессорный дизель.
Следует выделить изобретение англичанином Ч. Парсонсом в 1824 г. паровой реактивной многоступенчатой турбины. В 1889 г. шведский инженер Г. Лаваль получает в Англии патент на расширяющееся сопло, которое позволяет в отличие от суживающегося превращать в кинетическую энергию потока высокие перепады давления пара. В 1891 г. паротурбинный двигатель (ПТД) снабжается конденсатором, что делает его более экономичным, чем поршневой, при сохранении превосходства над последним и в удельной мощности - основной двигатель электростанций.
Первый газо(паро)турбинный двигатель (ГТД) с процессом горения при постоянном давлении - спроектировал и построил русский инженер П. Д. Кузьминский в 1897 г. В 1906 г. В.В. Караводин разработал, а в 1908 г. построил и испытал более экономичный ГТД - с пульсирующим процессором (горением при постоянном объѐме). В настоящее время широко используются возможности прямого превращения химической и
5
тепловой энергии в электрическую. Разрабатываются и используются энергетические установки на радиоактивных дорогостоящих изотопах, топливные элементы, термоэлектрогенераторы, магнитогазодинамические электрогенераторы, солнечные электрогенераторы. Такова хронология истории теплоэнергетики на практических примерах. Обзор теоретических исследований следует начать с определения всех явлений
вприроде как различных форм движения материи, которое принадлежит нашему великому соотечественнику, гениальному учѐному - материалисту М.В. Ломоносову. В 1746 г. он сформулировал единый всеобщий закон сохранения материи и энергии: "Все перемены в натуре случающиеся такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому. Так ежели где убудет несколько материи, то умножится в другом месте. Сей всеобщий естественный закон простирается и в самые правила движения: ибо тело, движущее своей силой другое столько оныя у себя теряет, сколько сообщает другому". В 1750 г. физик Георг Рихман заложил основы калориметрии, что в дальнейшем привело к разделению понятия теплоѐмкости и скрытой теплоты. Только через 16-20 лет после Ломоносова французский химик Лавуазье подтвердил закон сохранения материи, и только через 100 лет был окончательно утверждѐн закон сохранения энергии, в основном, благодаря трудам Роберта Майера, Джеймса Джоуля, Германа Гельмгольца, русских академиков Г.И. Гесса и Э.Х. Ленца.
Наблюдения за работой паровых машин показали неравноценность превращения теплоты в механическую работу и обратно, что побудило гениального французского инженера Сади Карно к опубликованию в 1824 г. труда "Размышление о движущей силе огня и о машинах, способных развивать эту силу". В нѐм содержались, хотя и полученные с помощью теории "теплорода", оба начала термодинамики, и еѐ основные понятия, и идеальный цикл тепловых машин, и разработка схемы работы ДВС.
Лишь через 10 лет, после издания "Мемуара о движущей силе теплоты" Б. Клапейрона, эта работа стала почти сенсацией. Клапейрон "перевѐл" еѐ на математический язык, вскрыв великое содержание этого труда, и первым применил графический метод исследования работы тепловых машин - метод циклов. В 1853 г. Виллиам Томсон (лорд Кельвин) даѐт первое точное определение энергии. Рудольф Клаузиус формулирует уже на основе механической теории тепла два начала термодинамики и получает знаменитое выражение к.п.д. идеального цикла Карно при наличии двух источников тепла разной температуры. В 1855-1865 г.г. вводятся понятия обратимых и необратимых процессов и энтропии (Клаузиусом) - величины, рост которой
внеобратимых процессах характеризует ту часть энергии тел, которая не может быть превращена в работу, а рассеивается в виде теплоты. Строго систематически - второй закон термодинамики был обоснован австрийским физиком Людвигом Больцманом в 1877 г. Здесь же следует отметить работы М. Смолуховского и профессора Киевского университета Н.Н. Шиллера.
Отечественные учѐные внесли большой вклад в дело развития основ термодинамики: труды А.Г Столетова и М.П. Авенариуса, работавших в области изучения веществ в критическом состоянии; работы Д.П. Коновалова и Л.Г. Богаевского по вопросу об упругости насыщенных паров смесей жидкостей.
Значительные успехи в теории тепловых двигателей связаны с именами выдающихся отечественных учѐных И.П. Алымова, М.Ф. Окатова, Л.К. Попова, И.А. Вышнеградского, В.И. Гриневецкого, Л.К. Рамзина.
Особо следует отметить работы советских учѐных М.П. Вулкаловича, В.А. Кириллина, И.И. Новикова в МЭИ; Д.А.Тимрота, Н.Б. Варгафтика в
ВТИ; учѐных ЦКТИ им. И.И. Ползунова, ЭНИНа им. Г.М. Кржижановского, ЦАГИ и ряда других институтов.
Теперь уже теория освещает путь практике, служит указателем направлений и пределов совершенствования энерготехники. В 50-х годах прошлого столетия был разработан новый раздел термодинамики -термодинамика необратимых процессов;

6
получает развитие термодинамика плазмы. Тщательного изучения требуют вопросы термодинамических свойств и процессов реагирующих газовых смесей, течения диссоциированных газовых смесей, ионизированных газов и др.
Термодинамические параметры состояния.
Известно, что вещества обычно пребывают в одном из трѐх состояний: в виде газа, жидкости или твѐрдого тела. Четвѐртое состояние - плазма (ионизированный газ) в этом курсе мы рассматривать не будем. В заданных неизменных условиях конкретное вещество всегда будет находиться в одном и том же состоянии. Чтобы однозначно определить состояние рассматриваемого вещества вводятся так называемые параметры состояния. Параметры, не зависящие от размеров системы (части материи, выделенной для исследования), например температуру, давление, называют интенсивными, зависящие же, например объем, - экстенсивными. Удельные, то есть отнесѐнные к единице количества вещества, экстенсивные свойства (удельный объѐм, удельная теплоѐмкость и т.п.) приобретают смысл интенсивных свойств. Интенсивные свойства, определяющие состояние термодинамической системы, называют термодинамическими параметрами состояния. За основные из них приняты наиболее удобные: абсолютное давление Р, удельный объем и абсолютная температура Т.
Абсолютным давлением р называется сила Р, действующая по нормали к поверхности тела и отнесѐнная к единице площади F этой поверхности
p FP
Давление газа на стенки-сосуда есть результат ударов о них молекул и согласно молекулярно-кинетической теории идеального газа, давление p численно равно 2/3 кинетической энергии поступательного движения молекул, заключѐнных в единице объѐма:
p |
2 N m |
ср2 |
|
2 |
т |
m |
ср2 |
||||
|
|
|
|
|
|
|
|
|
|||
|
|
2 |
|
|
|
|
|||||
|
3 |
|
|
|
3 |
2 |
|
||||
Здесь N - полное число молекул в объѐме ; m и ср2 - масса молекулы и еѐ средняя
квадратичная скорость.
н
Давление измеряется в паскалях 1Па=1 м2 в СИ, хотя известно много различных
единиц.
Соотношения между единицами измерения давления:
Единиц |
|
|
кгс/с |
мм. рт. |
мм. вод. |
|
ы |
Па |
бар |
||||
м 2 |
ст. |
ст. |
||||
|
|
|
||||
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
1Па |
1 |
10 5 |
1,02 |
7,51 |
0,102 |
|
|
|
10 5 |
10 3 |
|
||
|
|
|
|
|||
1 бар |
|
1 |
1,02 |
7,51 |
1,02 |
|
10 5 |
102 |
104 |
||||
|
|
|
||||
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
||||
|
|
|
|
|
|
|
1 |
9,81 |
0,981 |
1 |
735 |
104 |
|
кгс/см 2 |
104 |
|||||
|
|
|
|
7
1 мм. рт. |
|
1,33 |
1,36 |
|
|
ст. |
133 |
10 3 |
10 3 |
1 |
13,6 |
|
|
|
|
|
|
1 мм. |
9,81 |
9,81 |
10 4 |
7.35 |
|
вод. ст. |
10 5 |
|
10 2 |
1 |
|
|
|
||||
|
|
|
|
|
|
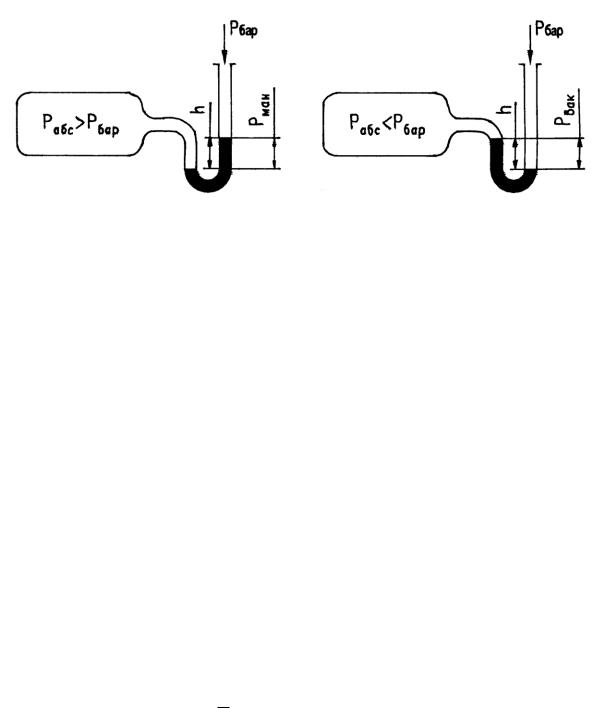
Для измерения давления в технике используются манометры и вакууметры.
PАБС PБАР |
PАБС PБАР PМАН |
PАБС PБАР |
PАБС PБАР PВАК |
Избыточное давление Pман или |
разрежение Pвак может быть измерено |
жидкостным прибором:
PМАН PАБС PБАР gh
PВАК PАБС PБАР gh
Где g , h и - соответственно ускорение свободного падения, разность уровней
жидкости в приборе и плотность жидкости, заполняющей жидкостный манометр. Удельный объѐм - есть объѐм единицы массы
|
V |
m3 |
|
|
см3 |
|
||
|
|
|
|
или |
|
|
||
m |
кг |
г |
||||||
|
|
|
|
|
||||
Обратная ему величина |
m |
- называется плотностью |
кг |
|
, она выражается в |
||
|
|
|
|
|
|||
|
|
3 |
|||||
|
V |
|
|
м |
|
|
|
единицах СИ. Иногда употребляется понятие удельного веса - это вес вещества в единице его объѐма
|
G |
|
кг |
|
||
|
|
|
|
- единицы технической системы |
||
м |
3 |
|||||
|
||||||
|
V |
|
|
|
||
Видно, что 1, а
g g , где g - ускорение свободного падения.
Температура характеризует интенсивность теплового движения частиц в системе. Количественное определение температуры связано с использованием любого зависящего от степени нагретости свойства тела. Используется тепловое расширение жидкостей (ртутные, спиртовые термометры) или газов (газовые термометры). Часто
8
применяются термометры сопротивления, в которых используется изменение при нагревании электрического сопротивления металлической нити, а также термопары, в которых измеряется напряжение термотока, развивающегося при нагревании спая двух металлов. Гениальная идея судить об изменениях температуры по другим измеряемым изменениям в телах принадлежит Галилею. По сути дела, измерение температуры термопарами основано на законе термического равновесия, из которого следует, что термометр показывает свою собственную температуру, которая равна температуре тела, с которым термометр находится в термическом равновесии (Дж. Блэк - вторая половина
XVIII в).
Каждый прибор, используемый для измерения температуры, должен быть отградуирован (оттарирован) в соответствии с твердо установленной температурной шкалой. История хранила имена многих учѐных, работавших в этом направлении. Во Флорентийской Академии экспериментальных исследований (1657-1667) открыли, что в смеси воды со льдом один и тот же термометр всегда показывает одно и то же. В 1694 г. Карло Ренальдини первый предложил принять в качестве фиксированных температур при градуировке термометра температуру таяния льда и температуру кипения воды. В 1724 г. это окончательно установил немецкий стеклодув Габриэль Даниэль Фаренгейт. Он предложил шкалу с тремя фиксированными точками: 0° соответствует температуре смеси воды, льда и нашатыря, 98° -температура тела здорового человека под мышкой или во рту;
вкачестве контрольной температуры для сверки различных термометров было принято значения 32° для точки таяния льда.
В1730 г. Рене Антуан Фермо де Реомюр предложил применять в термометрах спирт и ввѐл шкалу в соответствии с тепловым расширением спирта (у Фаренгейта произвольно). А т.к. он обнаружил, что спирт, смешанный в пропорции 5:1 с водой, расширяется в отношении 1000:1080 при изменении температуры от точки замерзания до точки кипения воды, то предложил шкалу от 0 до 80°. В 1742 г. астроном А. Цельсий предложил стоградусную шкалу с точкой "О", соответствующей кипению воды, и точкой "100", соответствующей еѐ замерзанию. Изменение направления было произведено в 1750 г. другим астрономом Мартином Штрѐмером. К концу века число различных шкал быстро возросло. В "Пирометрии" Ламберта приводится 19 шкал.
ВСИ температуру выражают в Кельвинах (К). Согласно молекулярно - кинетической теории материи абсолютная термодинамическая температура Т, измеряемая
вградусах Кельвина, равна
|
2 |
|
m ср2 |
|
|
||
T |
|
|
|
, где m- масса молекулы, k =1,3805 |
10 23 |
Дж/градконстанта |
|
3k |
2 |
||||||
|
|
|
|
||||
Больцмана.
Абсолютная или термодинамическая шкала установлена по температуре абсолютного нуля (состояние тела, при котором прекращается поступательное движение молекул идеального газа) и тройной точке воды, которая равна 273,16 К (состояние вещества, при котором совместно могут находится все три фазы). Известна ещѐ шкала Ренкина, которая представляет собой шкалу Фаренгейта, отсчитанную от абсолютного нуля.
Соотношение между различными температурными шкалами:
Наименование |
|
|
|
|
|
Шкала |
Шкала Реомюра |
||
Шкала Цельсия |
Шкала Ренкина |
Фаренгейта |
|||||||
шкал |
|
||||||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
Шкала |
- |
|
5 |
|
|
t 0Ф 32 |
|
1,25 t°R |
|
Цельсия,°С |
|
9 |
Т°Ra-273,15 |
1,8 |
|
||||
|
|
|
|
||||||
|
|
|
|
|
|
||||

9
Шкала |
1,8 |
|
|
|
|
|
|
1,8(1,25t°R+ |
|||
- |
t°Ф+459,67 |
+273,15) |
|||||||||
Ренкина,°Rа |
(t°С+273,15) |
||||||||||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
Шкала |
1,8 t°С+32 |
t° Rа-459,67 |
|
|
- |
|
9 |
t°R+32 |
|||
Фаренгейта,°Ф |
|
|
4 |
||||||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||||
Шкала |
|
0,8( |
5 |
Т°Ra- |
|
4 |
|
|
|
|
|
0,8 t°С |
9 |
(t°Ф-32) |
- |
||||||||
Реомюра,°R |
|
|
9 |
||||||||
|
273,15) |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
||||
Величина градуса по шкале Кельвина принимается равной градусу по стоградусной шкале и
Т(К)= t°С +273,15 0С
ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ
Термодинамическое рабочее тело (ТРТ) - непрерывное, однородное физическое тело, заполняющее всѐ пространство и не имеющее других поверхностей раздела, кроме границ данного объѐма.
Под термодинамической системой понимают любую совокупность материальных тел, находящихся в энергетическом взаимодействии. Она включает в себя следующие элементы:
1.Окружающую (внешнюю) среду.
2.ТРТ, которое обеспечивает энергетические превращения в системе.
3.Несколько источников энергии с различной температурой.
4.Аккумуляторы энергии (работы).
Термодинамическая система в общем случае взаимодействует с окружающей средой.
Изолированной системой называется такая материальная система, которая не имеет никакой энергетической связи с внешней средой.
Полный запас энергии изолированной системы не изменяется согласно закону сохранения и превращения энергии.
E из.сист. const
E из.сист. 0
Под адиабатической системой в термодинамике понимается система без внешнего теплообмена, т.е. такая система, которая никакого тепла не отдаѐт во внешнюю среду и никакого тепла из внешней среды не получает, хотя при этом механическое взаимодействие с внешней средой может быть.
dQ 0 Q 0
Всякое изменение, происходящее в термодинамической системе и связанное с изменением хотя бы одного из термодинамических параметров ТРТ, называется термодинамическим процессом.
По существу, это ряд плавно сменяющихся состояний ТРТ. При изображении проекции термодинамического процесса на плоскость в p -
координатах под процессом расширения понимается процесс, идущий с увеличением объѐма системы. Принято
