
Классические методы химического анализа (110
..pdfМИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «ВОРОНЕЖСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
КЛАССИЧЕСКИЕ МЕТОДЫ ХИМИЧЕСКОГО АНАЛИЗА
Учебно-методическое пособие для вузов
Составители: О.Ф. Стоянова, И.В. Шкутина, В.Ф. Селеменев
Издательско-полиграфический центр Воронежского государственного университета
2011
Утверждено научно-методическим советом химического факультета 17 мая 2011 г., протокол № 5
Рецензент д-р хим. наук, проф. Е.Г. Гончаров
Учебно-методическое пособие подготовлено на кафедре аналитической химии химического факультета Воронежского государственного университета.
Рекомендуется для студентов 3 курса высшего профессионального образования дневного отделения химического факультета.
Для специальности 020101 – Химия
2
СОДЕРЖАНИЕ |
|
Введение................................................................................................................ |
4 |
Аналитические характеристики и статические оценки ................................... |
5 |
Стехиометрические расчеты ............................................................................. |
12 |
Титриметрический анализ................................................................................. |
25 |
Гравиметрический анализ и равновесие осадок-раствор................................ |
43 |
Литература........................................................................................................... |
48 |
3
Введение
Основу аналитической химии составляют методы анализа, разнообразные по назначению, природе, метрологическим характеристикам. Целью преподавания дисциплины является обучение студентов теоретическим и практическим основам разных методов качественного и количественного анализа. Специалисты-химики, работающие в заводских или клинических лабораториях, используют химические знания для анализа реальных образцов и, как правило, несут ответственность за результат. От уровня химического анализа зависит развитие многих наук. Обработка и интерпретация данных являются жизненно необходимыми для всех видов аналитических методов.
Поэтому в данном методическом пособии детально описывается как выразить точность и правильность аналитических результатов, как оценить погрешности в измерениях с приложением строгих математических и статистических концепций (раздел «Аналитические характеристики и статистические оценки»).
Для выполнения вычислений при проведении химического анализа необходимо знание стехиометрии, т.е. количественных соотношений, в которых взаимодействуют химические вещества. В методическом пособии приведены такие фундаментальные понятия, как масса, количество вещества, моль, эквивалент. Рассмотрены различные формы представления результатов анализа применительно к твердым веществам и растворам (раздел «Стехиометрические расчеты»).
В учебно-методическом пособии также уделено внимание теоретическим основам классических методов количественного анализа – титриметрии и гравиметрии (разделы «Титриметрический анализ», «Гравиметрический анализ и равновесие осадок – раствор»), отличающихся простотой аппаратурного оформления, малой трудоемкостью и высокой точностью. Студентам предлагаются задачи для расчета концентрации и массы аналита в титриметрии и гравиметрии.
Учебно-методическое пособие дает возможность студентам химического и фармацевтических факультетов углубить профессиональную подготовку и грамотно представлять результаты практического химического анализа.
4
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ И СТАТИСТИЧЕСКИЕ ОЦЕНКИ
При обсуждении качества анализа (особенно количественного) аналитик оперирует целым рядом величин и понятий. К ним относятся те, которые можно оценить в результате градуировки и статистической обработки данных: чувствительность, точность, воспроизводимость, правильность, а также предел обнаружения и граница определяемых содержаний. Характеристикой, способной определять компоненты в присутствии посторонних веществ, служит селективность (избирательность), а экономическими показателями – затраты ресурсов, стоимость и время анализа.
Градуировка и ее роль в процессе анализа
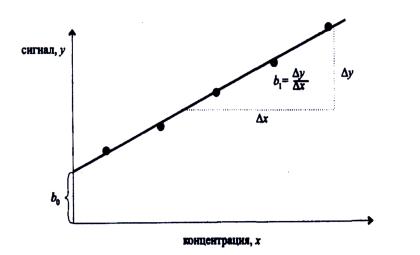
Для определения содержания компонента на основе результатов измерений необходимо в процессе анализа хотя бы один раз выполнить градуировку. Цель градуировки – описание связи между величиной (интенсивностью) аналитического сигнала и массой, относительным содержанием либо концентрацией определяемого компонента с помощью градуировочной функции – как правило, прямолинейной (рис. 1).
Рис. 1. Линейная градуировочная функция, построенная по пяти значениям концентраций х и соответствующим величинам сигнала у
Выразим градуировочную функцию в виде следующего уравнения:
y = b0 + b1x.
Свободный член b0 (отрезок, отсекаемый градуировочной прямой на оси ординат), представляет собой сигнал фона. Сигнал фона – это величина аналитического сигнала, соответствующая нулевой концентрации определяемого компонента. Следует иметь в виду, что при обработке градуировочных данных численными методами сигнал фона, вообще говоря, всегда
5
отличен от нуля. Если сигнал фона можно экспериментально измерить, то его можно вычитать из всех сигналов и представить уравнение градуировки в виде y = b1x. Для оценки значимости сигнала фона, рассчитанного математическими методами, следует применить соответствующие статистические тесты.
Тангенс угла наклона градуировочной прямой, b1, называют коэффициентом чувствительности. В случае искривленной градуировочной функции значения коэффициента чувствительности в разных ее точках различны. При этом обычно используют значение, соответствующее середине диапазона определяемых концентраций.
Среди методов анализа различают абсолютные и относительные. К абсолютным методам относят те, в которых концентрацию определяют при помощи фундаментальных физических постоянных, таких, как молярные массы и соотношения стехиометрии в гравиметрии и титриметрии, постоянная Фарадея и законы электролиза в кулонометрии. Абсолютные методы не нуждаются в градуировке (в самом крайнем случае градуировку можно выполнить один раз). В относительных методах параметры градуировочной функции (коэффициент чувствительности и сигнал фона) следует каждый раз заново определять экспериментально. Методы, основанные на физических явлениях, как правило, являются относительными и требуют градуировки.
Для нахождения неизвестной концентрации по измеренному значению аналитического сигнала уА необходимо решить уравнение (1) относительно концентрации хА. В результате получим аналитическую функцию:
хА = |
уА −bо |
. |
(1) |
|
|||
|
b1 |
|
|
Применение метода добавок для учета матричных эффектов
Особым способом градуировки является метод добавок. Применение этого метода призвано исключить влияние матрицы на результаты анализа, например, при анализе плазмы крови. В этом случае градуировочную функцию строят не отдельно от образца, используя серию специально приготовленных растворов различной концентрации, а непосредственно добавляют известные количества определяемого компонента к отдельным порциям раствора образца. Из результатов измерения растворов образца без добавок и с различными добавками находят неизвестную концентрацию компонента в образце, как показано на рис. 2.
6
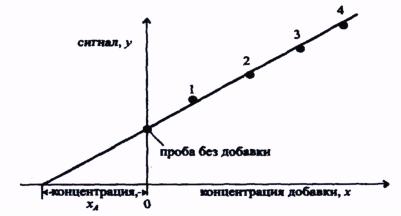
Рис. 2. Градуировка по методу добавок: к пробе добавлены четыре раствора определяемого компонента известной концентрации
Из рис. 2 можно убедиться, что метод позволяет проводить определение и в случае изменения коэффициента чувствительности, обусловленного влиянием матрицы. Однако величина сигнала фона с помощью метода добавок не может быть найдена. При использовании метода добавок она должна быть точно известна.
Внутренний и внешний стандарт
Для учета влияния различных внешних условий на результаты анализа следует измерять аналитический сигнал по отношению к сигналу некоторого стандарта. Если сигнал компонента, служащего стандартом, измерен отдельно от образца, такой стандарт называют внешним. Если же он вносится непосредственно в пробу либо в качестве стандарта используют один из компонентов самой пробы, он называется внутренним стандартом.
Метод внутреннего стандарта можно использовать и для проверки методик, если необходимо проконтролировать весь ход анализа от пробоподготовки до обработки результатов. В этом случае внутренний стандарт вносится в исходную пробу до начала выполнения анализа.
Точность результатов анализа: воспроизводимость и правильность
При выполнении любого аналитического измерения могут возникнуть погрешности двух видов. В одном случае результаты измерений при их повторении случайным образом разбросаны друг относительно друга. Такая погрешность называется случайной. Величину случайной погрешности результатов анализа характеризует понятие воспроизводимость. В другом случае результаты анализа отклоняются от истинного значения на постоянную величину. Такая погрешность называется систематической, ее характеризует понятие правильность.
7

Воспроизводимость результатов анализа можно оценить, выполнив независимую серию повторных измерений (параллельных определений) одной и той же пробы и рассчитав величину стандартного отклонения результатов относительно среднего.
Среднее значение обобщенно характеризует результат измерения, т.е. положение точки на некоторой числовой оси (применительно к измерению сигнала это будет ось ординат, у). Среднее из n параллельных определений равно
− |
1 |
n |
|
у = |
∑ yi . |
(2) |
|
|
n |
i=1 |
|
Стандартное отклонение s есть мера разброса значений измеряемой величины относительно среднего:
|
n |
− |
|
|
s = |
∑( yi − y)2 |
. |
(3) |
|
i=1 |
|
|||
|
n −1 |
|||
|
|
|
|
|
Стандартное отклонение можно выразить и в относительной форме,
разделив его на среднее значение. Относительное стандартное отклоне-
ние sr вычисляется как
sr |
= |
sy |
|
. |
(4) |
|
|
|
|
||||
|
|
|||||
|
|
|
y |
|
||
Его можно выразить и в процентах: sr(%) = sr · 100.
Все величины (среднее, стандартные отклонения), рассчитанные по формулам (2)–(4), относятся к величине сигнала у. Для точности в уравнении (3) следовало бы написать sy.
Чтобы охарактеризовать воспроизводимость применительно к концентрации х, надо использовать соответствующую величину sх. Ее можно рассчитать, используя градуировочную зависимость:
sX = sby . (5)
1
Величину sx называют стандартным отклонением методики.
Общая погрешность процесса анализа определяется не только погрешностью измерения соответствующим образом подготовленной пробы, но и погрешностями пробоотбора, пробоподготовки и обработки данных. Некоторую погрешность может внести даже процесс считывания результатов со шкалы измерительного прибора или оцифровка измеряемой величины. Для оценки общей погрешности служит закон распространения погрешностей. При наличии несколько суммирующихся независимых друг от друга источников погрешностей следует сложить квадраты стандартных отклонений – дисперсии – отдельных составляющих. Для оценки погрешности произведе-
8

ния или частного следует сложить квадраты относительных случайных погрешностей.
Пусть общая погрешность результатов анализа s2 состоит из погрешности пробоотбора s2р и погрешности измерения s2м. При этом было отобрано m проб, и каждая была проанализирована n раз. В этом случае
s |
2 |
= |
s2p |
+ |
s2 |
|
|
|
|
м |
. |
(6) |
|||
|
m |
|
|||||
|
|
|
|
n m |
|
||
Множество отдельных источников погрешностей надо особенно тщательно учитывать для многостадийных методик анализа, т.е. таких, где проба от отбора до измерения сигнала проходит через множество операций: разложение, концентрирование, разделение компонентов.
Под истинным значением следует понимать значение, известное с высокой точностью и потому принимаемое в качестве истинного.
Воспроизводимость – это лишь одна из составляющих точности результатов анализа. Может так случиться, что достаточно хорошо воспроизводящиеся результаты тем не менее не соответствуют действительности: найденная концентрация компонента значительно отличается от его истинного содержания в образце. Подобное систематическое отличие измеренной величины от истинной характеризуется понятием правильность. Общая погрешность одного единичного результата анализа, еi, складывается из случайной и систематической составляющей:
еi = (хi – х) + ( х – хист). (7)
Для характеристики правильности используют процентную меру правильности (англ. recovery). Она представляет собой выраженное в процентах отношение найденной концентрации (среднего значения) к истинному значению концентрации компонента в пробе и для одного анализа рассчитывается как
recovery (%) = |
|
х |
|
100. |
(8) |
|
х |
||||||
|
|
|
||||
|
ист |
|
|
|||
Истинное значение можно получить путем анализа образца множеством различных, независимых друг от друга, методов либо при помощи стандартных образцов, для которых значение содержания официально удостоверено. Анализ образца независимыми методами обычно проводят в форме межлабораторного эксперимента. Для этого образец рассылают в разные лаборатории и там анализируют. Истинное значение находят в результате анализа и оценки массива полученных данных. Содержание компонентов в стандартном образце находят подобным же образом; кроме того, состав стандартных образцов тщательно контролируют уже на стадии их приготовления.
9
Доверительный интервал результата анализа
При представлении результатов анализа требуется указать и оценку их неопределенности. Неопределенность результатов выражают в форме доверительного интервала. Для абсолютных методов – таких, как титриметрия, – доверительный интервал рассчитывают из стандартного отклонения s и числа параллельных определений n при помощи специального статистического коэффициента – коэффициента Стъюдента t для выбранной доверительной вероятности Р и числа степеней свободы f:
∆х = t(P, f )s . |
(9) |
n |
|
Для результатов анализа одной пробы f = n – 1. Оценку величины стандартного отклонения s, как правило, находят из той же самой серии параллельных результатов либо определяют отдельно.
Для относительных методов при расчете доверительного интервала необходимо учитывать и погрешность, вносимую градуировочной функцией:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
х = s t(P, f ) |
1 |
+ |
1 ( |
y |
− |
y |
)2 |
|
. |
(10) |
||
|
|
|
|
|
|
|
m |
|
|||||||||
|
|
|
|
|
|
m |
|
n b12 ∑(xi − |
|
)2 |
|
|
|||||
|
|
|
|
|
|
|
x |
|
|||||||||
|
|
|
|
|
|
|
|
|
i=1 |
|
|
|
|||||
Здесь |
|
|
– среднее значение сигнала для n параллельных анализов про- |
||||||||||||||
|
y |
||||||||||||||||
|
|
|
среднее значение сигналов для всех |
m точек градуировочного |
|||||||||||||
|
|
|
|||||||||||||||
бы, а у– |
|||||||||||||||||
графика.
Результат анализа представляют в форме среднего значения из серии параллельных определений с рассчитанным доверительным интервалом:
х |
±Δx. |
(11) |
Предел обнаружения – минимальная концентрация, которая может быть обнаружена
Значение величины предела обнаружения особенно важно при анализе следовых количеств.
Аналитический сигнал ymin, соответствующий пределу обнаружения, особенно важен при анализе следовых количеств.
Аналитический сигнал ymin, соответствующий пределу обнаружения, складывается из величины сигнала фона yB и стандартного отклонения сигнала фона sB как
ymin = yB + 3sB. |
(12) |
C помощью градуировочной функции можно выразить предел обнаружения непосредственно в единицах концентрации:
10
