
Шейко Політравма
.pdf
Глава4 Шокипротивошоковаятерапия |
|
121 |
|
|
|
избежать ееосложнений.Повышенноепосле инфузииЦВД наблюдается у пациентов с хроническими обструктивными заболеваниями легких и при развитии респи- раторногодистресс-синдромалегких.
Постоянная переоценка данных мониторинга позволит своевременно выявить угрожающие осложнения как в динамике заболевания так и ятрогенных осложненийвходеинтенсивнойтерапии.
Другим немаловажным побочным эффектом инфузионной терапии при шоке являетсяреперфузия,когдавсистемныйкровотокпослепериодаишемиипоступаетвесьмассивпогибшихвследствиегипоксииклеточныхструктур,продуктованаэробного метаболизма, кишечные и раневые бактериальные токсины, каскады медиаторов аутоагрессии. Синдром реперфузии наиболее выражен у пациентов при краш-синдроме,длительноналоженныхжгутахнаконечности,привозобновлении микроциркуляторной перфузии в ранее ишемизированных тканях после длительнойгипотензииможетсопровождатьсяразвитиемклиникиэндотоксическогошока с устойчивой депрессией гемодинамики, респираторного дистресс-синдрома легких,остройпочечнойнедостаточности.
Гипотермия и шок. У пациентов с тяжелыми расстройствами гемодинамики имеется неизбежная гипотермия, сама являющаяся дополнительным повреждающим фактором, усугубляющим метаболические расстройства и системную воспалительную реакцию. Гипотермия у пациента наиболее выражена при алкогольной интоксикации, вследствие расширения периферических сосудов. Доказано, что у пациентовстяжелымшокомгипотермияспособствуетразвитиюкоагулопатии.Для устранениянеблагоприятныхпоследствийгипотермиипришокепострадавшихнеобходимообеспечитьсогреваниемодеялами,грелкамиинагретымиинфузионными средами. Нагревание растворов у пациентов с шоком должно осуществляться минимумдо37°С,аупациентовсвыраженнойгипотермиейдо39°С.
РЕЗЮМЕ
1.Шок при политравме развивается вследствие комбинации трех ведущих этиологических компонентов: кровопотери, расстройства сократительной функции сердца и сосудистого тонуса, определяющих нарушение микроциркуляторной перфузии с ишемическим поражением органов и тканей; декомпенсированный шокдополнительноусугубляетсявазодилятациейиповышеннойпроницаемостю сосудистойстенкивследствиегиперэергическойсистемнойвоспалительнойреакции,прогрессирующейпропорциональномасштабутравматическойигипоксическойдеструкциитканей.
2.Характер шока при политравме зависит от доминирующего патогенетического компонента, определяющего три вида травматического шока: геморрагический (встречается у 86,9% пострадавших), кардиогенный (при тяжелом ушибе

122 В.Д.ШЕЙКО  Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени
сердца – у 0,4% и/или компрессии сердца из-вне – у 10,3%) и нейрогенный (при позвоночно-спиномозговойтравме–у2,4%).
3.Диагностический поиск при политравме не должен задерживать начало интенсивной инфузионной терапии для восполнения ОЦК, что является приоритетной задачейприлюбомвидетравматическогошока.
4.Диагноз шока основан исключительно на клинической оценке гемодинамическихрасстройствидисфункцийсистемжизнеобеспечениявследствиенарушения перфузии тканей; компенсированные гемодинамические расстройства (шок без гипотензии) позволяет выявить функциональная ортостатическая проба по факту ортостатическойтахикардиииортостатическойгипотензии.
5.Шок – это не артериальная гипотензия, это неадекватная оксигенация периферических тканей и развивается при их продолжительной ишемии; поэтому норма- лизацияартериальногодавленияупострадавшегосполитравмой–лишьэтапная задача, основной целью противошоковых мероприятий является достижение адекватнойоксигенациивсехишемизированныхтканей.
6.Объем и структура интенсивной противошоковой терапии определяется первичной клинической оценкой дефицита ОЦК на основании гемодинамических расстройств, с последующей переоценкой ее эффективности и коррекцией в двух ключевых точках: (1) после вливания 2 литров инфузионных сред и (2) при получении положительной гемодинамической реакции на инфузию с достижением уровнясистолическогоАДболее80ммрт.ст.
7.УровеньсистолическогоАД=80ммрт.ст.отражаетналичиеминимальногоорганного кровотока и позволяет медикаментозно пролонгировать такую гипотензию (гипотензивная ресусцитация без достижения нормотензии) при наличии неконтролируемого внутреннего кровотечения с целью уменьшения темпа кровопотеридоосуществленияадекватногохирургическогогемостаза.
8.Особенностью шока при политравме является наличие двух клинических феноменов: (1) несоответствие тяжести шока и его устойчивость к адекватной интенсивной противошоковой терапии; (2) несоответствие тяжести шока и характера имеющихся анатомических повреждений, что обусловлено синдромом взаимногоотягощенияповреждений.
9.Пациенты с выраженным физическим развитием (атлеты) и возбужденные пациентысдисфорическойформойалкогольногоопьяненияспособныпродолжительное время компенсировать массивную кровопотерю и шок, угрожая внезапной смертьюпотипуостройнадпочечниковойнедостаточности.
10.Шок у пожилых пациентов угрожает значимыми ишемическими поражениями органов и систем даже при невыраженном дефиците ОЦК ввиду слабой гемодинамическойреакциинамощнуюадренергическуюстимуляцию.
11.У женщин во второй половине беременности шок на ранних стадиях легко компенсируются физиологической гиперволемией, но сопровождается снижением маточно-плацентарногокровотокаиугрожаетантенатальнойгибельюплода.

Глава |
Полиорганная недостаточность |
5 |
при политравме |
|
|
На протяжении ХХ века изучение госпитальной летальности у пострадавших с травмамиопределилоосновнойпричинойсмертикритическиерасстройствафункцийосновныхсистемжизнеобеспечениятравмированногоорганизма.Какнозологическаякатегорияполиорганнаянедостаточность(ПОН)инициированнаятяжелой травмой и шоком изучается на протяжении 40 лет. В середине 70-x годов ХХ века описание последовательной множественной системной дисфункции и недостаточности, как синдрома у критических пациентов, было представлено N.Тylney (1973) иA.Baue(1975),атермин«полиорганнаянедостаточность»–предложилB.Eiseman (1977).В1980г.D.Fryпредставилпервуюкритериальнуюоценочнуюшкалудлядиагностики ПОН. За этот временной промежуток значительной трансформации подверглись взгляды на терминологию, патофизиологию и подходы к лечению этого патологического состояния, развивающегося у крайне тяжелой категории пострадавших. Эпидемиология ПОН неразрывно связана с тяжелой травмой и, несмотря на значительные успехи в ее лечении, остается основной причиной смерти после тяжелыхтравмвотделенияхреанимациииинтенсивнойтерапии.
Большинствоорганныхрасстройств,составляющихполиорганнуюнедостаточность, известны давно. В первой четверти прошлого века ведущей причиной неблагоприятных исходов при травмах и ранениях была определена кровопотеря. Это определило ведущее направление поиска оптимальных методов лечения. Уже
впериодВтороймировойвойны(1939-1945гг.)ведущейпричинойсмертираненых была признана острая сердечно-сосудистая недостаточность, которая развивалась вследствие острой кровопотери (шок). Утверждаются основополагающие критерии оказания экстренной помощи – экстренная эвакуация в полевые госпиталя и восполнение кровопотери трупной и донорской кровью. В период Корейской войны стандартная трансфузионная терапия дополняется вливанием плазмы крови. Предложеннаялечебнаятактика привела к значительному улучшению результатов лечения–выживаемостьвполевыхгоспиталяхвэтотпериод возросла. Однако побочным эффектом расширяющейся трансфузионной терапии явилось резкое возрастание частоты почечной недостаточности. Разработка этой проблемы обоснованно связала недостаточную эффективность лечебной тактики с обезвоживанием интерстициального сектора при шоке, что определило решение использовать изотонические солевые растворы при лечении шокогенной травмы. В период войны
вИндокитае (1960-1970 гг) в структуре инфузионной терапии начинается широкое использование кристаллоидов, а в мониторинг включается почасовая оценка диуреза.Подобнаякоррекцияинтенсивнойтерапииоказаласьэффективнойипривела к снижению отсроченной летальности и значительному снижению частоты почеч-

124 В.Д.ШЕЙКО  Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени
нойнедостаточности.Однакодостигнутыеуспехивинтенсивнойтерапиираненных ознаменовалисьростомудельноговесалегочнойнедостаточности–констатирова- но появление синдрома «шокового легкого». Новый виток в понимании посттравматических функциональных расстройств был связан с развитием и внедрением в 1970-хгодахпрошлоговекаметодоваппаратнойорганопротекции–аппаратыИВЛ и гемодиализа, вазопрессорных и инотропных препаратов в реанимации пострадавших. В результате достижения в лечении критических пациентов стали еще более значимы, улучшились результаты лечения изолированных посттравматических функциональныхрасстройствдыхания,сердечнойдеятельностиипочек. Нопараллельносдостижениямивклиническойпрактикеначалпроявлятьсяновыйсиндром
– прогрессирующей полиорганной недостаточности, который до сих пор остается основной причиной смерти пострадавших после выведения их из шока. В ходе исследования проблемы полиорганной недостаточности нередко оказывалось, что орган, наиболее пострадавший при критическом состоянии, не был поврежден изначально,авовлекалсявпроцессвторично.
В1980-90-хгодахведущуюрольвразвитииПОНотдавалиинфекционномуна- чалу. С сепсисом связывали доктрину «вторичной волны», когда первичное травматическоеповреждениеишокистощаюткомпенсаторныереакциииугнетаютреактивность, чем определяется неспособность организма отвечать на реанимацию
спрогрессированием первичной ПОН, либо если первичная ПОН не развивается, организм становится чрезвычайно восприимчив к любой дополнительной агрессии, наиболее часто – системной воспалительной реакции (ССВР) инфекционного генеза. При этом между ССВР и ПОН выявляется четкая взаимосвязь. Установлено, чточемболеевыраженпервичныйССВР,темболеевысокрискразвитияфатальной ПОН и, наоборот, незначительный или умеренно выраженный первичный посттравматический ССВР сопровождается благоприятным течением травматической болезни.
Терминология ПОН. Сегодня ПОН определяют как синдром, развивающийся
унаиболее тяжелой категории пациентов, находящихся в критическом состоянии. Терминология синдрома ПОН за весь период изучения проблемы также подвергалась неоднократному переосмыслению. Большинством автором при определении описывается типичная клиническая картина прогрессирующих дисфункций восьми систем и органов – кровообращение, дыхание, почки, печень, ЖКТ, ЦНС, кровь и метаболизм. Для каждой из систем определяются критерии манифестации и степени выраженности функциональной недостаточности. Появляются динамические термины нарастающих расстройств – дисфункция, недостаточность и несостоятельность.
Воснове понятия синдрома полиорганной недостаточности лежит описа-
ниеполиэтиологическогокритическогосостояния,характеризующегосяустойчивой функциональнойнедостаточностьюдвухиболеепервичнонесвязанныхмеждусобойорганов,сопровождающегосявысокимрискомнеблагоприятногоисхода.
Последниегоды,нарядустерминомПОН,чащеиспользуюттермин«синдром полиорганной дисфункции» (СПОД). Понятие «синдром полиорганной дисфунк-

Глава5 Полиорганнаянедостаточностьприполитравме |
|
125 |
|
|
|
ции» отражает динамику прогрессирующей органной дисфункции, включая ее инициацию, в то время как «полиорганная недостаточность» констатирует развитиефинального,клиническиопределенногоэтапаэтойдисфункции.
Анализ течения травматической болезни, функционального и лабораторного мониторингаприполитравмепозволяетвыделитьнесколькофазразвитиясиндромаприинициацииипрогрессированииорганныхдисфункций.
I.СПОД в фазе манифестированной дисфункции. Общее состояние потер-
певшихкрайнетяжелоеиликритическое.Выявляютсяединичныеклиническиеилифункциональные,илилабораторныепроявлениядисфункции двух систем жизнеобеспечения.Приэтомвозникающиерасстройствахорошореагируютналечение.
II.СПОД в фазе функциональной недостаточности. Общее состояние по-
страдавшихкритическое.Выявляютсявыраженныеклинические,функциональные и лабораторные проявления дисфункции двух и более систем. Приэтомреакцияналечениенеустойчива,носохранена.
III.СПОД в фазе функциональной несостоятельности. Общее состоя-
ние потерпевших критическое. В структуре синдрома в большей мере проявляются признаки полной утраты функций центральной нервной, сердечно-сосудистой систем и дыхания. Отмечается резистентность расстройствклюбымлечебныммероприятиям,процесс,какправило,необратим.
При этом первые две фазы являются потенциально обратимым состоянием, последняя – необратимым и терминальным, предшествующим неблагоприятному исходу.
Дисфункция систем жизнеобеспечения в первые 48 часов после травмы неможетбытьопределенакаксиндромПОНилиСПОД,посколькутакая дисфункция в большинстве клинических ситуаций является типичной реакцией на травму и шок, оказывается транзиторной и обратимой, легкокорригируетсяинтенсивнойтерапией.
ПриопределенииПОНилиСПОДтрадиционновыделяютпервичнуюилираннюю и вторичную или позднюю ПОН. Несмотря на типичные посттравматические патофизиологические процессы, инициирующие как первичную, так и вторичную ПОН, рассматриваются они как отдельные синдромы с различными провоцирующимифакторами,критериямиоценкииисходами.
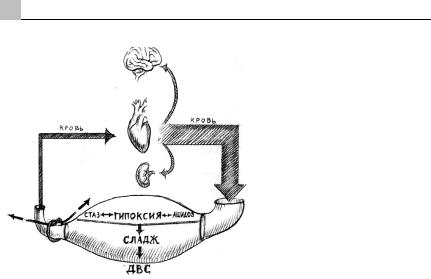
Посттравматическая органная дисфункция – типичная реакция организма на тяжелую травму и шок (Рис. 5.1). В большинстве клинических ситуаций первичная, инициированная политравмой дисфункция является транзиторной и коррегируется своевременной интенсивной терапией. Использование методов «протезирования» функциональных расстройств аппаратами ИВЛ, вазопрессоров и инотропов приводит к восстановлению и стабилизации функций систем жизнеобеспечения в первые 24-48 часов после травмы. Однако у 10-40% пострадавших инициирован-
126 В.Д.ШЕЙКО  Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени
|
ная |
политравмой органная |
||||
|
дисфункция, |
несмотря |
на |
|||
|
адекватную |
реанимацию |
||||
|
и интенсивную |
терапию |
не |
|||
|
регрессирует, |
а оказывается |
||||
|
резистентной |
к |
лечению |
с |
||
|
формированием |
устойчивой |
||||
|
или прогрессирующей поли- |
|||||
|
органной дисфункции. Имен- |
|||||
|
но такой вариант именуют |
|||||
|
первичной или ранней ПОН |
|||||
|
и констатируют ее исключи- |
|||||
|
тельно позднее 48 часов по- |
|||||
|
слетравмы |
|
|
|
|
|
|
|
Вторичная или поздняя |
||||
|
ПОН |
констатируется |
после |
|||
|
более или менее продолжи- |
|||||
Рис.5.1.Шокиполиорганнаянедостаточность. |
тельной стабилизации |
пер- |
||||
|
вично нарушенных функций |
|||||
системжизнеобеспечения,как«втораяволна»органныхдисфункцияиликаквпервые возникшая ПОН позднее 72 часов после травмы. Принято считать, что этот вариант ПОН развивается вследствие воздействия вторичного, даже умеренного по выраженности ССВР, на организм в состоянии стимулированного системного воспалительного ответа и посттравматического иммунодефицита. Поэтому ведущими триггерами вторичной ПОН являются метаболические расстройства и инфекция, преимущественно–пневмония,раневаяиинтраабдоминальнаяинфекция.
ПОНилиСПОД,какправило,развиваетсявопределеннойпоследовательности в зависимости от эффективности адаптацианно-компенсаторных реакций и глубины расстройств микроциркуляторной перфузии, является универсальной клиникофизиологической основой любого критического состояния вне зависимости от его этиологии, трудно поддается лечению и сопровождается высокой летальностью. Так, при поражении одной функциональной системы летальность составляет 13%, двух–34%,трех–80%,четырехиболее–95-100%.
Патогенез посттравматической полиорганной недостаточности. В основе развития ПОН или СПОД лежит ССВР, который инициирует системные функциональные расстройства при первично гипердинамическом развитии, либо повторных«атаках»наослабленныеборьбойзасуществованиерегуляторныесистемы.
Синдромсистемнойвоспалительнойреакции(ССВР)илиSystemInflammatory Response Syndrome (SIRS) – характеризуется инициацией системной воспалительной реакции организма на экстремальную экзо-, реже эндогенную агрессию, сопровождающуюся каскадным высвобождением в системный кровоток провоспалительных медиаторов. ССВР как правило возникает вследствие масштабного поражающего воздействия на ткани патологического фактора, определяющего не-

Глава5 Полиорганнаянедостаточностьприполитравме |
|
127 |
|
|
|
способность организма к его локализации. Традиционно инициаторами ССВР при политравме считают тяжелое травматическое, термическое или ишемическое повреждениетканейиинфекцию.
При политравме полифокальные очаги травматической деструкции являются поставщиками факторов с провоспалительной цитокин-индуцирующей активностью – фаза разгара SIRS. Выработка реактивными клетками – нейтрофилы, макро- фагиисосудистыйэндотелийпровоспалительныхмедиаторов(TNFa,IL-1,-6,-8,-12, -15, IFNγ, ГМ-КСФ) превышает нормальные величины в десятки раз. Масштабная травматическая и ишемическая деструкция тканей может приводить к избыточной стимуляции реактивных клеток, что обусловливает их гиперактивацию с резко возрастающей продукцией медиаторов воспаления – фаза иммунотоксикоза SIRS (R.Bone, 1996). Нейтрофилы являются именно теми клетками, которые способствуют как генерализации местной воспалительной реакции из очага повреждения (в комплексе с эндотелием капилляров), так и непосредственно разрушающих функцио- нальноактивныеструктурыжизненноважныхорганов–впервуюочередьлегких.
Установлено, что первично стимулированный в очаге воспаления эндотелий капилляров активирует циркулирующие нейтрофилы, которые, во-первых, направляются и фиксируются к стенке капилляра для миграции в очаг поражения, и, во-вторых, продуцируют провоспалительные медиаторы, способные при полифокальной активации, «приобретать эндокринные свойства» трансформируя микроциркуляцию, сосудистую проницаемость, внутриклеточный метаболизм. Однократно активированные при прохождении через очаг воспаления циркулирующие нейтрофилы сохраняют повышенную цитотоксическую активность на протяжении 48-72 часов, что делает их избыточно агрессивными и готовыми к генерализованной «атаке» в ответ даже на незначительный дополнительный внешний или внутреннийимпульс.
Полифокальная местная воспалительная реакция способствует избыточной активациициркулирующихнейтрофилов,которыемогутдегранулироватьвсосудистом русле, вызывая при этом повреждение эндотелия капилляров жизненноважныхоргановиструктур,кудавторичноустремляютсянейтрофилы,реализуякаскад гиперактивногоССВР.Приэтомвозникновениемасштабныхочаговтравматической и ишемической деструкции определяет не селективное воздействие на локальный клеточный субстрат, но дегрануляцию нейтрофилов с одномоментным выбросом как протеолитических ферментов, коллагеназы и эластазы, так и активных форм кислородаигипохлорида.
В основе локальных эффектов нейтрофилов лежит их способность фиксироваться к эндотелию капилляров в зоне повреждения и осуществлять миграцию в интерстицийнепосредственнокзонеместноговоспаленияилитравматическойдеструкции.Генерализованнаясистемнаяактивациякомплемента,преимущественно компонентов СЗа и С5а, приводит к их фиксации на эндотелии капилляров интенсивно функционирующих органов и структур. Возникают вазодилятация и нарастающая сосудистая проницаемость, адгезия и дегрануляция нейтрофилов на эндотелии с повреждением сосудистой стенки. Избыточная стимуляция способствует

128 В.Д.ШЕЙКО  Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени
дегрануляции нейтрофилов, которая моментально приобретает цепную реакцию, что определяет локальное повреждение и разрушение как поврежденных, так и жизнеспособныхклеток,имежклеточногоматрикса.Врезультатезащитнаяпосути воспалительная реакция при избыточной стимуляции становится аутодеструктивной и определяет неизбежность функциональной несостоятельности в очаге повреждения(Рис.5.2).
Вазодилятация, повышенная проницаемость сосудистой стенки, снижение интенсивности периферического кровообращения, микротромбообразование развиваются не только в очагах тканевой деструкции, но в микроциркуляторном русле всех тканей и органов. Особенно подвержены такому повреждающему эффектукапиллярылегких,через которые неизбежно проходит вся кровь для оксигенации. Развитие интерстициального отека легких – ОРДС, неизбежно дополняет патологический процесс гипоксией. При таком развитии событий инициируется полифокальная
и полиситемная функциональная недостаточность и несостоятельность. Таким образом,эндотелиальнаядисфункциястановитсяосновойфункциональнойнесостоятельностиоргановисистеморганизма.
Диагностические критерии ССВР. Стандартными критериями констатации ССВР, в соответствии с рекомендациями Согласительной Конференции (Чикаго, 1991г),являетсяналичиедвухиболееизчетырехклиническихпризнаков:
•температурателавыше38оСилиниже36°С;
•частотасердечныхсокращенийсвыше90вминуту;
•частотадыханийсвыше20в1минилиPaco2<32mmHg;
•количестволейкоцитовпериферическойкровисвыше12*109/лилиниже 4*109/лиликоличествонезрелыхформпревышает10%.
К основным четырем клиническим признакам ССВР в международных рекомендациях Surviving Sepsis Campaing (2008 г) добавлено еще три, но констатирующая схема осталась без изменений – ССВР определяется наличием двух и более признаковиз4основныхи3дополнительных:
•нарушениесознания;

Глава5 Полиорганнаянедостаточностьприполитравме |
|
129 |
|
|
|
•отекиилиположительныйводныйбаланс(>20мл/кг/сут);
•гипергликемия(>7,7ммоль/л)приотсутствиидиабета.
Травма, реанимация и неотложная хирургия являются типовыми триггерами ССВР. Физиологически ССВР является адаптационным защитным механизмом в борьбе организма за существование, развивается в течение трех часов после травмыисдостижениемфункциональнойстабилизациирегрессируетсамостоятельно. Однако ответная реакция организма на травму и первичную реанимацию индивидуальна и при избыточной стимуляции вследствие политравмы или вынужденно агрессивной неотложной помощи определяет возникновение гипердинамического ССВР.ИзбыточнопервичностимулированнаяипролонгированнаялибоповторноиндуцированнаясистемнаявоспалительнаяреакцияявляютсяосновойразвитияПОН.
Непосредственнымиусловиями,определяющимиразвитиетранзиторнойили устойчивой полиорганной дисфункции или недостаточности в остром посттравматическом периоде, являются: характер и масштаб повреждения тканей и конкретных органов, различная способность тканей противостоять гипоксии, исходное функциональное состояние самого органа. Таким образом, дисфункция органа первично определяется его физиологическим резервом и исходной способностью противостоять метаболическим постагрессивным расстройствам. Если пациент страдал каким-либо заболеванием до травмы, то способность его противостоять разрушающим эффектам дефицита микроциркуляции, развивающейся гипоксии и постагрессивногоССВРчрезвычайномала.
Патофизиология полиорганной недостаточности. Центральное место в об-
щей патофизиологической схеме развития ПОН принадлежит так называемому феномену «двойного удара», в основе которого лежит факт усиленного, гиперреактивного ответа травмированного организма на дополнительную, даже незначительную,агрессию.
Первоначальные травматическое повреждение и шок при политравме являются«первымударом»,которыйменяетметаболизмфункциональноактивныхклеток, эндотелия, нейтрофилов и т.д., и вызывает расстройства основных витальных функций.«Вторымударом»могутбытьреперфузия,агрессивнаяинтенсивнаятерапия или хирургическое вмешательство, а также любой фактор, усиливающий воспалительную реакцию, например, посттравматический панкреатит, поступление в кровоток токсинов из инфицированной раны или кишечника. В ответ на дополнительное повреждение, или «второй удар», подготовленные, активированные клетки воспаления, эти своеобразные «фабрики медиаторов» синтезируют и выбрасывают в циркуляторное русло значительно большее количество воспалительных каскадов,чемтоготребуетинтенсивностьэтойдополнительнойагрессии.Иужесама ответнаягиперэргическаявоспалительнаяреакциястановитсяаутодеструктивнойи приводит к повреждению раннее неповрежденных тканей, дестабилизирует гемодинамику,газообменидругиежизненноважныефункцииорганизма.
Традиционно в динамике травматической болезни выделяют два временных «пика»развитияпосттравматическойПОН.РанняяПОНвозникаетвпервые72часа

130 В.Д.ШЕЙКО  Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени
после травмы, поздняя – в более отсроченные роки. При этом в абсолютном боль- шинствеклиническихситуацийранняяилипервичнаяПОН–инициируетсяпервич- ным гипердинамическимССВР, вследствие массивнойтравматической и ишемиче- ской(шок)деструкциитканей.ПоздняяиливторичнаяПОН–чащеповторная«вол- на» органных дисфункций, возникающая на 5-е сутки после травмы и позднее. В абсолютномбольшинствеклиническихситуацийвторичнойПОНвыявляетсяболее или менее выраженная транзиторная органная дисфункция в период шока. Кроме того, у половины пострадавших инициирует вторичную ПОН повторный ССВР, обусловленныйинфекциейнафонеимеющегосяиммунодефицита.
Первичная или ранняя ПОН. При первичной ПОН расстройства функций органов непосредственно связаны с фактором внешнейагрессии – политравмой. Состояние функционально активных структур организма при этом определяется (1) непосредственным механическим разрушением тканей и их (2) гипоксическим поражениемвследствиенарушенияперфузиииишемиипришоке.
У большинства пострадавших с политравмой посттравматическая органная дисфункция, развившаяся в первые сутки после травмы, достаточно эффективно корригируется противошоковой терапией. Поэтому функциональную дисфункцию инедостаточностьвпервыедвоесутокименуюттранзиторнойинеквалифицируют как ПОН. Если же дисфункция оказывается резистентной к лечению в течение 48 часов с формированием устойчивой или прогрессирующей полиорганной недостаточности,токонстатируютсиндромПОН.
ССВР и первичная ПОН. Традиционно различают два варианта возникновения раннейПОН.Во-первых,ПОНможетявитьсяследствиемпервичногогипердинами- ческогоССВР,дезадаптирующегокомпенсаторныереакцииорганизмасразвитием картины рефрактерного декомпенсированного шока. Это, так называемая, однофазная пиковая модель первичного ПОН. Во-вторых, провоцировать первичную ПОНможетвторая«волна»ССВР,когдадезадаптированныйполитравмойорганизм на фоне умеренно выраженного первичного системного воспалительного ответа, подвергается дополнительной агрессии в первые 12-24 часа. Вентиляционная гипоксия, аспирация, реперфузия, массивная гемотрансфузия, травматичная стабилизация переломов, рецидив кровотечения – могут стать вторичным повреждающимфактором,провоцирующимпрогрессированиеПОН.Такойсценарийразвития первичнойПОНназываютдвухфазным.
ВобщейпатофизиологическойсхемеинициированныйССВРзначительноусугубляется пролонгированным нейро-эндокринным компонентом. Боль, беспокойство, психомоторное возбуждение и гипотермия усугубляют уже имеющиеся физиологические и метаболические расстройства увеличенным выбросом катехоламинов, что индуцирует состояние гиперметаболизма, вызывает повышение тонуса симпатической нервной системы. Тахикардия и периферическая вазоконстрикция усугубляют нарушение микроциркуляторной перфузии, дестабилизируют гемодинамику и подавляют иммунную защиту. Психическое возбуждение, бессонница приводят к усилению катаболизма, дальнейшему нарастанию потребности тканей вкислородесразвитиемкислороднойзадолженности.
