
- •Органика теория
- •1. Состав органических веществ, их многообразие. Место органической химии в системе естественных наук. Источники органических соединений.
- •2. Формирование и основные положения теории строения органических соединений (а.М. Бутлеров, а. Кекуле, а. Купер).
- •4. Основные признаки классификации органических веществ. Основные классы органических веществ.
- •5. Номенклатура органических соединений. Основные принципы построения названий органических соединений.
- •7. Типы связей в молекулах органических соединений. Σ- и π-связи. Гибридизация, понятие о молекулярных орбиталях.
- •8. Представление о механизмах реакций. Представление о промежуточных частицах: радикалы, карбокатионы, карбанионы. Классификация реагентов: радикалы, нуклеофилы, электрофилы.
- •9. Энергетический профиль реакции; энергетический барьер реакции, энергия активации, энергия переходного состояния, тепловой эффект реакции. Кинетический и термодинамический контроль.
- •10. Кислоты и основания (Бренстед, Льюис). Сопряженные кислоты и основания. Кислотно-основные равновесия. Константа кислотной ионизации и ее показатель (рКа).
- •11. Взаимное влияние атомов в молекулах, ионах, радикалах. Электронные и пространственные эффекты в органических реакциях (индуктивный эффект, эффект поля, мезомерный эффект, гиперконьюгация).
- •13. Гомологический ряд, номенклатура, электронное строение, sp3-гибридизация и физические свойства алканов.
- •14. Химические свойства алканов. Общие представления о механизме цепных радикальных реакций замещения в алканах (на примере реакции галогенирования).
- •15. Номенклатура, структурная и пространственная изомерия, электронное строение, sp2-гибридизация и физические свойства алкенов.
- •16. Химические свойства алкенов: каталитическое гидрирование, реакции электрофильного присоединения к двойной связи алкенов, их механизмы.
- •17. Химические свойства алкенов: реакции присоединения галогенов, галогеноводородов, воды. Правило Марковникова и его объяснение.
- •18. Представление о стереохимии присоединения галогенов у алкенов. Перегруппировки карбокатионов. Реакции радикального присоединения (по Харашу).
- •20. Окислительное расщепление алкенов (восстановительный и окислительный озонолиз). Гидроборирование алкенов и использование в синтезе спиртов.
- •21. Полимеризация алкенов как важнейший метод получения высокомолекулярных соединений. Полиэтилен, полипропилен. Понятие о стереорегулярных полимерах.
- •22. Аллильное хлорирование алкенов, механизм. Аллильный радикал. Окисление алкенов кислородом воздуха (пероксидное окисление).
- •23. Номенклатура, классификация, изомерия диеновых углеводородов.
- •25. Изопреновое звено в природных соединениях. Понятие об изопреноидах. Каучук. Синтетические каучуки.
- •26. Номенклатура, электронное строение, sp-гибридизация и физические свойства алкинов.
- •27. Химические свойства алкинов: каталитическое гидрирование и восстановление натрием в жидком аммиаке, использование в синтезе (z)- и (e)-алкенов.
- •28. Химические свойства алкинов: реакции электрофильного присоединения к тройной связи – галогенирование, гидрогалогенирование, гидратация (реакция Кучерова).
- •29. Кислотность ацетилена и терминальных алкинов. Димеризация, тримеризация ацетилена. Полиацетилен.
- •30. Классификация, номенклатура, структурная изомерия и пространственное строение циклоалканов.
- •32. Классификация и номенклатура аренов. Природа связей в молекуле бензола. Конденсированные ароматические углеводороды: нафталин, антрацен, фенантрен, бензпирен.
- •33. Ароматичность, критерии ароматичности. Правило Хюккеля.
- •35. Влияние заместителей в бензольном кольце на изомерный состав продуктов и скорость реакции. Активирующие и дезактивирующие заместители. Орто-, пара- и мета-ориентанты.
- •36. Реакции радикального замещения и окисления в боковой цепи. Причины устойчивости бензильных радикалов.
- •37. Классификация, номенклатура, изомерия галогенуглеводородов.
- •40. Литий- и магнийорганические соединения и их использование в органическом синтезе.
- •41. Биологическое действие галогенпроизводных, их применение в народном хозяйстве. Хлороформ, иодоформ, перфторуглеводороды, перфторполиэтилен (тефлон). Инсектициды.
- •42. Одноатомные спирты. Номенклатура, изомерия. Электронное строение. Физические свойства спиртов, роль водородной связи.
- •43. Химические свойства спиртов: кислотно-основные свойства. Алкоголяты металлов, их основные и нуклеофильные свойства.
- •44. Реакции нуклеофильного замещения с участием спиртов. Биологически важные реакции нуклеофильного замещения с участием эфиров фосфорных кислот.
- •45. Внутри- и межмолекулярная дегидратация спиртов (образование алкенов и простых эфиров). Окисление первичных и вторичных спиртов.
- •47. Фенолы. Номенклатура и изомерия. Простейшие представители: фенол, крезолы, пирокатехин, резорцин, гидрохинон, флороглюцин, пирогаллол. Электронное строение фенола. Кислотность фенолов.
- •48. Образование простых и сложных эфиров фенолов. Реакции электрофильного замещения в ряду фенолов (галогенирование, сульфирование, нитрование, алкилирование).
- •49. Карбоксилирование фенолятов щелочных металлов (реакция Кольбе). Окисление фенолов.
- •50. Хиноны и их биологическая роль. Фенольные соединения в природе. Витамин е. Флавоноиды.
- •51. Простые эфиры. Номенклатура, классификация. Расщепление кислотами. Образование гидропероксидов, их обнаружение и разложение. Циклические простые эфиры. Тетрагидрофуран. 1,4-Диоксан.
- •52. Оксираны: получение, взаимодействие с водой, аммиаком и аминами, магнийорганическими соединениями. Краун-эфиры: комплексообразование с ионами металлов, применение.
- •53. Кислотность тиолов. Нуклеофильные свойства тиолов, тиолятов и органических сульфидов. Окисление тиолов. Образование дисульфидов и их роль в биохимических процессах.
- •54. Классификация, номенклатура и изомерия аминов. Алифатические и ароматические амины, первичные, вторичные и третичные амины.
- •57. Классификация, номенклатура и изомерия карбонильных соединений.
- •58. Строение карбонильной группы в альдегидах и кетонах и реакции нуклеофильного присоединения (реактивами Гриньяра, циановодородом). Механизм реакций.
- •59. Реакции карбонильных соединений с гетеронуклеофилами: присоединение воды и спиртов, образование ацеталей. Реакции карбонильных соединений с аммиаком, аминами.
- •60. Реакции енольных форм карбонильных соединений: α-галогенирование, галоформное расщепление, изотопный обмен водорода. Альдольно-кротоновая конденсация, кислотный и основный катализ.
- •61. Взаимодействие неенолизирующихся альдегидов со щелочами (реакция Канниццаро). Реакции окисления и восстановления карбонильных соединений.
- •62. Монокарбоновые кислоты. Номенклатура. Строение карбоксильной группы и карбоксилат-иона. Кислотность карбоновых кислот.
- •63. Производные карбоновых кислот: сложные эфиры и тиоэфиры (s-эфиры карбоновых кислот), галогенангидриды, ангидриды, амиды, нитрилы, их получение и взаимопревращения.
- •64. Кислотный и щелочной гидролиз сложных эфиров и амидов.
- •65. Реакции ацилирования, этерификации, аминирования и восстановления карбоновых кислот и их производных.
- •66. Жирные кислоты, важнейшие представители (пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая). Жиры, сложные липиды (фосфатидовая кислота и ее производные), мыла.
- •67. Ненасыщенные карбоновые кислоты: акриловая, метакриловая, полимеры на их основе.
- •68. Дикарбоновые кислоты. Основные представители: щавелевая, малоновая, адипиновая, фталевые кислоты. Фумаровая и малеиновая кислоты. Полиэфирные волокна на основе терефталевой и адипиновой кислот.
- •69. Классификация углеводов. Биологическая роль и распространенность углеводов.
- •72. Дисахариды и их типы (восстанавливающие и невосстанавливающие). Сахароза, лактоза, мальтоза, целлобиоза.
- •73. Полисахариды (крахмал, целлюлоза, хитин, гликоген).
- •75. Классификация аминокислот. Основные представители природных α-аминокислот, их стереохимия.
- •76. Свойства аминокислот: амфотерность, изоэлектрическая точка. Реакции по карбоксильной и аминогруппе. Отношение к нагреванию.
- •77. Пептидная связь. Синтез пептидов: активация и защита функциональных групп аминокислот. Белки, их строение и биологическая роль
- •79. Шестичленные гетероциклы с одним гетероатомом: пиридин, хинолин, изохинолин. Ароматичность пиридина и особенности проведения реакций электрофильного замещения. Пиридин как основание.
35. Влияние заместителей в бензольном кольце на изомерный состав продуктов и скорость реакции. Активирующие и дезактивирующие заместители. Орто-, пара- и мета-ориентанты.
Ответ.
В молекуле незамещенного бензола
электронная плотность распределена
равномерно, поэтому электрофильный
реагент может атаковать в равной степени
любой из шести атомов углерода. Если в
бензольном кольце содержится какой-либо
заместитель, то под его влиянием
происходит перераспределение π-электронной
плотности цикла и новая группа вступает
уже в определенные положения по отношению
к имеющемуся заместителю. В реакциях
электрофильного замещения монозамещенных
бензола, в зависимости от электронной
природы заместителя, вступающая группа
может занимать преимущественно орто-,
мета- или пара-положения, а реакция
соответственно протекать быстрее или
медленнее, чем с незамещенным бензолом.
По влиянию на направление реакций
электрофильного замещения и реакционную
способность бензольного кольца
заместители можно разделить на две
группы — заместители I рода (орто-,
пара-ориентанты) и заместители II рода
(мета-ориентанты). К заместителям I рода
относятся атомы и атомные группы,
проявляющие положительный индуктивный
или положительный мезомерный эффекты:
—O–, —NR2, —NHR,
—NH2,
—OH,
—OR,
—NHCOR,
—OCOR,
—SR,
—F,
—Cl,
—Br,
—I, —Alk и др. Заместители I рода (за
исключением галогенов) увеличивают
электронную плотность в бензольном
кольце и тем самым активируют его в
реакциях электрофильного замещения.
Заместители I рода направляют замещение
преимущественно в орто- и параположения.
К заместителям II рода относятся группы,
проявляющие отрицательный индуктивный
или отрицательный мезомерный эффекты:
—NO2,
—SO3H,
—CN,
—CHO,
—COR,
—COOH,
—COOR,
—CONH2,
—CCl3
и др. Заместители II рода уменьшают
электронную плотность в бензольном
кольце и снижают скорость реакции
электрофильного замещения по сравнению
с незамещенным бензолом. Заместители
II рода направляют замещение преимущественно
в мета-положение. Ориентация замещения
не является абсолютной, а свидетельствует
лишь о предпочтительном направлении
реакции с преобладающим образованием
того или иного изомера. Так, при нитровании
нитробензола образуется 93 % мета-, 6 %
орто- и 1 % парадинитробензола. Механизм
влияния заместителей в бензольном
кольце на направление и скорость реакций
электрофильного замещения можно
объяснить с учетом электронных эффектов,
которые играют существенную роль как
в распределении электронной плотности
в стационарном состоянии молекулы
(статический фактор), так и в стабилизации
образующихся в процессе реакции
σ-комплексов (динамический фактор).
Заместители I рода (кроме галогенов) за
счет +I-или +М-эффекта проявляют
электронодонорные свойства. Они повышают
электронную плотность на всех атомах
углерода бензольного кольца, но в большей
степени на углеродных атомах в орто- и
пара-положениях (статический фактор).
Это является причиной облегчения
электрофильного замещения в сравнении
с реакциями SE у незамещенного бензола
и преимущественной атаки электрофильной
частицей орто- и пара-положений.
Заместители II рода, наоборот, за счет
–I- или –М-эффектов проявляют
электроноакцепторные свойства, вызывая
общее уменьшение электронной плотности
в бензольном кольце, но в большей степени
это влияние сказывается в ортои
пара-положениях. Поэтому они затрудняют
реакции электрофильного замещения
вообще и особенно с участием орто- и
пара-положений. В результате замещение
протекает преимущественно в мета-положении.
Наряду со статическим фактором
существенное, а в некоторых случаях
решающее влияние на направление
электрофильного замещения оказывает
динамический фактор. Его сущность
определяется влиянием имеющегося в
бензольном кольце заместителя на
устойчивость образующегося в момент
реакции того или иного σ-комплекса. Из
всех возможных σ-комплексов для молекулы
энергетически более выгодны те, в которых
имеется возможность дополнительной
делокализации положительного заряда
за счет заместителя. Эти σ-комплексы
обладают меньшей энергией, а следовательно,
они более устойчивы и поэтому их
образование в ходе реакции будет более
предпочтительным. В реакциях SЕ заместители
I рода вследствие своих электронодонорных
свойств повышают устойчивость всех
σ-комплексов по сравнению с незамещенным
бензолом и, таким образом, увеличивают
скорость реакции, но в большей степени
они стабилизируют σ-комплексы, отвечающие
продуктам орто- и паразамещения. Например,
при нитровании метоксибензола каждый
из σ-комплексов, образующихся в результате
орто-, мета- и пара-замещения, стабилизирован
за счет делокализации положительного
заряда между атомами углерода бензольного
кольца. Но в σ-комплексах при орто- и
пара-замещении положительный заряд
может быть дополнительно делокализован
с участием неподеленной пары электронов
атома кислорода метоксигруппы. Поэтому
образование их в ходе реакции более
предпочтительно. В результате образуются
преимущественно продукты орто- и
пара-замещения. Заместители ІІ рода
вследствие своих электроноакцепторных
свойств дестабилизируют в той или иной
мере все три возможных σ-комплекса и
тем самым затрудняют электрофильное
замещение в сравнении с незамещенным
бензолом. Однако σ-комплекс в мета-положении
дестабилизируется в меньшей степени,
чем σ-комплекс в орто- и пара-положениях.
Так, при нитровании нитробензола возможно
образование следующих σ-комплексов:

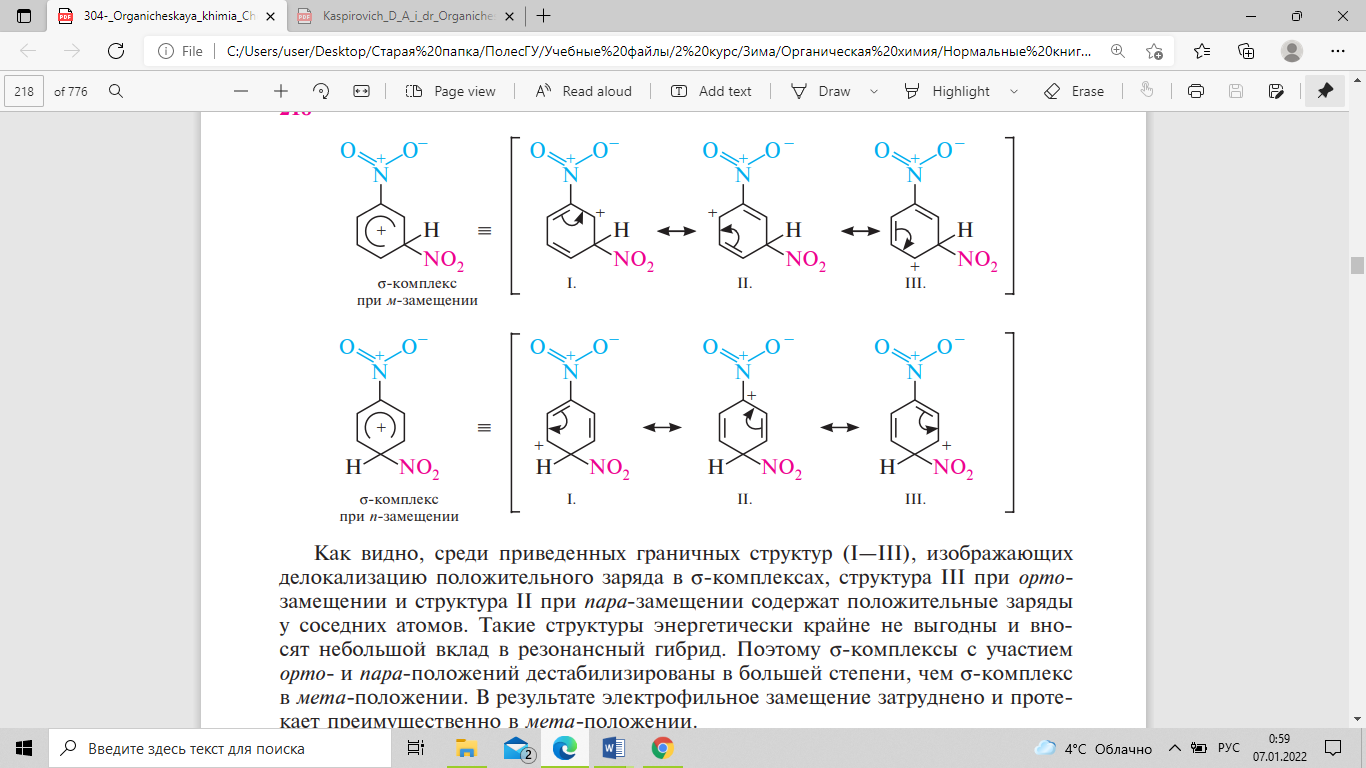 Такие
структуры энергетически крайне невыгодны
и вносят небольшой вклад в резонансный
гибрид. Поэтому σ-комплексы с участием
орто- и пара-положений дестабилизированы
в большей степени, чем σ-комплекс в
мета-положении. В результате электрофильное
замещение затруднено и протекает
преимущественно в мета-положении. В
большинстве случаев статический и
динамический факторы действуют
согласованно. Но если их влияние
проявляется в противоположных
направлениях, то решающее значение на
направление электрофильного замещения
оказывает динамический фактор. Наглядным
примером могут служить арилгалогениды,
в которых атомы галогена проявляют
электроноакцепторные свойства, но
вместе с тем направляют электрофильное
замещение в орто- и пара-положения.
Причиной такого поведения галогенов в
качестве заместителя является
несогласованное действие статического
и динамического факторов. Как известно,
атом галогена в бензольном ядре проявляет
отрицательный индуктивный и положительный
мезомерный эффекты, причем в статическом
состоянии –I-эффект значительнее
+М-эффекта. В результате происходит
смещение электронной плотности
бензольного кольца в сторону атома
галогена и, следовательно, реакционная
способность цикла по отношению к
электрофильным реагентам снижается.
Следовательно, в статическом состоянии
галогены, подобно ориентантам II рода,
затрудняют электрофильное замещение.
Однако в процессе реакции неподеленные
пары электронов атома галогена, которые
находятся в сопряжении с π-электронной
системой бензольного кольца, принимают
участие в дополнительной стабилизации
σ-комплексов, образующихся при орто- и
пара-замещении, но не участвуют в
стабилизации мета-σ-комплекса. Поэтому
галогены выступают как заместители I
рода и направляют электрофильное
замещение в орто- и пара-положения. Кроме
заместителей I и II рода, имеется небольшое
число заместителей, проявляющих смешанное
действие (—CH2NO2, —CH2Hal, —CH2OH, —CHHal2 и др.).
Эти заместители несколько затрудняют
электрофильное замещение в бензольном
ядре, но в результате реакции, как
правило, образуется смесь примерно
равных количеств орто-, мета- и
пара-изомеров.
Такие
структуры энергетически крайне невыгодны
и вносят небольшой вклад в резонансный
гибрид. Поэтому σ-комплексы с участием
орто- и пара-положений дестабилизированы
в большей степени, чем σ-комплекс в
мета-положении. В результате электрофильное
замещение затруднено и протекает
преимущественно в мета-положении. В
большинстве случаев статический и
динамический факторы действуют
согласованно. Но если их влияние
проявляется в противоположных
направлениях, то решающее значение на
направление электрофильного замещения
оказывает динамический фактор. Наглядным
примером могут служить арилгалогениды,
в которых атомы галогена проявляют
электроноакцепторные свойства, но
вместе с тем направляют электрофильное
замещение в орто- и пара-положения.
Причиной такого поведения галогенов в
качестве заместителя является
несогласованное действие статического
и динамического факторов. Как известно,
атом галогена в бензольном ядре проявляет
отрицательный индуктивный и положительный
мезомерный эффекты, причем в статическом
состоянии –I-эффект значительнее
+М-эффекта. В результате происходит
смещение электронной плотности
бензольного кольца в сторону атома
галогена и, следовательно, реакционная
способность цикла по отношению к
электрофильным реагентам снижается.
Следовательно, в статическом состоянии
галогены, подобно ориентантам II рода,
затрудняют электрофильное замещение.
Однако в процессе реакции неподеленные
пары электронов атома галогена, которые
находятся в сопряжении с π-электронной
системой бензольного кольца, принимают
участие в дополнительной стабилизации
σ-комплексов, образующихся при орто- и
пара-замещении, но не участвуют в
стабилизации мета-σ-комплекса. Поэтому
галогены выступают как заместители I
рода и направляют электрофильное
замещение в орто- и пара-положения. Кроме
заместителей I и II рода, имеется небольшое
число заместителей, проявляющих смешанное
действие (—CH2NO2, —CH2Hal, —CH2OH, —CHHal2 и др.).
Эти заместители несколько затрудняют
электрофильное замещение в бензольном
ядре, но в результате реакции, как
правило, образуется смесь примерно
равных количеств орто-, мета- и
пара-изомеров.
