
- •Органика теория
- •1. Состав органических веществ, их многообразие. Место органической химии в системе естественных наук. Источники органических соединений.
- •2. Формирование и основные положения теории строения органических соединений (а.М. Бутлеров, а. Кекуле, а. Купер).
- •4. Основные признаки классификации органических веществ. Основные классы органических веществ.
- •5. Номенклатура органических соединений. Основные принципы построения названий органических соединений.
- •7. Типы связей в молекулах органических соединений. Σ- и π-связи. Гибридизация, понятие о молекулярных орбиталях.
- •8. Представление о механизмах реакций. Представление о промежуточных частицах: радикалы, карбокатионы, карбанионы. Классификация реагентов: радикалы, нуклеофилы, электрофилы.
- •9. Энергетический профиль реакции; энергетический барьер реакции, энергия активации, энергия переходного состояния, тепловой эффект реакции. Кинетический и термодинамический контроль.
- •10. Кислоты и основания (Бренстед, Льюис). Сопряженные кислоты и основания. Кислотно-основные равновесия. Константа кислотной ионизации и ее показатель (рКа).
- •11. Взаимное влияние атомов в молекулах, ионах, радикалах. Электронные и пространственные эффекты в органических реакциях (индуктивный эффект, эффект поля, мезомерный эффект, гиперконьюгация).
- •13. Гомологический ряд, номенклатура, электронное строение, sp3-гибридизация и физические свойства алканов.
- •14. Химические свойства алканов. Общие представления о механизме цепных радикальных реакций замещения в алканах (на примере реакции галогенирования).
- •15. Номенклатура, структурная и пространственная изомерия, электронное строение, sp2-гибридизация и физические свойства алкенов.
- •16. Химические свойства алкенов: каталитическое гидрирование, реакции электрофильного присоединения к двойной связи алкенов, их механизмы.
- •17. Химические свойства алкенов: реакции присоединения галогенов, галогеноводородов, воды. Правило Марковникова и его объяснение.
- •18. Представление о стереохимии присоединения галогенов у алкенов. Перегруппировки карбокатионов. Реакции радикального присоединения (по Харашу).
- •20. Окислительное расщепление алкенов (восстановительный и окислительный озонолиз). Гидроборирование алкенов и использование в синтезе спиртов.
- •21. Полимеризация алкенов как важнейший метод получения высокомолекулярных соединений. Полиэтилен, полипропилен. Понятие о стереорегулярных полимерах.
- •22. Аллильное хлорирование алкенов, механизм. Аллильный радикал. Окисление алкенов кислородом воздуха (пероксидное окисление).
- •23. Номенклатура, классификация, изомерия диеновых углеводородов.
- •25. Изопреновое звено в природных соединениях. Понятие об изопреноидах. Каучук. Синтетические каучуки.
- •26. Номенклатура, электронное строение, sp-гибридизация и физические свойства алкинов.
- •27. Химические свойства алкинов: каталитическое гидрирование и восстановление натрием в жидком аммиаке, использование в синтезе (z)- и (e)-алкенов.
- •28. Химические свойства алкинов: реакции электрофильного присоединения к тройной связи – галогенирование, гидрогалогенирование, гидратация (реакция Кучерова).
- •29. Кислотность ацетилена и терминальных алкинов. Димеризация, тримеризация ацетилена. Полиацетилен.
- •30. Классификация, номенклатура, структурная изомерия и пространственное строение циклоалканов.
- •32. Классификация и номенклатура аренов. Природа связей в молекуле бензола. Конденсированные ароматические углеводороды: нафталин, антрацен, фенантрен, бензпирен.
- •33. Ароматичность, критерии ароматичности. Правило Хюккеля.
- •35. Влияние заместителей в бензольном кольце на изомерный состав продуктов и скорость реакции. Активирующие и дезактивирующие заместители. Орто-, пара- и мета-ориентанты.
- •36. Реакции радикального замещения и окисления в боковой цепи. Причины устойчивости бензильных радикалов.
- •37. Классификация, номенклатура, изомерия галогенуглеводородов.
- •40. Литий- и магнийорганические соединения и их использование в органическом синтезе.
- •41. Биологическое действие галогенпроизводных, их применение в народном хозяйстве. Хлороформ, иодоформ, перфторуглеводороды, перфторполиэтилен (тефлон). Инсектициды.
- •42. Одноатомные спирты. Номенклатура, изомерия. Электронное строение. Физические свойства спиртов, роль водородной связи.
- •43. Химические свойства спиртов: кислотно-основные свойства. Алкоголяты металлов, их основные и нуклеофильные свойства.
- •44. Реакции нуклеофильного замещения с участием спиртов. Биологически важные реакции нуклеофильного замещения с участием эфиров фосфорных кислот.
- •45. Внутри- и межмолекулярная дегидратация спиртов (образование алкенов и простых эфиров). Окисление первичных и вторичных спиртов.
- •47. Фенолы. Номенклатура и изомерия. Простейшие представители: фенол, крезолы, пирокатехин, резорцин, гидрохинон, флороглюцин, пирогаллол. Электронное строение фенола. Кислотность фенолов.
- •48. Образование простых и сложных эфиров фенолов. Реакции электрофильного замещения в ряду фенолов (галогенирование, сульфирование, нитрование, алкилирование).
- •49. Карбоксилирование фенолятов щелочных металлов (реакция Кольбе). Окисление фенолов.
- •50. Хиноны и их биологическая роль. Фенольные соединения в природе. Витамин е. Флавоноиды.
- •51. Простые эфиры. Номенклатура, классификация. Расщепление кислотами. Образование гидропероксидов, их обнаружение и разложение. Циклические простые эфиры. Тетрагидрофуран. 1,4-Диоксан.
- •52. Оксираны: получение, взаимодействие с водой, аммиаком и аминами, магнийорганическими соединениями. Краун-эфиры: комплексообразование с ионами металлов, применение.
- •53. Кислотность тиолов. Нуклеофильные свойства тиолов, тиолятов и органических сульфидов. Окисление тиолов. Образование дисульфидов и их роль в биохимических процессах.
- •54. Классификация, номенклатура и изомерия аминов. Алифатические и ароматические амины, первичные, вторичные и третичные амины.
- •57. Классификация, номенклатура и изомерия карбонильных соединений.
- •58. Строение карбонильной группы в альдегидах и кетонах и реакции нуклеофильного присоединения (реактивами Гриньяра, циановодородом). Механизм реакций.
- •59. Реакции карбонильных соединений с гетеронуклеофилами: присоединение воды и спиртов, образование ацеталей. Реакции карбонильных соединений с аммиаком, аминами.
- •60. Реакции енольных форм карбонильных соединений: α-галогенирование, галоформное расщепление, изотопный обмен водорода. Альдольно-кротоновая конденсация, кислотный и основный катализ.
- •61. Взаимодействие неенолизирующихся альдегидов со щелочами (реакция Канниццаро). Реакции окисления и восстановления карбонильных соединений.
- •62. Монокарбоновые кислоты. Номенклатура. Строение карбоксильной группы и карбоксилат-иона. Кислотность карбоновых кислот.
- •63. Производные карбоновых кислот: сложные эфиры и тиоэфиры (s-эфиры карбоновых кислот), галогенангидриды, ангидриды, амиды, нитрилы, их получение и взаимопревращения.
- •64. Кислотный и щелочной гидролиз сложных эфиров и амидов.
- •65. Реакции ацилирования, этерификации, аминирования и восстановления карбоновых кислот и их производных.
- •66. Жирные кислоты, важнейшие представители (пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая). Жиры, сложные липиды (фосфатидовая кислота и ее производные), мыла.
- •67. Ненасыщенные карбоновые кислоты: акриловая, метакриловая, полимеры на их основе.
- •68. Дикарбоновые кислоты. Основные представители: щавелевая, малоновая, адипиновая, фталевые кислоты. Фумаровая и малеиновая кислоты. Полиэфирные волокна на основе терефталевой и адипиновой кислот.
- •69. Классификация углеводов. Биологическая роль и распространенность углеводов.
- •72. Дисахариды и их типы (восстанавливающие и невосстанавливающие). Сахароза, лактоза, мальтоза, целлобиоза.
- •73. Полисахариды (крахмал, целлюлоза, хитин, гликоген).
- •75. Классификация аминокислот. Основные представители природных α-аминокислот, их стереохимия.
- •76. Свойства аминокислот: амфотерность, изоэлектрическая точка. Реакции по карбоксильной и аминогруппе. Отношение к нагреванию.
- •77. Пептидная связь. Синтез пептидов: активация и защита функциональных групп аминокислот. Белки, их строение и биологическая роль
- •79. Шестичленные гетероциклы с одним гетероатомом: пиридин, хинолин, изохинолин. Ароматичность пиридина и особенности проведения реакций электрофильного замещения. Пиридин как основание.
22. Аллильное хлорирование алкенов, механизм. Аллильный радикал. Окисление алкенов кислородом воздуха (пероксидное окисление).
Ответ.
При действии на алкены галогенирующих
реагентов (Cl2, N-бромсукцинимид и др.) в
присутствии инициаторов процесса
образования свободных радикалов
(пероксиды, температура, УФ-свет)
происходит не присоединение галогена
по месту разрыва двойной связи, а
свободнорадикальное замещение на
галоген атома водорода, находящегося
при атоме углерода в α-положении к
двойной связи (аллильное положение).
Так, при температуре 500—600 °С пропен
реагирует с хлором, образуя аллилхлорид:
![]() .
Реакция используется в промышленном
синтезе глицерина. Аллильное галогенирование
протекает по свободнорадикальному
механизму и включает стадию образования
аллильного радикала. В цепном процессе
выделяют три стадии: инициирование,
рост цепи, обрыв цепи. Инициирование.
Под действием энергии квантов света
(hn) или нагревания молекула хлора
активируется и претерпевает гомолитический
разрыв связи с образованием двух
свободных радикалов: Cl· ·Cl hn 2Cl·. Рост
цепи. Свободные радикалы хлора атакуют
связь С—Н в молекуле, отрывая при этом
атом водорода с образованием хлороводорода
HCl и свободного радикала, он, в свою
очередь, атакует молекулу хлора, отрывает
атом галогена. Образовавшийся радикал
хлора повторяет цикл указанных
превращений, то есть происходит цепной
процесс, в котором атом хлора,
прореагировавший на предыдущей стадии
роста цепи, способствует высвобождению
нового радикала хлора на последующей
стадии. Цепной процесс прекращается
только после исчезновения всех свободных
радикалов, образующихся в ходе реакции.
Обрыв цепи. В результате рекомбинации
(димеризации) свободных радикалов
происходит обрыв цепи. В результате
сопряжения неспаренного электрона с
π-электронами двойной связи аллильные
радикалы являются более устойчивыми,
чем обычные алкильные радикалы:
.
Реакция используется в промышленном
синтезе глицерина. Аллильное галогенирование
протекает по свободнорадикальному
механизму и включает стадию образования
аллильного радикала. В цепном процессе
выделяют три стадии: инициирование,
рост цепи, обрыв цепи. Инициирование.
Под действием энергии квантов света
(hn) или нагревания молекула хлора
активируется и претерпевает гомолитический
разрыв связи с образованием двух
свободных радикалов: Cl· ·Cl hn 2Cl·. Рост
цепи. Свободные радикалы хлора атакуют
связь С—Н в молекуле, отрывая при этом
атом водорода с образованием хлороводорода
HCl и свободного радикала, он, в свою
очередь, атакует молекулу хлора, отрывает
атом галогена. Образовавшийся радикал
хлора повторяет цикл указанных
превращений, то есть происходит цепной
процесс, в котором атом хлора,
прореагировавший на предыдущей стадии
роста цепи, способствует высвобождению
нового радикала хлора на последующей
стадии. Цепной процесс прекращается
только после исчезновения всех свободных
радикалов, образующихся в ходе реакции.
Обрыв цепи. В результате рекомбинации
(димеризации) свободных радикалов
происходит обрыв цепи. В результате
сопряжения неспаренного электрона с
π-электронами двойной связи аллильные
радикалы являются более устойчивыми,
чем обычные алкильные радикалы:
![]() .
Поэтому замещение атома водорода на
атом галогена в аллильном положении
алкенов происходит легче, чем в алканах.
Аллил
— углеводородный радикал, производное
пропилена, у которого удален атом
водорода от третьего атома углерода.
Аллильная группа — органический
заместитель, часть химического соединения,
которое имеет вид CH2=CH-CH2-R. Соединения с
аллильной группой часто встречаются в
природе в растениях. Своё название аллил
получил от латинского названия чеснока
— Allium sativum.
.
Поэтому замещение атома водорода на
атом галогена в аллильном положении
алкенов происходит легче, чем в алканах.
Аллил
— углеводородный радикал, производное
пропилена, у которого удален атом
водорода от третьего атома углерода.
Аллильная группа — органический
заместитель, часть химического соединения,
которое имеет вид CH2=CH-CH2-R. Соединения с
аллильной группой часто встречаются в
природе в растениях. Своё название аллил
получил от латинского названия чеснока
— Allium sativum.
23. Номенклатура, классификация, изомерия диеновых углеводородов.
Ответ.
Алкадиенами называют алифатические
углеводороды, содержащие две двойные
углеродуглеродные связи. Общая
формула алкадиенов СnН2n–2. В зависимости
от расположения двойных связей в молекуле
различают три
основных типа
алкадиенов: Алкадиены с кумулированными
двойными связями (двойные связи
расположены у одного атома углерода)
С——С——С . Такие соединения называют
алленами (по тривиальному названию
простейшего представителя этого ряда
— аллена). Алкадиены с сопряженными
двойными связями (двойные связи разделены
одной простой C—C-связью). Алкадиены с
изолированными двойными связями (двойные
связи разделены одним и более
sp3-гибридизованными атомами углерода).
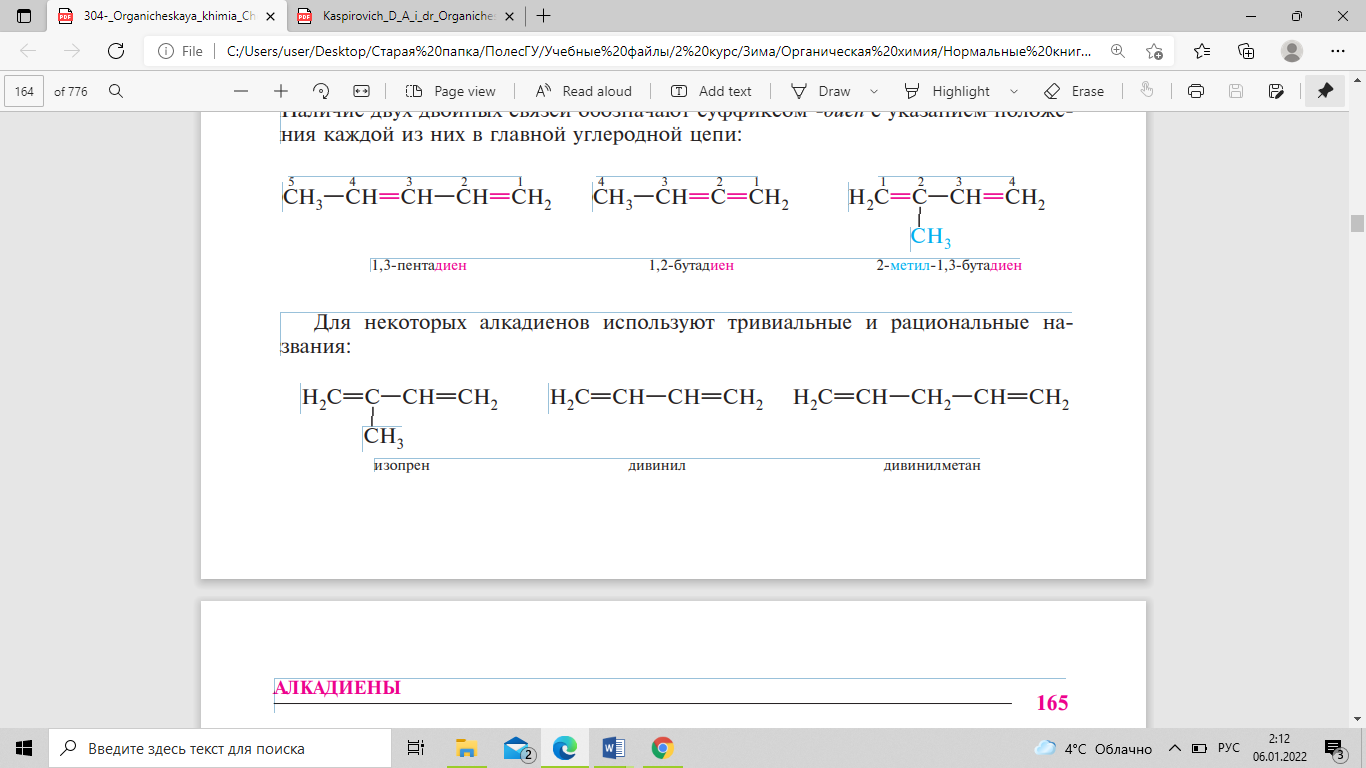
Названия алкадиенов по номенклатуре
IUPAC образуют аналогично алкенам.
Наличие двух двойных связей обозначают
суффиксом -диен с указанием положения
каждой из них в главной углеродной цепи.
Для некоторых алкадиенов используют
тривиальные и рациональные названия:
 В
молекуле алкадиенов с кумулированной
системой двойных связей атом углерода,
образующий две двойные связи, находится
в состоянии sp-гибридизации, а соседние
с ним атомы углерода — в sp2-гибридизации.
Эти три атома углерода расположены в
пространстве линейно, а π-связи находятся
в двух взаимно перпендикулярных
плоскостях. Четыре заместителя при
углеродных атомах в sp2-гибридизации
тоже расположены в двух взаимно
перпендикулярных плоскостях. Вследствие
такого пространственного строения
молекулы алленов, у которых при каждом
из атомов углерода в sp2-гибридизации
имеются разные заместители, являются
хиральными, а следовательно, для них
возможна оптическая изомерия:
В
молекуле алкадиенов с кумулированной
системой двойных связей атом углерода,
образующий две двойные связи, находится
в состоянии sp-гибридизации, а соседние
с ним атомы углерода — в sp2-гибридизации.
Эти три атома углерода расположены в
пространстве линейно, а π-связи находятся
в двух взаимно перпендикулярных
плоскостях. Четыре заместителя при
углеродных атомах в sp2-гибридизации
тоже расположены в двух взаимно
перпендикулярных плоскостях. Вследствие
такого пространственного строения
молекулы алленов, у которых при каждом
из атомов углерода в sp2-гибридизации
имеются разные заместители, являются
хиральными, а следовательно, для них
возможна оптическая изомерия:
 Если
двойные связи в молекуле разделены
одной углерод-углеродной σ-связью
(алкадиены с сопряженными связями),
происходит дополнительное перекрывание
р-электронных облаков соседних π-связей
(π,π-сопряжение) и образуется единая
π-электронная система, в которой
π-электроны уже не принадлежат отдельным
связям, а делокализованы по всей системе.
Перераспределение электронной плотности
в молекуле приводит к укорочению σ-связи,
расположенной между этиленовыми
группами, и сопровождается выделением
энергии, что способствует повышению
стабильности системы. Эту энергию
называют энергией сопряжения. Так, в
молекуле 1,3-бутадиена длина связи С-2—С-3
составляет 0,148 нм, тогда как длина связи
С—С в этане равна 0,154 нм. Энергия
сопряжения 1,3-бутадиена составляет
примерно 15 кДж/моль. С помощью метода
электронографии установлено, что
алкадиены с сопряженными связями имеют
преимущественно трансоидную конформацию
(транс-расположение двойных связей по
отношению к одинарной). Алкадиены с
изолированными двойными связями
построены аналогично алкенам. Особенности
строения алкадиенов различных типов
сказываются на их реакционной способности.
В частности, алкадиены с кумулированными
и изолированными связями по химическим
свойствам во многом напоминают алкены.
Они легко вступают в многочисленные
реакции присоединения, только в них
принимает участие не одна, а две двойные
связи. Алкадиены с сопряженными двойными
связями проявляют своеобразные химические
свойства.
Если
двойные связи в молекуле разделены
одной углерод-углеродной σ-связью
(алкадиены с сопряженными связями),
происходит дополнительное перекрывание
р-электронных облаков соседних π-связей
(π,π-сопряжение) и образуется единая
π-электронная система, в которой
π-электроны уже не принадлежат отдельным
связям, а делокализованы по всей системе.
Перераспределение электронной плотности
в молекуле приводит к укорочению σ-связи,
расположенной между этиленовыми
группами, и сопровождается выделением
энергии, что способствует повышению
стабильности системы. Эту энергию
называют энергией сопряжения. Так, в
молекуле 1,3-бутадиена длина связи С-2—С-3
составляет 0,148 нм, тогда как длина связи
С—С в этане равна 0,154 нм. Энергия
сопряжения 1,3-бутадиена составляет
примерно 15 кДж/моль. С помощью метода
электронографии установлено, что
алкадиены с сопряженными связями имеют
преимущественно трансоидную конформацию
(транс-расположение двойных связей по
отношению к одинарной). Алкадиены с
изолированными двойными связями
построены аналогично алкенам. Особенности
строения алкадиенов различных типов
сказываются на их реакционной способности.
В частности, алкадиены с кумулированными
и изолированными связями по химическим
свойствам во многом напоминают алкены.
Они легко вступают в многочисленные
реакции присоединения, только в них
принимает участие не одна, а две двойные
связи. Алкадиены с сопряженными двойными
связями проявляют своеобразные химические
свойства.
24. Сопряженные диены (1,3-бутадиен и изопрен), сопряжение двойных связей (π,π-сопряжение) и реакции электрофильного присоединения. Диеновый синтез (реакция Дильса-Альдера), представление о механизме реакции.
Ответ.
Если двойные связи в молекуле разделены
одной углерод-углеродной σ-связью
(алкадиены с сопряженными
связями),
происходит дополнительное перекрывание
р-электронных облаков соседних π-связей
(π,π-сопряжение)
и образуется единая π-электронная
система, в которой π-электроны уже не
принадлежат отдельным связям, а
делокализованы по всей системе.
Перераспределение электронной плотности
в молекуле приводит к укорочению σ-связи,
расположенной между этиленовыми
группами, и сопровождается выделением
энергии, что способствует повышению
стабильности системы. Эту энергию
называют энергией сопряжения. Так, в
молекуле 1,3-бутадиена длина связи С-2—С-3
составляет 0,148 нм, тогда как длина связи
С—С в этане равна 0,154 нм. Энергия
сопряжения 1,3-бутадиена составляет
примерно 15 кДж/моль.С помощью метода
электронографии установлено, что
алкадиены с сопряженными связями имеют
преимущественно трансоидную конформацию
(трансрасположение двойных связей по
отношению к одинарной). Для алкадиенов
с сопряженными связями характерны
реакции присоединения и полимеризации,
свойственные алкенам. Однако в химическом
поведении 1,3-алкадиенов имеются и
некоторые особенности. Во-первых, по
сравнению с алкенами сопряженные диены
проявляют более высокую реакционную
способность. Во-вторых, в реакциях
электрофильного присоединения чаще
всего образуется два продукта, из которых
один является результатом присоединения
по месту двойной связи (1,2-присоединение),
а второй — по концам сопряженной системы
(1,4-присоединение). Соотношение этих
продуктов зависит от условий проведения
реакции (температуры, растворителя), а
также природы электрофильного
реагента. Водород
в момент выделения образует с
1,3-алкадиенами обычно продукты
1,4-присоединения:
![]() В
присутствии катализаторов (Ni, Рt)
1,3-алкадиены присоединяют водород в
1,2- и 1,4-положения с образованием
соответствующих алкенов, которые
подвергаются дальнейшему гидрированию
до алканов:
Присоединение
галогенов
к сопряженным диенам приводит к
образованию смеси продуктов 1,2- и
1,4-присоединения, состав которой зависит
от природы галогена, структуры диенового
углеводорода и условий проведения
реакции. Как правило, при повышении
температуры и переходе от хлора к йоду
возрастает выход продукта 1,4-присоединения.
В процессе бромирования 1,3-бутадиена
при температуре –80 °С образуется
преимущественно продукт 1,2-присоединения,
а при 40 °С — продукт 1,4-присоединения:
В
присутствии катализаторов (Ni, Рt)
1,3-алкадиены присоединяют водород в
1,2- и 1,4-положения с образованием
соответствующих алкенов, которые
подвергаются дальнейшему гидрированию
до алканов:
Присоединение
галогенов
к сопряженным диенам приводит к
образованию смеси продуктов 1,2- и
1,4-присоединения, состав которой зависит
от природы галогена, структуры диенового
углеводорода и условий проведения
реакции. Как правило, при повышении
температуры и переходе от хлора к йоду
возрастает выход продукта 1,4-присоединения.
В процессе бромирования 1,3-бутадиена
при температуре –80 °С образуется
преимущественно продукт 1,2-присоединения,
а при 40 °С — продукт 1,4-присоединения:
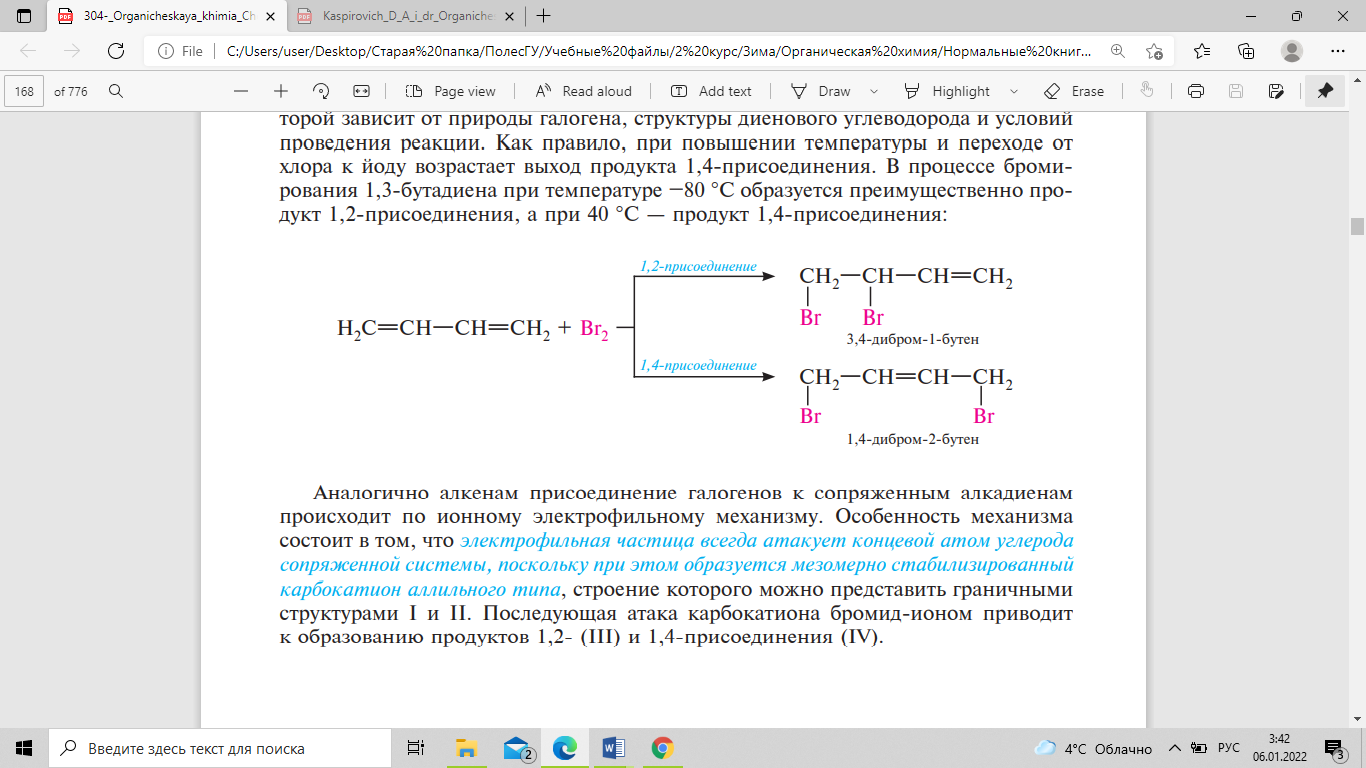 Аналогично
алкенам присоединение галогенов к
сопряженным алкадиенам происходит по
ионному электрофильному механизму.
Особенность механизма состоит в том,
что электрофильная частица всегда
атакует концевой атом углерода сопряженной
системы, поскольку при этом образуется
мезомерно стабилизированный карбокатион
аллильного типа, строение которого
можно представить граничными структурами
I и II. Последующая атака карбокатиона
бромид-ионом приводит к образованию
продуктов 1,2- (III) и 1,4-присоединения (IV).
Как и в случае галогенирования,
присоединение к сопряженным диенам
галогеноводородов
происходит с образованием продуктов
1,2- и 1,4-присоединения. Реакция
Дильса—Альдера
основана на взаимодействии сопряженных
диенов с диенофилами — веществами,
имеющими в своем составе двойную или
тройную углерод-углеродную связь.
Особенно легко эта реакция происходит
с диенофилами, содержащими активированную
двойную связь, то есть когда двойная
связь находится в сопряжении с
электроноакцепторной или электронодонорной
группой (—СN, —NO2, —СНО, —СОR, —СООН,
—СООR, —Hal, —ОR и др.). В процессе реакции
сопряженные диены присоединяют диенофилы
в положение 1,4 с образованием циклических
структур:
Аналогично
алкенам присоединение галогенов к
сопряженным алкадиенам происходит по
ионному электрофильному механизму.
Особенность механизма состоит в том,
что электрофильная частица всегда
атакует концевой атом углерода сопряженной
системы, поскольку при этом образуется
мезомерно стабилизированный карбокатион
аллильного типа, строение которого
можно представить граничными структурами
I и II. Последующая атака карбокатиона
бромид-ионом приводит к образованию
продуктов 1,2- (III) и 1,4-присоединения (IV).
Как и в случае галогенирования,
присоединение к сопряженным диенам
галогеноводородов
происходит с образованием продуктов
1,2- и 1,4-присоединения. Реакция
Дильса—Альдера
основана на взаимодействии сопряженных
диенов с диенофилами — веществами,
имеющими в своем составе двойную или
тройную углерод-углеродную связь.
Особенно легко эта реакция происходит
с диенофилами, содержащими активированную
двойную связь, то есть когда двойная
связь находится в сопряжении с
электроноакцепторной или электронодонорной
группой (—СN, —NO2, —СНО, —СОR, —СООН,
—СООR, —Hal, —ОR и др.). В процессе реакции
сопряженные диены присоединяют диенофилы
в положение 1,4 с образованием циклических
структур:
 Реакция
Дильса–Альдера протекает по молекулярному
механизму, который характеризуется
синхронным процессом разрыва и образования
связей в реагентах. Эта реакция относится
к реакциям [4+2]-циклоприсоединения,
поскольку в ней принимает участие
4π-электронная система диена и
2π-электронная система диенофила. Реакция
впервые была открыта в 1928 году немецкими
химиками Дильсом и Альдером. Диеновый
синтез широко используется для синтеза
полициклических соединений, в том числе
при синтезе биологически активных
соединений сложного строения.
Реакция
Дильса–Альдера протекает по молекулярному
механизму, который характеризуется
синхронным процессом разрыва и образования
связей в реагентах. Эта реакция относится
к реакциям [4+2]-циклоприсоединения,
поскольку в ней принимает участие
4π-электронная система диена и
2π-электронная система диенофила. Реакция
впервые была открыта в 1928 году немецкими
химиками Дильсом и Альдером. Диеновый
синтез широко используется для синтеза
полициклических соединений, в том числе
при синтезе биологически активных
соединений сложного строения.
