
- •Введение в биохимию
- •Биохимия
- •Признаки живой материи:
- •Признаки живой материи:
- •Место в структуре программы специалитета. Биохимия относится к дисциплинам базовой части.
- •Объекты биохимических исследований. Современные направления исследований.
- •Биохимические анализы крови, мочи, ликвора, слюны -
- •Клиническая биохимия -
- •Структура дисциплины
- •Успехов в освоении дисциплины!
- •Вся наша жизнь - нелепое чудо, пробившееся в реальность вопреки всем законам мироздания.
- •Проблемы и задачи протеомики в медицине
- •Основные вопросы лекции:
- •Белки (протеины)
- •«Жизнь есть способ существования белковых тел» Ф. Энгельс
- •Международный проект «Протеом человека» (Human Proteome Project, НРР)
- •Белки – высокомолекулярные органические полимеры, построенные из аминокислот, связанных между собой
- •В процессе биосинтеза белка в полипептидную цепь включаются 20 α-аминокислот, кодируемых генетическим кодом
- •Качественный состав белка зависит от состава аминокислот.
- •Строение белков
- •Первичная структура белка. Аминокислоты могут ковалентно связываться друг
- •Характеристика пептидной связи
- •Пептидные связи очень прочны и самопроизвольно не разрываются при нормальных условиях.
- •Количество аминокислот в составе пептидов (белков) может сильно варьировать.
- •В организме вырабатывается множество пептидов, участвующих в регуляции биологических процессов и обладающих высокой
- •Молекулярная масса (ММ) белка зависит от количества
- •Роль первичной структуры
- •Вторичная структура белков -
- •Пептидные цепи могут приобретать структуры 2 типов:
- •β- структура
- •Нерегулярные вторичные структуры
- •Третичная структура белков -
- •Третичная структура белка
- •Фолдинг -
- •Форма белковой молекулы
- •Растворимость белка определяется его структурой
- •ИЭТ – индивидуальная характеристика белка
- •Центр связывания белка (активный центр) - участок
- •Этапы формирования функционально активного белка. В основе функционирования любого белка лежит его способность
- •Домен белка— элемент третичной структуры белка.
- •Сложные белки (холопротеины)
- •Сложные белки
- •Белки обладают антигенными свойствами.
- •Конформационная лабильность белков -
- •Четвертичная структура белков. Характеризуются белки, состоящие из 2 и более полипептидных цепей.
- •ОСОБЕННОСТИ ФУНКЦИОНИРОВАНИЯ ОЛИГОМЕРНЫХ БЕЛКОВ
- •Гемоглобин (НЬ) — олигомерный белок, состоит из 4 протомеров
- •Кооперативные изменения конформации протомеров Нb ускоряют нагрузку О2 в легких и разгрузку в
- •Изменение конформации облегчает взаимодействие следующего
- •Характерная для гемоглобина S-образная кривая насыщения О2 свидетельствует, что связывание первой молекулы О2
- •Размер белка может измеряться в числе аминокислотных остатков или в дальтонах (молекулярная масса,
- •Денатурация белка -
- •Денатурация белка. Ренативация белка.
- •Применение денатурирующих агентов в биологических исследованиях и медицине
- •Полиморфизм белков -
- •Полиморфизм белков в онтогенезе. Изофункциональные белки.
- •Полиморфизм белков при патологии. ИЗМЕНЕНИЯ БЕЛКОВОГО СОСТАВА ОРГАНИЗМА
- •Первичные протеинопатии.
- •Прионы
- •Вторичные протеинопатии: причины и следствия
- •Благодарю за внимание!

Успехов в освоении дисциплины!

Вся наша жизнь - нелепое чудо, пробившееся в реальность вопреки всем законам мироздания. Мы родились, мы живем, мы ссоримся и миримся, мы существуем - оргия биохимии в восьмидесяти среднестатистических килограммах. Вы до
сих пор верите, что сложные биохимические реакции научили Вас любить? Это Ваше право.
Сергей Лукьяненко

Проблемы и задачи протеомики в медицине

Основные вопросы лекции:
Строение и функции белков.
Классификация и физико-химические свойства протеиногенных аминокислот.
Классификация белков: простые и сложные, глобулярные и фибриллярные, мономерные и олигомерные.
Физико-химические свойства белков: растворимость, ионизация, гидратация, осаждение.
Уровни структурной организации белков: первичная, вторичная, надвторичная, третичная и четвертичная структуры, домены, надмолекулярные структуры.
Связи, поддерживающие структуры белка: дисульфидные, ионные, водородные, гидрофобные. Взаимосвязь структуры и функции.
Денатурация и ренатурация.
Миоглобин и гемоглобин. Конформационные изменения и кооперативные взаимодействия субъединиц гемоглобина.
Роль протеомики в оценке патологических состояний.

Белки (протеины)
Структура изучалась с середины XVIII в.
Г. Мульдер (Голландия) в начале XIX в. предложил
термин «протеины» (от греч. Protos – первый).
Термином «белок» в России стали называть
вещества, выделяемые из организма и имеющие сходство в строении с белком куриного яйца.
|
Герман Эмиль Фишер (1852 - 1919) |
|
|
|
создал пептидную теорию строения |
|
белков |
(Нобелевская |
|
премия по химии, 1902 ). |
|
|
В 30-е годы XX века впервые выделены и |
|
|
|
получены белки в кристаллическом виде |
|
В 50-е годы ХХ века установлена вторичная и |
|
|
|
третичная структуры белковой молекулы. |

«Жизнь есть способ существования белковых тел» Ф. Энгельс
●В организме человека на долю белков приходится до 1/4 массы тела (~15 кг).
●Белки составляют основу структуры всех клеток.
●Фенотипические признаки каждого организма обусловлены определенным набором белков.
●Известно > 100.000 белков организма человека, выполняющих разные функции.
Сбелками (протеинами) связаны следующие свойства живого организма:Разнообразие структур и их высокая упорядоченностьСпособность к воспроизведению себе подобныхСократимость и движениеОбмен веществ и др.

|
Ферменты |
|
> 50% |
Регуляторная |
Транспортная |
Защитная |
Функции |
Резервная |
|
белков |
|||
|
|
Структурная |
Рецепторная |
Сократи- тельная

Международный проект «Протеом человека» (Human Proteome Project, НРР)
международный проект по созданию протеомной карты, включающей все белки, кодируемые геномом человека.
Первоочередной задачей проекта является составление протеомных карт основных белков плазмы крови, печени, головного мозга.
Ворганизме 26000 генов (геном человека) кодируют структуру белков. Протеом человека – отображение генетической информации в конкретной структуре и функции каждой молекулы белка.
Участие России в проекте – изучение протеома 18-й хромосомы
(30.000 белков, кодируемых 286 генами)
Изучение протеома 18-й хромосомы позволит определить параметры состава белков здорового человека и создать системы диагностики
различных заболеваний
(шизофрения, диабет, гепатит В, болезнь Паркинсона, рак и др.)
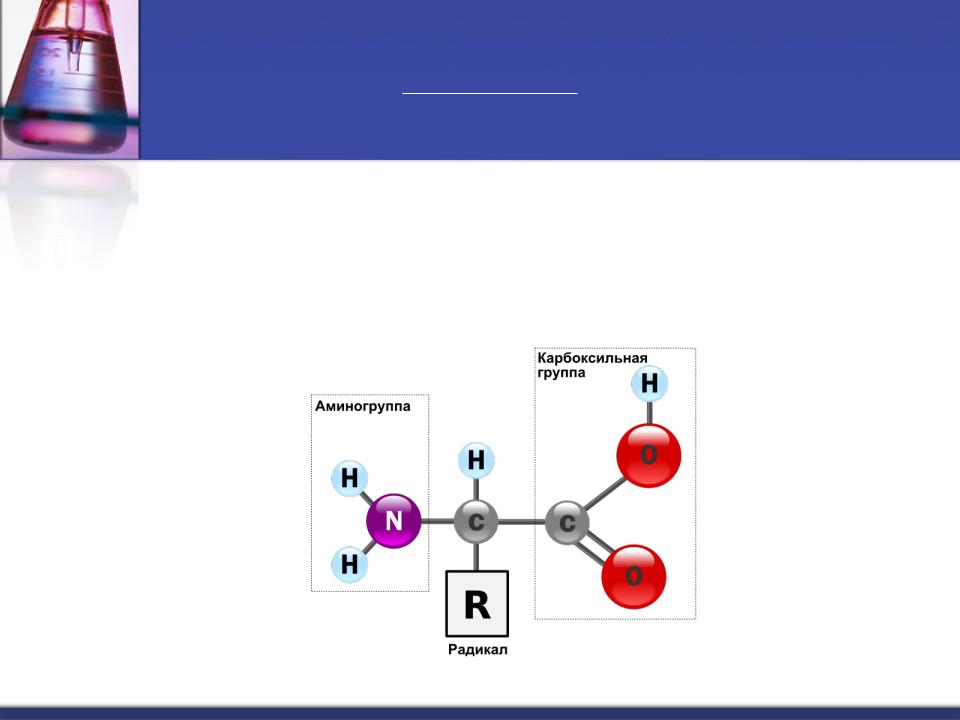
Белки – высокомолекулярные органические полимеры, построенные из аминокислот, связанных между собой
пептидными связями.
Аминокислоты — органические соединения, в молекуле которых
одновременно содержатся карбоксильные и аминогруппы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминогруппы.

В процессе биосинтеза белка в полипептидную цепь включаются 20 α-аминокислот, кодируемых генетическим кодом –протеиногенные аминокислоты
