
- •Оглавление
- •Введенние
- •1 Способы получения металлорганических соединений
- •2 Органические производные металлов первой группы
- •2.1 Литийорганические соединения
- •2.2 Натрий- и калийорганические соединения
- •3 Органические производные металлов второй группы
- •3.1 Магнийорганические соединения
- •3.2 Цинкорганические соединения
- •3.3 Ртутьорганические соединения
- •4 Органические производные металлов третьей группы
- •4.1 Борорганические соединения
- •4.1.1 Способы получения борорганических соединений
- •4.1.2 Бороновые кислоты
- •4.2 Алюминийорганические соединения
- •5 Органические производные металлов четвёртой группы
- •5.1 Кремнийорганические соединения
- •5.1.1 Углерод и кремний. Физические и химические эффекты, связанные с заменой в органической молекуле углерода кремнием
- •5.1.2 Химические свойства связей атомов кремния и углерода с другими элементами
- •5.1.3 Способы получения органических производных кремния
- •5.1.4 Кремнийорганические полимеры
- •5.1.5 Биологическая активность кремнийорганических соединений
- •5.1.6 Метаболизм кремнийорганических соединений
- •5.2 Оловоорганические соединения
- •5.3 Органические производные свинца
- •6 Органические производные металлов пятой группы
- •6.1 Мышьякорганические соединения
- •Заключение
- •Литература
4.2 Алюминийорганические соединения
Первый способ получения алюминийорганических соединений был разработан в 1865 г. В его основе лежало взаимодействие ртутьорганических соединений с металлическим алюминием. Для получения больших количеств органических производных алюминия этот способ слишком затратен, но он позволяет получать их в чистом виде без растворителей.
Алюминийорганические соединения могут быть получены действием алкилгалогенидов на металлический алюминий:
![]()
Взаимодействием алюминия с метилиодидом в присутствии иода с хорошим выходом получают дииодид метилалюминия:
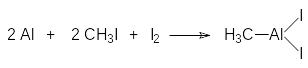
Соответствующие арильные производные можно получать по реакции арилгалогенидов с алюминием, который активирован размалыванием с хлоридом алюминия.
Хлориды алкильных производных алюминия стабильны, тогда как соответствующие бромиды и иодиды легко диспропорционируют. В соответствии с этим триметилалюминий можно получать по реакции металлического алюминия с метилиодидом при нагревании:
![]()
При взаимодействии с диазометаном органические галогениды алюминия превращаются в очень нестойкие хлорметильные производные.
Ещё один способ получения алюминийорганических соединений представлен реакцией алкилгалогенидов со сплавом алюминия с более электроположительным металлом, например, с магнием:
![]()
Алюминийорганические соединения получают также по реакции реактивов Гриньяра с хлоридом алюминия. Эти реакции проводят в среде абсолютного эфира, который образует очень стабильные комплексы с алюминийорганическими соединениями. Понятно, что при проведении реакции хлорида алюминия с алкил- и арилмагнийгалогенидами, синтезированными в углеводородах, можно получать несольватированные органические производные алюминия. Менее реакционноспособные металлорганические соединения кремния и свинца также реагируют с хлоридом алюминия с образованием алюминийорганических соединений.
Было известно, что гидрид алюминия реагирует с этиленом и его высшими гомологами с образованием триэтилалюминия и, соответственно, других триалкильных производных алюминия, в которых атом алюминия связан с первичным атомом углерода. Объединение стадии образования гидрида алюминия и его реакции с олефинами в один процесс, когда алюминий реагирует с водородом и с олефином, представило возможность получения алюминийорганических соединений в любом количестве. В эту реакцию вступают олефины общей формулы СН2=СRR′, но в отдельных случаях можно получать алюминийорганические соединения с вторичными алкильными радикалами, образующимися из олефинов с непредельной связью в середине цепи. Олефины с терминальной двойной связью (например, изобутен) непосредственно превращаются в триалкилалюминий при взаимодействии с активированным алюминием и водородом в присутствии полученного ранее триалкилалюминия. С другими олефинами (в том числе и с этиленом) течение реакции осложняется тем, что при температуре реакции, составляющей около 120 °С, первично образовавшийся продукт реакции реагирует далее, превращаясь в высшие алкильные производные алюминия. Для направленного получения триэтилалюминия реакцию разделяют на две стадии:
![]()
![]()
В общем случае первая стадия этого превращения протекает при температуре от 110 до 140 °С и давлении около 200 ат, тогда как для второй стадии достаточно температуры от 80 до 100 °С, а давление может составлять 10 ат. Понятно, что первая реакция представляет собой способ получения гидрида диалкилалюминия. Гидрид диалкилалюминия образуется также при нагревании триалкилалюминия с водородом при температуре 140-160 °С.
Легко получаемый по реакции изобутена с гидридом алюминия триизобутилалюминий может вступать в реакции обмена с другими олефинами по схеме:
![]()
В общем случае взаимодействие триизобутилалюминия с олефином проводят при нагревании в присутствии небольшого количества бензола, толуола или гептана для того, чтобы получить температуру реакции, определяемую температурой кипения растворителя. Мягкое течение реакции наблюдается при температуре выше 100 °С, правда, для олефинов с концевой непредельной связью RCH=CH2 температура при этом не должна превышать 110 °С, поскольку при более высоких температурах протекает каталитическая димеризация таких олефинов.
Как отмечалось выше, при превышении определённой температуры триалкильные производные алюминия реагируют с олефинами общей формулы RCH=CH2, в частности с этиленом, присоединяясь по двойной связи. Эта реакция приводит к получению высших алкильных производных алюминия. При этом триалкильные производные алюминия реагируют с этиленом при температуре 90–120 °С. Реакция протекает по схеме:
![]()
Этим способом, используя в качестве исходных соединений этилен, алюминий и водород, можно получать органические производные алюминия, которые можно превращать в алифатические соединения с чётным числом атомов углерода, например, первичные олефины, первичные спирты и алканы нормального строения. Для получения таких соединений с нечётным числом атомов углерода можно в качестве исходных продуктов использовать, например, этилен и трипропилалюминий. Условия протекания таких реакций с другими олефинами и триалкильными производными алюминия подбираются для каждого конкретного случая.
Триалкильные производные алюминия могут также присоединяться по тройной связи ацетиленов уже при температуре от 40 до 60 °С. Так, например, взаимодействие эквимолярных количеств ацетилена и триэтилалюминия приводит к образованию диэтилбутенилалюминия:
![]()
При этом, конечно, протекают и такие побочные реакции, как присоединение ацетилена по другим Al–C-связям, а также замещение подвижного атома водорода в ацетилене.
С молекулами, которые являются донорами электронов, органические производные алюминия образуют очень стабильные комплексы. Например, с такими простыми эфирами, как диэтиловый эфир и анизол, они образуют эфираты, некоторые из которых перегоняются без разложения даже при достаточно высоких температурах.
В роли доноров электронов могут выступать и карбанионы. Так, например, триметилалюминий и метиллитий реагируют с образованием тетраметилалюмината лития Li[Al(CH3)4]. Получен также тетрафенилалюминат лития Li[Al(C6H5)4]. Триалкильные производные алюминия образуют комплексные соли со многими галогенидами и цианидами щелочных металлов с координационно четырёхвалентным атомом алюминия состава M[A1R3X] или MX∙2A1R3 (где М означает атом щелочного металла и Х – галогенидный или цианидный анион), а из диалкилалюминийхлорида и хлорида калия образуются соли состава K[A1R2Cl2].
В результате взаимодействия соли Na[Al(C2H5)3Cl] с бензолом в присутствии алкоксида натрия образуется этан и тетрафенилалюминат натрия Na[Al(C6H5)4], из которого действием хлорида диметилалюминия можно получить трифенилалюминий:
![]()
Таким способом можно получать арильные производные алюминия из доступных этильных производных. Кроме того, получаемые по реакции гидридов алюминия с олефинами алюминийорганические соединения могут быть использованы для получения органических производных других металлов.
Алкильные производные алюминия широко используются для получения смесевых катализаторов полимеризации олефинов (в частности, этилена) при низком давлении. Эти катализаторы называют катализаторами Циглера–Натты по имени немецкого и итальянского исследователей (K. Ziegler, G. Natta), руководивших исследованиями в этой области. Классический катализатор Циглера–Натты основан на соединениях титана (например, тетрахлорида титана) и на алюминийорганических соединениях, в числе которых триэтилалюминий и триизобутилалюминий. При полимеризации пропилена и других α-олефинов в присутствии этих катализаторов получают отличающиеся более высокими прочностными характеристиками изотактические (стереорегулярные) полимеры.
