
- •Часть 3
- •Оглавление
- •Предисловие
- •После изучения дисциплины необходимо знать
- •После изучения дисциплины необходимо уметь
- •Содержание дисциплины
- •Самостоятельная работа и контроль знаний студентов
- •После изучения главы необходимо знать следующее:
- •1.1. Геометрическая оптика
- •1.2. Интерференция света
- •1.3. Дифракция света
- •1.4. Поляризация света
- •1.5. Дисперсия и поглощение света
- •После изучения главы необходимо знать следующее:
- •2.1. Тепловое излучение
- •2.2. Взаимодействие электромагнитного излучения с веществом
- •После изучения главы необходимо знать следующее:
- •3.1. Строение атомов
- •3.2. Спектр атома водорода
- •3.3. Волновые свойства частиц вещества
- •3.4. Элементы квантовой механики
- •3.5. Электронная оболочка атома
- •3.6. Атом водорода в квантовой механике
- •После изучения главы необходимо знать следующее:
- •4.1. Строение и свойства атомного ядра
- •4.2. Радиоактивность
- •4.3. Ядерные реакции
- •После изучения главы необходимо знать следующее:
- •5.1. Краткие исторические сведения
- •5.2. Классы элементарных частиц
- •5.3. Основные характеристики элементарных частиц
- •В опросы для самоконтроля По теме Волновая оптика
- •По теме Квантовая оптика
- •По теме Физика атома
- •По теме Физика атомного ядра
- •По теме Физика элементарных частиц
- •Т олковый словарь
- •З аключение
- •Библиографический список
- •Краткий курс физики
- •Часть 3
- •394026 Воронеж, Московский просп.,14
3.3. Волновые свойства частиц вещества
К пересмотру многих фундаментальных представлений и понятий физика подошла в результате открытия волновых свойств частиц вещества и соотношения неопределенностей.
Волны де Бройля. В 1924 г. Луи де Бройль впервые высказал гипотезу о том, что сочетание волновых и корпускулярных свойств является общим свойством любых материальных объектов, а не только света: движение реальной частицы соответствует распространению бесконечной волны в пространстве. Любое тело массой m, движущееся со скоростью v, может быть определено не только координатами в пространстве, импульсом р и энергией Е, но и длиной волны и частотой = с/ = /2. Де Бройль не пытался выяснить , какова природа волны, характеристики которой предсказал.
По предположению де Бройля, длина волны любого материального объекта связана с его импульсом таким же соотношением, каким связана длина волны фотона с его импульсом, то есть для частиц вещества c релятивистскими энергией Е и импульсом р:
Е
=
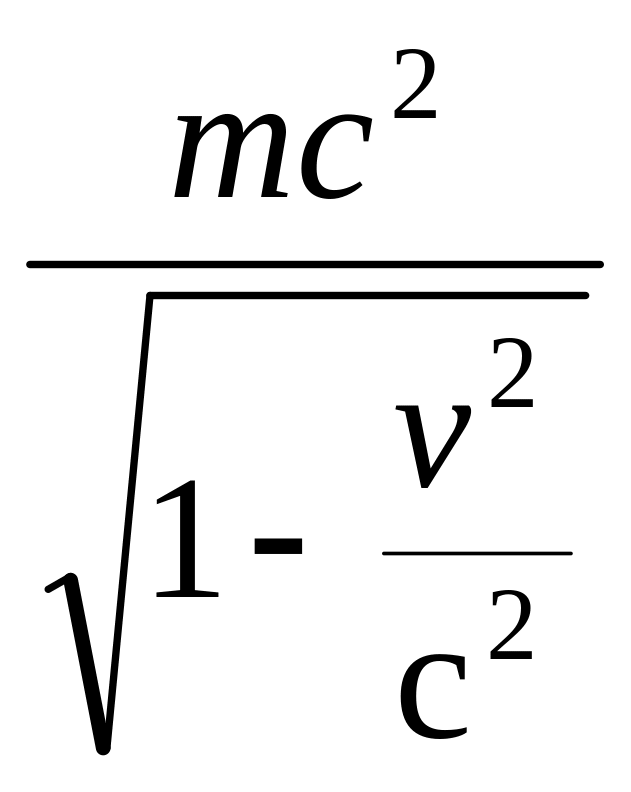 ,
р
=
,
р
=
 ,
,
то можно записать соотношения:
=
![]() ,
=
,
=
![]() = h
= h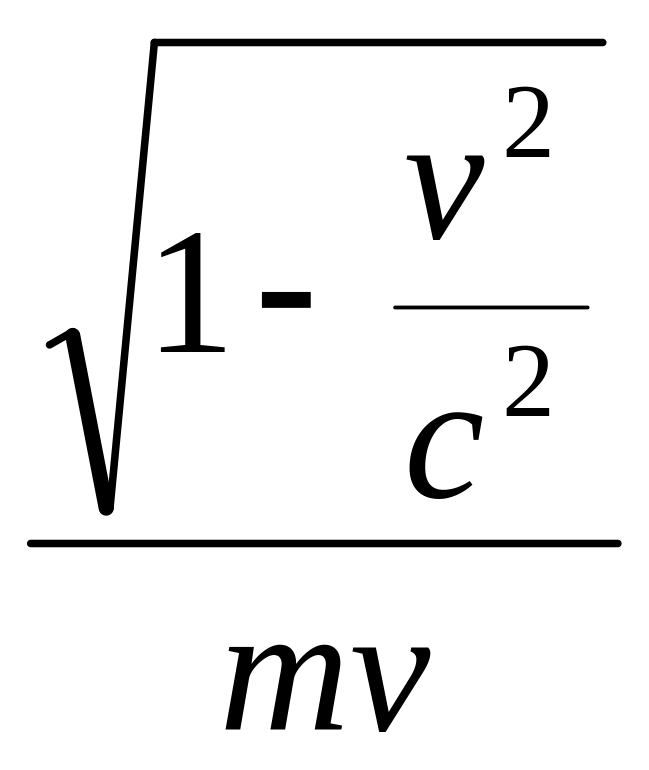 ,
p
= kћ
= k
,
,
p
= kћ
= k
,
где
k
=
=
![]() – волновое число. В нерелятивистском
приближении (v
c)
имеем:
– волновое число. В нерелятивистском
приближении (v
c)
имеем:
=
![]() .
.
Если вещество обладает волновыми свойствами, то для него должны наблюдаться явления дифракции (огибание волнами встречающихся на пути преград) и интерференции (сложения и вычитания волн).
Прямое экспериментальное доказательство того, что электроны могут дифрагировать и интерферировать, было получено в 1927 г. в опытах К. Дэвиссона и Л. Джемера, а также независимо П. С. Тарковским. Особенно впечатляющую картину дифракции наблюдал Дж. П. Томсон, сын Дж. Дж. Томсона, открывшего электрон. Он пропустил поток электронов сквозь тонкую золотую фольгу и получил классическую дифракционную картину, которую могли дать только волны. В настоящее время экспериментаторы наблюдают интерференцию и других частиц, вплоть до молекул. Так, в 2003 г. в Венском университете была впервые обнаружена квантовая интерференционная картина органических молекул биологического происхождения С44Н30N4, содержащих 78 атомов. В связи с этими экспериментами возникает вопрос: возможна ли квантовая интерференция живых существ?
Важным аргументом в пользу волн де Бройля было то обстоятельство, что с учетом определения волны частицы, например электрона, = h/p = h/(mеvn) правило квантования стационарных орбит электрона по Бору, которое записывается в виде mevnrn = nћ = nh/(2), принимает вид условия существования замкнутой стоячей волны: 2rn = n. Из полученного условия следует вывод: электрон, движущийся вокруг ядра, может иметь только такую траекторию, на которой укладывается целое число длин волн де Бройля (рис. 34).

Величина длины волны де Бройля зависит от массы и скорости движущегося объекта, поэтому в повседневной жизни практически невозможно измерить очень маленькие значения дебройлевских длин волн в опытах с макроскопическими телами. Например, дебройлевская длина волны тела массой 6,625 г, движущегося со скоростью 0,1 м/с:
=
![]() = 6,62510-34/(6,62510-30,
1) = 10-30
м,
= 6,62510-34/(6,62510-30,
1) = 10-30
м,
что в 1020 раз меньше размеров атомов.
Следует отметить, что условие целочисленности волн де Бройля на разрешенных орбитах электронов в атомах в определенной мере объясняет абсолютную идентичность атомов одного и того же элемента вне зависимости от условий их нахождения.
Дальнейшее развитие атомной физики привело к пониманию природы волн, описывающих движение атомных и субатомных частиц с вероятностной точки зрения. Возникла наука, получившая название «квантовая механика».
