
- •Введение
- •1. Спектральные и оптические методы анализа
- •1.1. Эмиссионный спектральный анализ. Фотометрия пламени
- •Контрольные вопросы
- •1.2. Молекулярно-абсорбционный анализ
- •Контрольные вопросы
- •1.3. Дифференциальная фотометрия
- •Контрольные вопросы
- •1.4. Фотометрическое титрование
- •Контрольные вопросы
- •1.5. Кинетический метод анализа
- •Контрольные вопросы
- •1.6. Фотометрия светорассеивающих систем
- •Контрольные вопросы
- •1.7. Люминесцентный анализ
- •Контрольные вопросы
- •1.8. Рефрактометрический метод анализа
- •Контрольные вопросы
- •1.9. Метрологические характеристики и статистическая обработка результатов анализа
- •2. Электрохимические методы анализа
- •2.1. Электрогравиметрия
- •Контрольные вопросы
- •2.2. Потенциометрия
- •Контрольные вопросы
- •2.3. Кондуктометрия
- •Контрольные вопросы
- •2.4. Полярографический анализ
- •Контрольные вопросы
- •2.5. Амперометрическое титрование
- •Контрольные вопросы
- •3. Хроматографические методы
- •3.1. Характеристика основных конструктивных узлов (блоков) хроматографа
- •3.2. Принцип работы газового хроматографа на примере chrom 5
- •3.3. Генератор водорода. Устройство и принцип работы
- •3.4. Методика выполнения работы Отбор пробы
- •Подготовка хроматографов к выполнению измерения
- •Выполнение измерений
- •Вычисление результатов анализа
- •3.5. Методы расчета хроматограмм
- •3.6. Методы расчета концентраций
- •Контрольные вопросы
- •4. Титриметрические методы анализа
- •Правила титрования
- •4.1. Кислотно-основное титрование в водном растворе
- •Контрольные вопросы
- •4.2. Осадительное титрование
- •Контрольные вопросы
- •4.3. Методы комплексообразования. Комплексонометрическое титрование
- •Контрольные вопросы
- •4.4. Окислительно-восстановительное титрование
- •Контрольные вопросы
- •Заключение
- •Библиографический список
- •Оглавление
- •394026 Воронеж, Московский просп., 14
Контрольные вопросы
1. Что является критерием чувствительности анализа?
2. Чувствительность, правильность и точность метода. Взаимосвязь между ними.
3. Сравните чувствительности прямой фотометрии, флуоресцентного и кинетического анализа.
4. Недостатки и преимущества фотоколориметров в сравнении со спектрофотометрами.
1.6. Фотометрия светорассеивающих систем
Ослабление светового потока при прохождении света через кювету с суспензией происходит вследствие его рассеяния и поглощения частицами дисперсной фазы и раствором:
I0 = In + Ip + I,
где I0, In, Ip, I, – интенсивности падающего, поглощаемого, рассеянного и прошедшего световых потоков соответственно.
Количественный анализ светорассеивающих систем осуществляют одним из двух методов – турбидиметрически и нефелометрически.
Метод нефелометрии основан на измерении величины Ip как функции концентрации. Зависимость Ip от влияющих факторов подчиняется закону Рэлея, который для данного прибора и конкретных условий фотометрирования можно представить в виде
Ip = I0 k C V,
где k – постоянная величина; С – концентрация ионов, дающих нерастворимую аналитическую форму; V – объем частиц осадка.
При турбидиметрических измерениях оценивают I в сравнении с I0, используя аналогичный оптической плотности параметр, называемый мутностью раствора:
S = lg I0/ I.
Прямая нефелометрия более чувствительный метод, чем прямая турбидиметрия. Однако количественный анализ по градуировочной зависимости характеризуется недостаточной воспроизводимостью и большой относительной ошибкой (10-15 %). Чаще используют титрование турбидиметрически и нефелометрически определяя точку эквивалентности.
Пример. Нефелометрическое титрование кальция оксалатом аммония.
При нефелометрическом титровании строят график зависимости “Ip – C”, на котором в точке эквивалентности наблюдается излом (рис. 6).
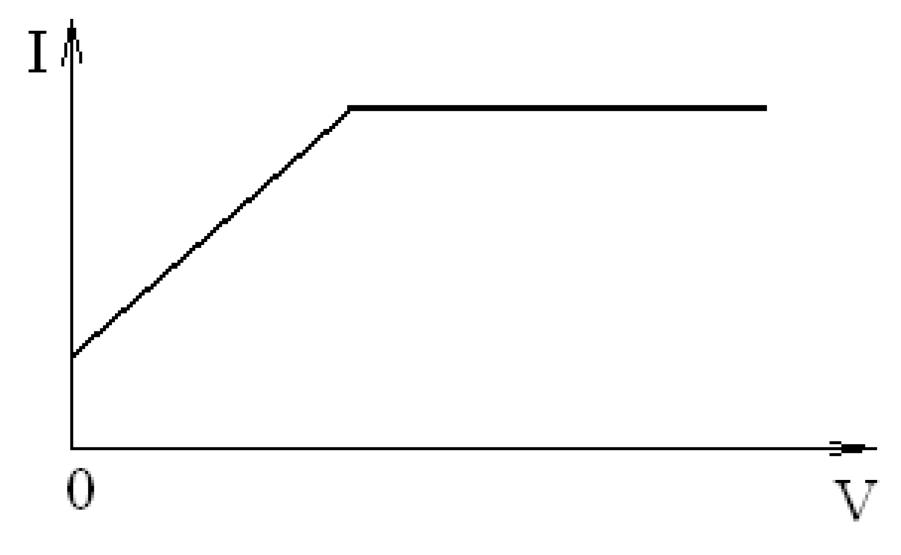
Рис. 6. Вид кривой нефелометрического титрования раствора соли кальция oкcалатoм аммония
Отбирают 5 мл стандартного раствора соли кальция и помещают в стакан на 100 мл. Приливают туда 30 мл ацетона и 40 мл дистиллированной воды. В стакан помещают магнитный элемент и устанавливают в гнездо прибора. Включают магнитную мешалку и перемешивают раствор до полного удаления пузырьков (около 10 мин). Воронка на поверхности раствора не должна попадать в световой поток.
Затем из бюретки в стакан приливают отдельными порциями по 1,0 мл титрованный раствор оксалата аммония. После прибавления каждой новой порции осадителя выжидают несколько минут, пока стрелка прибора не остановится. Записывают показания миллиамперметра и отсчеты по бюретке.
Если стрелка прибора при добавлении 3-4 порций оксалата (по 1,0 мл) не изменяет положения, титрование закончено.
Результаты заносят в таблицу и наносят на миллиметровую бумагу, откладывая по оси ординат Показания миллиамперметра, а по оси абсцисс – объем прибавленного осадителя. Массу Са находят, исходя из закона эквивалентов:
![]()
где Сн – эквивалентная концентрация кальция, моль/дм3; V – объём раствора, дм3.
Определив Сн(Са2+), рассчитывают массу кальция в пробе. Поскольку в данном случае известно количество взятого стандартного раствора, можно оценить погрешность метода.
Аналогично титруют и проводят расчеты для раствора, содержащего задачу (полностью соблюдать последовательность всех стадий).
