
Лекция №24 галогенпроизводные углеводородов.
План.
Классификация и номенклатура.
Методы получения.
Физические свойства и строение.
Химические свойства.
Галогенпроизводные углеводородов можно рассматривать как результат замещения однако или более атомов водорода в углеводороде на атомы галогенов. В зависимости от характера связи С-Hal различают следующие типы галогенуглеводородов:
1 .
Галогенпроизводные со связью С(sp3)-Hal
.
Галогенпроизводные со связью С(sp3)-Hal
где R, R1, R11 - атом водорода или алкильной радикал.
2. Галогенпроизводные со связью С(sp2)-Hal

3. Галогенпроизводные со связью С(sp)-Hal
R-CC-Hal
Галогенпроизводные типа с(sp3)-Hal Классификация и номенклатура
К галогенпроизводным углеводородов со связью С(sp3)-Hal относятся:
а) галогеналканы СnH2n+1 Hal, СnH2n+2–x Halx,
где х=0 ....... 2n+2
б) галогенциклоалканы СnH2n-1 Hal, СnH2n–х Halх,
где х=0 ...... 2n
в) галогеналкены с атомом галогена в алкильном заместителе при двойной связи
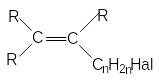
г) галогеналкины с атомом галогена в алкильном заместителе при тройной связи
R-CC-СnH2n- Hal
д) галогенарены с атомом галогена в боковой алкильной цепи
ArCnH2n – Hal, ArCnH2n+1–xHalх,
где х=0 ...... 2n+1
В основе названия галогенуглеводорода по номенклатуре IUPAC лежит название самой длинной неразветвленной цепи. Атомы углерода нумеруют таким образом, чтобы меньший номер получил заместитель, который в названии пишется первым, а сами заместители перечисляются в алфавитном порядке. Цепи углеродных атомов в галогенпроизводных алкенов и алкинов нумеруют с того конца, к которому ближе расположена кратная связь

Для некоторых простейших галогенпроизводных углеводородов сохраняются названия, в основе которых лежит название углеводородного остатка
СH3Cl – метилхлорид,
СH3J – метилиодид,
С2Н5Вr – этилбромид,
С6H5CHCl2 – бензилиденхлорид
СH2Cl2 – метиленхлорид,
С6H5CH2Cl – бензилхлорид,
Для некоторых галогенпроизводных сохраняются тривиальные названия:
СHCl3 – хлороформ,
СHBr3 –бромоформ,
CHJ3 – иодоформ
Для названия полностью галогенированных углеводородов используется префикс пер–:
С2F6 – перфторэтан
C3Cl8 – перхлорпропан
Для соединения СCl4 применяется название тетрахлорид углерода и четыреххлористый углерод.
Методы получения
1. Заместительное галогенирование.
Объектом заместительного галогенирования могут быть алканы. В общем виде реакции заместительного галогенирования алканов выражаются уравнением:
RH + Hal2 RHal + HНal
Таким способом можно получить фтор-, бром- и хлоралканы. Подробно об особенностях этих реакций – см. химические свойства алканов.
Аллильное хлорирование алканов можно осуществить при высоких температурах (400-500оС) в паровой фазе
t
СН2 = СН – СH3 + Cl2 CH2 = CH – CH2Cl + HCl
Д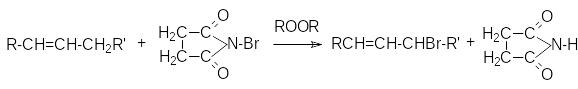 ля
аллильного бромирования алканов в
качестве реагента используют
бромсукцинимид
ля
аллильного бромирования алканов в
качестве реагента используют
бромсукцинимид
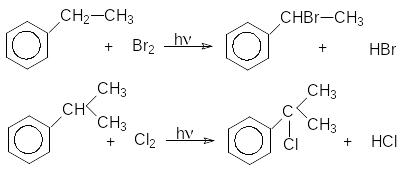
Хлорирование и бромирование боковых цепей алкиларенов можно осуществлять в условиях инициирования свободнорадикальных реакций (химические инициаторы, фотоинициирование), причем наиболее реакционноспособным оказывается -положения боковой цепи:
2. Присоединительное галогенирование алкенов и алкинов.
В озможности
этого метода можно проиллюстрировать
следующими реакциями:
озможности
этого метода можно проиллюстрировать
следующими реакциями:
Особенности приведенных реакций подробно обсуждались в разделах, посвященных химическим свойствам алкенов и алкинов. Здесь лишь отметим, что при реализации этих реакций в промышленности с целью форсирования процессов используют катализаторы типа кислот Льюиса (FeCl3, SnCl4, SbCl3 и др.)
3. Реакции замещения гидроксильных групп на галоген в спиртах.
К таким реакциям относятся:
а) взаимодействие галогеноводородов со спиртами
ZnCl2
ROH + HCl –––– RCl + H2O
Важным фактором эффективности этих реакций является высокая кислотность среды, обеспечивающая стабилизацию уходящей гидроксильной группы:
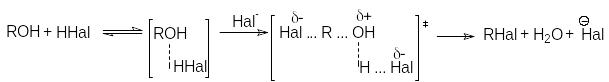
Каталитическое действие хлорида цинка связано с образованием более сильной протонной кислоты за счет донорно-акцепторного взаимодействия:
ZnCl2 + HCl H2[ZnCl4]
которая в последующем выполняет каталитическую функцию. В связи с важностью поддержания кислотности среды в этих реакциях в качестве гидрогалогенирующих реагентов можно использовать комбинации соль-кислота, например, KBr + H2SO4.
Иногда в качестве реагентов используют смеси, продуцирующие in situ необходимый галогеноводород:
2P + 3J2 + 6H2O 6HJ + 2H3PO3
б) Взаимодействие галогенангидридов кислот (PСl3, PВr3, PСl5, SOCl2, PJ3 и др.) со спиртами:
PCl3 + 3ROH 3rcl + H3PO3
PCl5 + 5ROH 5rcl + H3PO4 + H2O
SOCl2 + ROH RCl + SO2 + HCl
SF4 + 2KOH 2RF + SO2 + 2HF
в) Взаимодействие галогенангидридов кислот (PСl5, PBr5, SF4) c альдегидами и кетонами

где R’=H, R, Ar.
4. Замещение галогена на галоген.
Замещение более легкого галогена в галогенуглеводороде более тяжелым
RCl + KBr RВr + KCl
обеспечивается проведением реакции при умеренных температурах и избытке галогенирующего реагента в неполярных апротонных растворителях.
Замещение более тяжелого галогена более легким
RJ + KCl RCl + KJ
обеспечивается проведением реакции при повышенных температурах и избытке галогенирующего реагента в высокополярной среде в присутствии катализатров - кислот Люиса, например, Сu+, Ag+ и пр.
