
- •Коринебактерии Род Corynebacterium
- •Сибирская язва
- •Патогенные анаэробные спорообразующие бактерии-клостридии
- •Газовая гангрена
- •Столбняк
- •Ботулизм
- •Микробиология чумы
- •Микобактерии туберкулеза
- •Боррелии
- •Болезнь лайма
- •Лептоспироз
- •Патогенные грибы и актиномицеты
- •Микоплазмы. Хламидии.
- •Санитарная микробиология.
ЛЕКЦИЯ 1
ООИ-ОСОБО ОПАСНЫЕ ИНФЕКЦИИ. БРУЦЕЛЛЁЗ. ТУЛЯРЕМИЯ.
БРУЦЕЛЛЁЗ.
Возбудитель Бруцеллеза- впервые в 1886 году обнаружили английский ученый Дэвид Брюс. В честь его их и назвали бруцеллами, а вызываемое ими заболевание- бруцеллёзом.
Семейство: Brucellaceae
Род: Brucella
Вид: B. melitensis
B. abortus.
B. suits.
B. ovis.
B. canis
B. neotomae
Морфология и культуральные свойства.
Род объединяет грам(-) мелкие неподвижные палочки или коккобациллы, обладающие значительным полиморфизмом: в одном препарате наблюдают кокки и удлиненные палочки. Клетки B.melitensis чаще представлены кокковидными формами, B. Abortus и B. Suis- палочками с закругленными концами. В мазсках располагаются беспорядочно, не имеют жгутиков, не образуют спор и капсул. Легко окрашиваются анилиновыми красителями.
Хемоорганотрофы. Каталаза- и оксидаза- положительны.
Строгие аэробы, некоторые штаммы нуждаются в повышенной концентрации СО2.
Оптимум температуры +37, рН-6,6-7,4.
Грамм(-) мелкие неподвижные палочки или коккобациллы.
Бруцеллы требовательны к питательным средам.
Растут на обогащенных средах с добавлением крови или сыворотки крови, глюкоз, глицерина. Элективной средой для их культивирования является печеночный агар или печеночный бульон (например, печеночный агар Хеддльсона).
Культуральные свойства бруцелл.
Легко диссоциируют, переходя из S- в R-форму. Колонии в S-форме мелкие, выпуклые, гладкие, бесцветные, с перламутровым оттенком, при диссоциации образуют шероховатые R-формы колоний.
На жидких средах- равномерное помутнение.
При выделении из патологического материала в первых генерациях растут медленно, в течение 1-3 недель.
Биохимические свойства.
Биохимически бруцеллы малоактивны. Ферментируют глюкозу м арабинозу с образованием кислоты.
Восстанавливают нитраты.
Индол не образуют.
Образуют сереводород.
Антигенная структура рода Brucella.
Выделяют:
Родовой АГ
Видовые поверхностные
* М-(преобладает у B.melitensis).
*А- (преобладает у B.abortus и B.suis).
* R-антиген содержат шероховатые формы.
*L -антиген- поверхностный термолабильный (сходен с VI–антигенами сальмонелл).
Резистентность представителей рода Brucella
Бруцеллы обладают относительно высокой устойчивостью во внешней среде: в почве- до 100 и более дней, в пыли-до 44 дней, в воде- 6-150 дней, в засоленном мясе-80-100 дней. При низкой температуре воздуха бруцеллы не теряют жизнеспособности до 160 дней и более. В молоке до 273 дней, в сыре до 1 года.
Однако они чувствительны к высокой температуре- погибают при 70 градусах Цельсия через 10 мин, при кипячении- за несколько секунд.
Чувствительны к химическим дезинфектантам.
Факторы патогенности.
Экзотоксина нет, патогенность обусловлена эндотоксином.
Ферменты патогенности- гиалуронидаза, каталаза, уреаза.
Способны подавлять фагоцитоз, предотвращать «окислительный взрыв».
Обладают сильнейшим аллергенным свойством, определяющим патогенез и клинику.
Особенности эпидемиологии.
Бруцеллёз- это зоонозная инфекция, передающаяся от больных животных человеку, характеризующаяся множественным поражением органов и систем организма человека.
Основными носителями бруцелл являются овцы, козы (В.melitensis ), крупный рогатый скот (В. abortus), свиньи (В.suis) и северные олени (В.rangiferis ). Однако они могут переходить и на многие другие виды животных (яки, верблюды, буйволы, волки, лисицы, грызуны, ламы, сайгаки, бизоны, лошади, зайцы, ежи, куры и др.). Особенно большую эпидемиологическую опасность представляет переход Вrucella melitensis на крупный рогатый скот, так как в этом случае она сохраняет свою высокую патогенность для человека.
Из всех видов наиболее патогенным для человека в нашей стране является B.melitensis. Он служит причиной заболевания людей более чем в 95-97% всех случает бруцеллеза. B.abortus, как правило вызывает латентную форму болезни,и только в 1-3% отмечаются клинические проявления. Ещё реже заболевание вызывает B.suis(<1%). Патогенность бруцелл варьирует в зависимости не только от вида,но и от биовара. В частности, биовары 3,6,7,9 B.abortus по вирулентности не уступают B.melitensis.
Патогенез и клиника.
Ворота- микротравмы кожи и слизистой оболочки органов пищеварения и респираторного тракта. На месте ворот и в лимфатических путях региональных лимфоузлов изменений нет. Лимфаденопатия при бруцеллезе является генерализованной, что свидетельствует о гематогенной диссеминации микробов. Размножение и накопление в лимфоузлах- периодически в крови. Выраженная аллергическая перестройка организма, резко выраженная гиперчувствительность замедленного типа сохраняется длительное время после очищения организма от возбудителя.
Наиболее благоприятную среду для размножения бруцеллы находят в беременной матке, что приводит к эндометриту, нарушению питания плода и аборту.
Бруцеллы относятся к внутриклеточным паразитам. После проникновения в организм человека они фагоцитируются лейкоцитами и макрофагами, распространяясь в ретикулоэндотелиальной ткани. Возбудители могут размножаться в разных клетках, в том числе в эритроцитах. Заражение бруцеллезом сопровождается развитием гиперчувствительности замедленного типа к бруцеллезному антигену.
Организм больного реагирует на бруцеллезную инфекцию выработкой антител, среди которых выделяют агглютины, бактериолизины, опсонины, преципитины и комплемент связывающие антитела.
Инкубационный период составляет 1-2 недели. Заболевание развивается, как правило, постепенно и не имеет специфических черт. Но больные обычно предъявляют четыре основные жалобы: перемежающаяся боль в суставах, преимущественно в нижних конечностях, иногда весьма сильная и мучительная. Повышение температуры тела в виде длительного субфебрилитете (до 38*) или волнообразного типа с резкими подъемами или падениями. Усиленная потливость. Резкая слабость или упадок сил.
Системные поражения многообразны и затрагивают практически все органы. Плоражаются:
Опорно-длительный аппарат (септический моноартрит, асимметричный полиартрит коленного, тазобедренного, плечевого, сакроилиального и грудиноключичного соединений, остеомиелит позвоночника, миалгия).
Сердце (эндокардит, миокардит, перикардит).
Дыхательная система (бронхит и пневмония).
Пищеварительная система (безжелтучный гепатит, анорексия и потеря веса).
Мочеполовая система.
Центральная нервная система.
Лимфатические узлы, селезенка, глаза.
Бруцеллёз перехлодит в хроническую форму в 37-80% случаев, особенно при несвоевременном или неадекватном лечении.
Бруцеллёз редко становиться причиной смерти. Даже до появления антибиотиков смертность при нем не превышала 2% и была в основном обусловлена эндокардитом. Однако бпуцеллез нередко заканчивается инвалидностью. Тяжесть остаточных дефектов зависит от вида возбудителя. Самые тяжелые последствия оставляет бруцеллез, вызванный Brucella melitensis. Одна из причин инвалидности- неврологические расстройства, в том числе поражение спинного мозга и параплегия.
Схема лабораторной диагностики бруцеллеза.
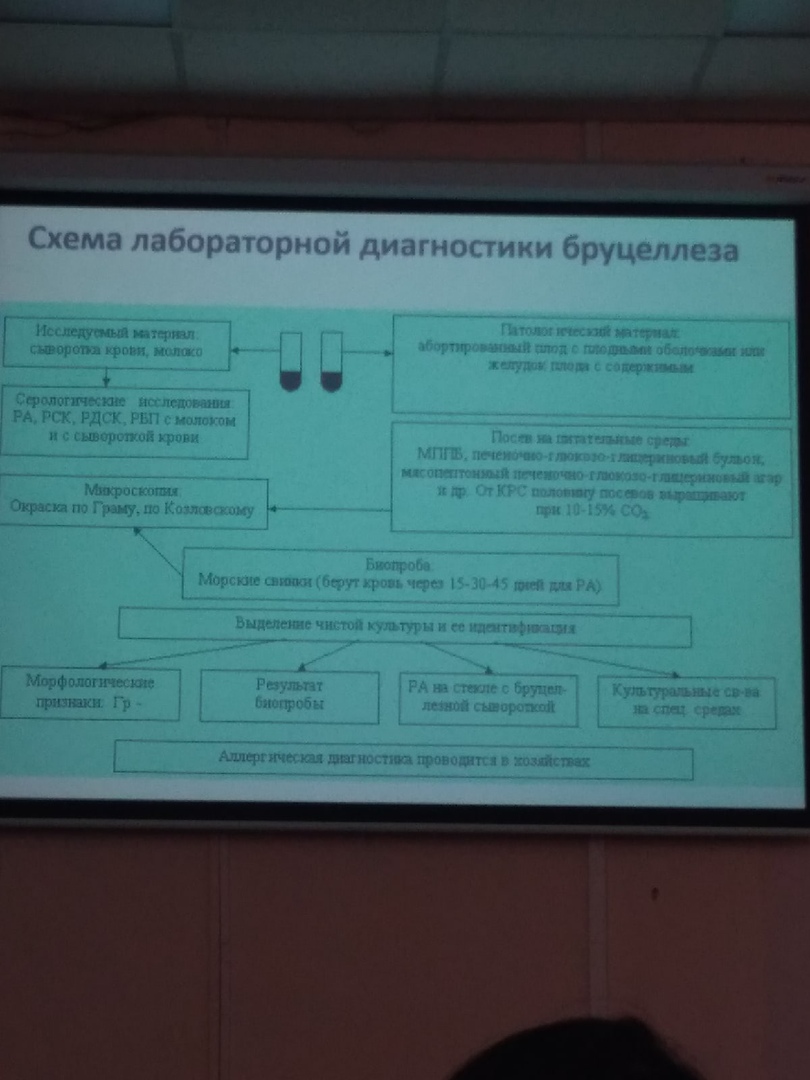
Посев крови на питательные среды положителен в 50-70% случаев у больных бруцеллезом.
Реакция Райта- положительна на 10-й день.
Реакция Кумбса- диагноз хронического бруцеллеза.
2-меркоптоэтанол-аглютинитовый тест.
Реакция Хеддлсона.
Кожная проба Бюрне.
Выявление ДНК Brucella spp. Методами амплификации нуклеиновых кислот (ПЦР).
Туляремия.
Семейство: Francisellaceae
Род: Francisella
Вид: Francisella tularensis.
Выделяют 3 подвида Francisella tularensis:
Н
 еарктический
(американский)- распространен только
в Северной Америке, высокопатогенен
для человеков и кроликов, ферментирует
глицерин, его выделяют от грызунов и
кровососущих насекомых.
еарктический
(американский)- распространен только
в Северной Америке, высокопатогенен
для человеков и кроликов, ферментирует
глицерин, его выделяют от грызунов и
кровососущих насекомых.Голарктический (европейско-азиатский)- регистрируется в Европе и Америке, умеренно патогенен для человека и кроликов, не ферментирует глицерин, выделяется из воды и ее обитателей. На территории России циркулирует подвид туляремийного микроба, относящийся к голарктическому типу.
Среднеазиатский- вызывает заболевание в средней Азии, ферментирует глицерин, умеренно патогенен для домашних кроликов и человека.
Грам (-) неподвижные, преимущественно кокковидные, палочки. Имеют очень мелкие размеры 0,3-0,5 мкм, способны проходить через некоторые бактериальные фильтры.
Морфология и культуральные свойства.
Это мелкая грамотрицательная полиморфная (преимущественно кокковидная) палочка, неподвижная, спор не образует. Некоторые штаммы имеют тонкую капсулу.
Относится к факультативным аэробам.
Чрезвычайно прихотлива к условиям культивирования, не растет на обычных питательных средах- мясо-пептонном агаре или бульоне. Оптимальными являются сложные агаровые или желточные слабощелочные среды с добавлением цистеина, кроличьей дефибринизированной крови, тканевых эстрактов и других стимуляторов роста.
Рост на кровяном агаре, агаре Мак Конки, шоколадном агаре.
Колонии среднего размера 2-4 мм светлые с опалесцирующим блеском.
Антигенная структура.
Francisella tularensis содержит соматический (О) и облочечный (Vi) антиген, обладает антигенным сродством с бруцеллами и возбудителем чумы, что объясняет перекрестные серологические реакции и должно учитываться клиницистами при интерпретиции результатов иммунологических исследований.
Факторы патогенности.
Основным фактором патогенности является эндотоксин, аналогичный таковому других грамотрицательных бактерий.
Вирулентные свойства обусловлены также Vi-антигеном.
Эпидемиология заболевания.
Источником являются грызуны, чаше водяная полевка, ондатра, домовая мышь, зайцы.
Пути передачи: трансмиссивный (основной путь передачи) через укусы насекомых, клещей, комаров, реже блох; контактно-бытовой-через поврежденную кожу или слизистую оболочку глаз; пищевой- при употреблении зараженной воды или пищевых продуктов; воздушно-пылевой- при вдыхании с воздухом пыли или капелек, загрязненных выделениями грызунов.
Заболевание от человека к человеку не передается. Чаще болеют сельские жители и люди определенных профессий, постоянно контактирующие с зараженными животными.
Туляремия-зооантропонозная инфекция.
Патогенез и клиника.
Входные ворота: поврежденная кожа и слизистые оболочки дыхательных путей и пищеварительного тракта. Попав в организм, возбудитель по лимфатическим сосудам распространяется по организму. Токсины возбудителя поражают лимфоузлы, в результате чего происходит образование бубонов. Инкубационный период составляет 3-7 дней. В результате воспаления лимфоузлов, они увеличиваются в размерах (от лесного ореха до куриного яйца). Бубоны часто нагнаиваются и долго на заживают. При генерализованной форме, когда возбудитель проникаетв кровь, наблюдается высокая температура (38-40°C), озноб, мышечные боли в области спины, ног, поражение селезенки, печени, дыхательных путей, пищеварительного тракта. По тяжести различают легкую, средней тяжести и тяжелую формы туляремии, по длительности острую и затяжную формы.
В среднем заболевание длится 16-30 дней и, как правило, заканчивается выздоровлением, При заболевании развивается аллергизация к антигенам возбудителя.
В зависимости от пути проникновения различают клинические формы туляремии:
Глазо-бубонная.
Бубонная.
Легочная.
Язвено-бубонная.
Абдоминальная.
Генерализованная.
Лабораторная диагностика.
Проводится в изолированных лабораториях 3-4 уровня (лаборатория особоопасных инфекций).
Исследуемый материал: смывы, кровь, содержимое бубонов. Методы диагностики: бактриологический, кожно-аллергическая проба с тулярином; серологический методс туляремийным диагностикумом,
Бактериологический выделение чистой культуры. Исследуемым материалом заражают внутрибрюшинно морских свинок (непосредственно от больного выделить чистую культуру не удается), которые погибают через 5-7 дней, их вскрывают, делают из органов мазки-отпечатки (бактериоскопический метод), а материал засевают на свернутую желточную среду;
Биопроба-заражение патологическим материалом белых мышей или морских свинок; морские свинки погибают на 4-6-ой день. Для обнаружения возбудителя у павших животных (в трупном материале) применяют микроскопию мазков-отпечатков из органов, выделение чистой культуры, биопробу, а также реакцию термокольцепреципитации с предварительно прокипяченной взвесью из печени или селезенки животных.
Профилактика.
Специфическая профилактика (вакцинация) проводится живой туляремийной вакциной. Контингенты, подлежащие вакцинации, определяются центрами Роспотребнадзора.
Всплеск заболеваемости людей туляремией в 2005 году связан с прекращением массовой вакцинации населения на территории природных очагов, необычайно большой численностью грызунов кровососущих насекомых.
Противопоказания к ведению вакцины.
Вакцину от туляремии нельзя вводить детям до 7 лет; женщинам в период беременности или лактации; при наличии любых острых заболеваний; при бронхиальной астме, склонности к тяжелым аллергическим pеакциям; онкологических заболеваниях, любых формах иммунодефицита.
ЛЕКЦИЯ 2
АЭРОБНЫЕ ГРАМ-ОТРИЦАТЕЛЬНЫЕ КОККИ
Семейство Neisseriaceae
род Neisseria
род Acinetobacter
род Moraxella
род Kingella
Общие признаки бактерий этой группы:
способны расти в присутствии кислорода,
представлены неподвижными диплококками и короткими палочками, отрицательно окрашивающимися по Граму,
спор не образуют.
Род Neisseria
Среди Грам- кокков наибольшее клиничесокое значение имеет род Neisseria
Род назван в честь немецкого дерматовенеролога Альберта Нейссера, открывшего возбудителя гонореи.
Род Neisseria образуют неподвижные аэробные или факультативно анаэробные споронеобразующие грамотрицательные диплококки, напоминающие кофейные зерна или бобы, прилегающие друг к другу уплощенными сторонами.
Для патогенных нейссерий характерно наличие капсулы, а также пилей и ворсинок, облегчающих адгезию к эпителию.
Свойства представителей рода Neisseria:
Грам (–) диплококки
Неподвижны
Аэробы или факультативные анаэробы
Споры не образуют
Некоторые имеют капсулу
Каталаза-отрицательные
Оксидаза-положительны
Некоторые виды синтезируют жёлтые каротиноидные пигменты
Большинство нейссерий неприхотливы, но патогенные виды для культивирования требуют среды с кровью или сывороткой. Оптимальная температура 35-37°С, рН- 7,2-7,4.
Представители нормальной микробиоты слизистой носоглотки и ВДП :
N.flava
N.subflava
N.mucosa
N.flava
N.subflava
N.mucosa
Патогенные виды рода Neisseria
N. meningitidis (менингококк)
N. gonorrhoeae (гонококк)
N. meningitidis
Возбудитель Neisseria meningitidis (менингококк) — открыл австрийский бактериолог А. Вексельбаум в 1887 г.
Патогенез и клиника менингококковой инфекции
Клинические формы инфекции можно разделить на:
локализованные
назофарингит
генерализованные
сепсис (менингококцемия),
менингит, менингоэнцефалит.
Носоглотка (бактерионосительство) →Инфекция верхних дыхательных путей (назофарингит) → Кровь (сепсис, септицемия) → Мягкие мозговые оболочки, мозг (менингит, менингоэнцефалит)
Форма инфекции обусловлена степенью вирулентности патогена и состоянием иммунитета зараженного. Чаще заболевание вызывают менингококки серологических групп А, В и С, а генерализованные формы – группы А.
Важна роль эндотоксина в развитии токсического шока, развивающегося иногда у больных менингококцемией и менингитом. Болезнь в таких случаях протекает молниеносно и часто заканчивается летальным исходом.
Наиболее тяжелая форма инфекции – цереброспинальный менингит, развивающийся после преодоления менингококком гематоэнцефалитического барьера.
При менигококковой септицемии имеет место васкулит и артрит за счет образование иммунных комплексов (аллергия 3 типа).ФАКТОРЫ ПАТОГЕННОСТИ N. meningitidis
Пили (адгезия и колонизация клеток эпителия носоглотки, оболочки мозга)
Белки наружной мембраны
Капсула (антифагоцитарная активность. AT, синтезируемые к полисахаридам капсулы, проявляют бактерицидные свойства).
Менингококки не продуцируют экзотоксинов.
Эндотоксин (липополисахарид клеточной стенки) опосредует большинство клинических проявлений, пирогенен, вызывает некроз, токсический шок
гиалуронидаза, нейроминидаза,
плазмокоагулаза, фибринолизин (способствуют распространению, повреждают ткани хозяина)
IgA-протеазы ответственный за расщепление секреторного IgA
Иммунитет
У 10 — 15 % заразившихся развивается картина острого назофарингита
У 1% - генерализованная форма инфекции
85 — 90 % заразившихся могут быть здоровыми носителями.
Приобретённый иммунитет чаще гумморальный, чем клеточный.
Эпидемиология.
Источник инфекции — человек (больной или бактерионоситель). Широкое здоровое носительство поддерживает циркуляцию возбудителя и создаёт опасность вспышек.
Путь передачи — воздушно-капельный, чаще реализуется при тесном контакте, т. к. возбудитель крайне неустойчив во внешней среде.
Чаще болеют дети, вспышки происходят в организованных коллективах.
Антигенная структура N. meningitidis
Представлена белковыми и полисахаридными антигенами разной специфичности и локализации:
Капсульные полисахаридные антигены делят на группы (более 13).
Наибольшее значение в патологии имеют полисахариды групп – А, В, С, Х, Y и W-135
Лабораторная диагностика
Лабораторная диагностика менингококковых заболеваний основана на бактериоскопии выделеной культуры и биохимической идентификации Neisseria meningitidis. Материал для исследования – спинномозговая жидкость (СМЖ), кровь и отделяемое носоглотки, взятое тампоном из глубоких отделов позади мягкого нёба. Забор материала желательно проводить до начала антибактериальной терапии.
В окрашенных мазках крови или отделяемого из носоглотки обнаруживают грамотрицательные одиночные кокки или диплококки, что значительно облегчает распознавание N. meningitidis при характерной клинической картине. Следует помнить, что обнаружение N. meningitidis в мазках СМЖ затруднено, и в этих случаях диагноз менингококкового менингита подтверждают обнаружением АГ N. meningitidis в реакциях латекс-агглютинации или встречного иммуноэлектрофореза. В период менингококцемии грамотрицательные диплококки могут быть обнаружены в окрашенных мазках в лейкоцитах периферической крови.
Посев материала для получения культуры производят на плотные или полужидкие питательные среды, содержащие сыворотку, кровь или асцитическую жидкость. Культуры инкубируют в течение 18-24 ч. при 37°С в сосуде со свечой или специальном термостате с повышенным содержанием (8-10%) СО2.
Оксидаза-положительные колонии предположительно рассматривают как принадлежащие к видам Neisseria.
Наличие в культуре N. meningitidis подтверждают образованием уксусной кислоты при ферментации глюкозы и мальтозы (но не лактозы, сахарозы и фруктозы).
Принадлежность к серогруппам определяют серологически (РА).
N. gonorrhoeae
впервые обнаружен Нейссером в 1879 г.
Нетривиальное название гонококк — возбудитель гонореи, инфекционного венерического заболевания, проявляющегося воспалением слизистых преимущественно мочеполовых путей.
АНТИГЕНЫ N.gonorrhoeae
По химической природе: белковые (клеточная стенка) и полисахаридные (капсула)
По специфичности:
Родоспецифические (общие с другими нейссериями и, особенно, с менингококком)
Видо- и вариантоспецифические: 3 белковых антигена клеточной стенки – I, II, III, играю-щие важную роль в патогенезе инфекции.
Антигенная вариабельность: по белку I более 50 вариантов, 16 антигенных вариантов пилей.
ФАКТОРЫ ПАТОГЕННОСТИ:
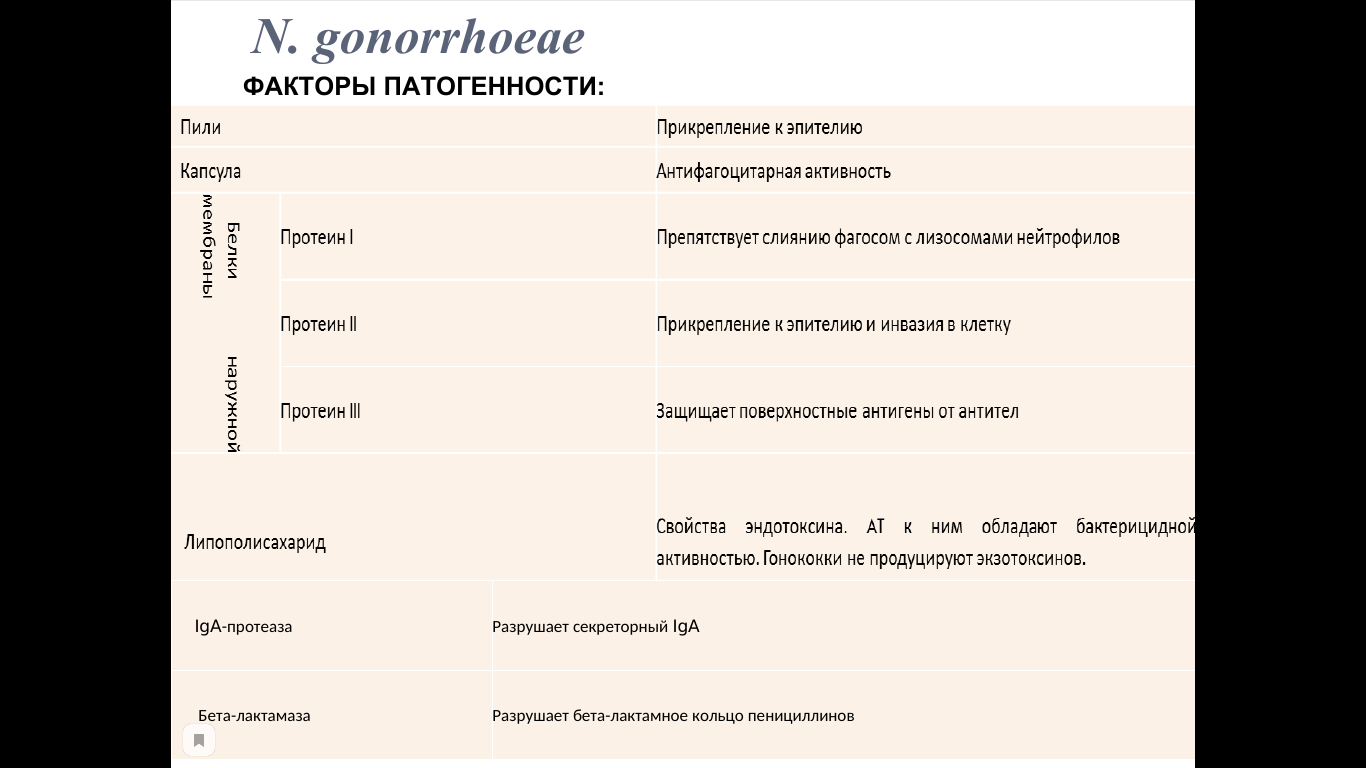
ФОРМЫ ИНФЕКЦИИ И ПАТОГЕНЕЗ
Основная форма: гонорея (от гр. honor - семя, rhoeae - истечение) — венерическая инфекция, характеризующаяся гнойным воспалением слизистых оболочек мочеполовой системы. У мужчин - уретра, у женщин – влагалище, уретра, шейка матки.
На слизистой бактерии фиксируются за счет пилей и протеина II. В дальнейшем проникают в клетки эпителия путем эндоцитоза и выходят путем экзоцитоза уже в подэпителиальную соединительную ткань, вызывая воспалительную реакцию с выделением содержащего гонококки гнойного экссудата.
Патогенез гонореи.
Инкубационный период от 1 до 14 дней, в среднем 2-5 дней. Гонококки с помощью ворсинок и некоторых поверхностных белков (Opa) прикрепляются к эпителиальным клеткам и проникают в них путем пиноцитоза, а через межклеточные щели достигают субэпителиального пространства.
Инвазия гонококков и разрушение клеток эпителия под действием эндотоксина сопровождается сильно выраженной воспалительной реакцией, образованием микроабсцессов и эксудацией гнойного материала в полость органа.
Большая часть гонококков разрушается в процессе фагоцитоза, часть гонококков не переваривается фагоцитами.
Гонококки проникают в кровяное русло, но не погибают под действием бактерицидных факторов сыворотки крови. Происходит диссеминация возбудителя и генерализация инфекции.
Свойство гонококков противостоять защитным силам организма приводит к сохранению инфекции. Этому способствует и их антигенная изменчивость и приобретение устойчивости к антибиотикам.
N. gonorrhoeae преимущественно поражают слизистые оболочки, покрытые цилиндрическим эпителием (мочеполовые органы, конъюнктива и др.).
Наиболее частым проявлением диссеминированной гонококковой инфекции (ДГИ) являются поражения суставов, одного или нескольких, и кожи.
При гонококковой септицемии имеет место васкулит и артрит за счет образование иммунных комплексов (аллергия 3 типа).
Иммунитет
Естественная восприимчивость высокая, особенно у лиц с дефицитом комплемента.
Постинфекционный иммунитет имеет преимущественно гуморальный механизм, однако прямой корреляции между уровнем антител и степенью защиты нет.
Местный гуморальный иммунитет поддерживается за счет IgА (в секрете предстательной железы, семенной жидкости, цервикальном отделяемом).
Иммунитет носит типоспецифический характер. Возможны реинфекция и даже суперинфекция.
Клеточный иммунный ответ характеризуется сенсибилизацией к антигенам и нарастает с увеличением продолжительности течения инфекции.
Эпидемиология.
N.gonorrhoeae вызывает заболевания только у людей.
Источник возбудителя: человек больной острой или хронической формой гонореи.
Механизм передачи возбудителя контактный.
Путь передачи - половой, редко – бытовой (белье, полотенце, мочалка).
Гонорея новорожденных (бленнорея) - поражение слизистой оболочки глаз. Новорожденные инфицируются при прохождении через половые пути больной матери.
Болезнь встречается повсеместно. Ее распространению способствуют случайные половые связи и проституция. Болеют лица обоего пола. Сезонность отсутствует.
ЛЕЧЕНИЕ ГОНОКОККОВОЙ ИНФЕКЦИИ
Лечение антибиотиками.
Следует учитывать возможность распространения гонококков, устойчивых к пенициллину, тетрациклину и фторхинолонам.
ПРОФИЛАКТИКА ГОНОРРЕИ
Специфической профилактики нет.
Для иммунотерапии используется вакцина – взвесь инактивированных фенолом гонококков.
Для профилактики гонорейного конъюнктивита всем новорожденным сразу после рождения закапывают в глаза 1% нитрат серебра.
ЛЕКЦИЯ 3
Коринебактерии Род Corynebacterium
Классификация
• Тип: Актинобактерии (Actinobacteria)
• Класс: Актинобактерии
• Порядок: Актиномицеты
• Семейство: Corynebacteriaceae
• Род: Corynebacterium
• Типовой вид: Corynebacterium diphtheriae (возбудитель дифтерии).
Представители рода Corynebacterium (Дифтероиды) широко распространены на растениях, в почве, воздухе, пищевых продуктах (молоке). Среди них можно выделить три экологические группы:
- патогены человека и животных;
- патогены растений;
- непатогенные коринебактерии.
Возбудитель дифтерии был открыт в 1883—1884 гг. Т. Клебсом и Ф. Леффлером. Нетривиальное название – дифтерийная палочка (палочка Клебса-Лёффлера).
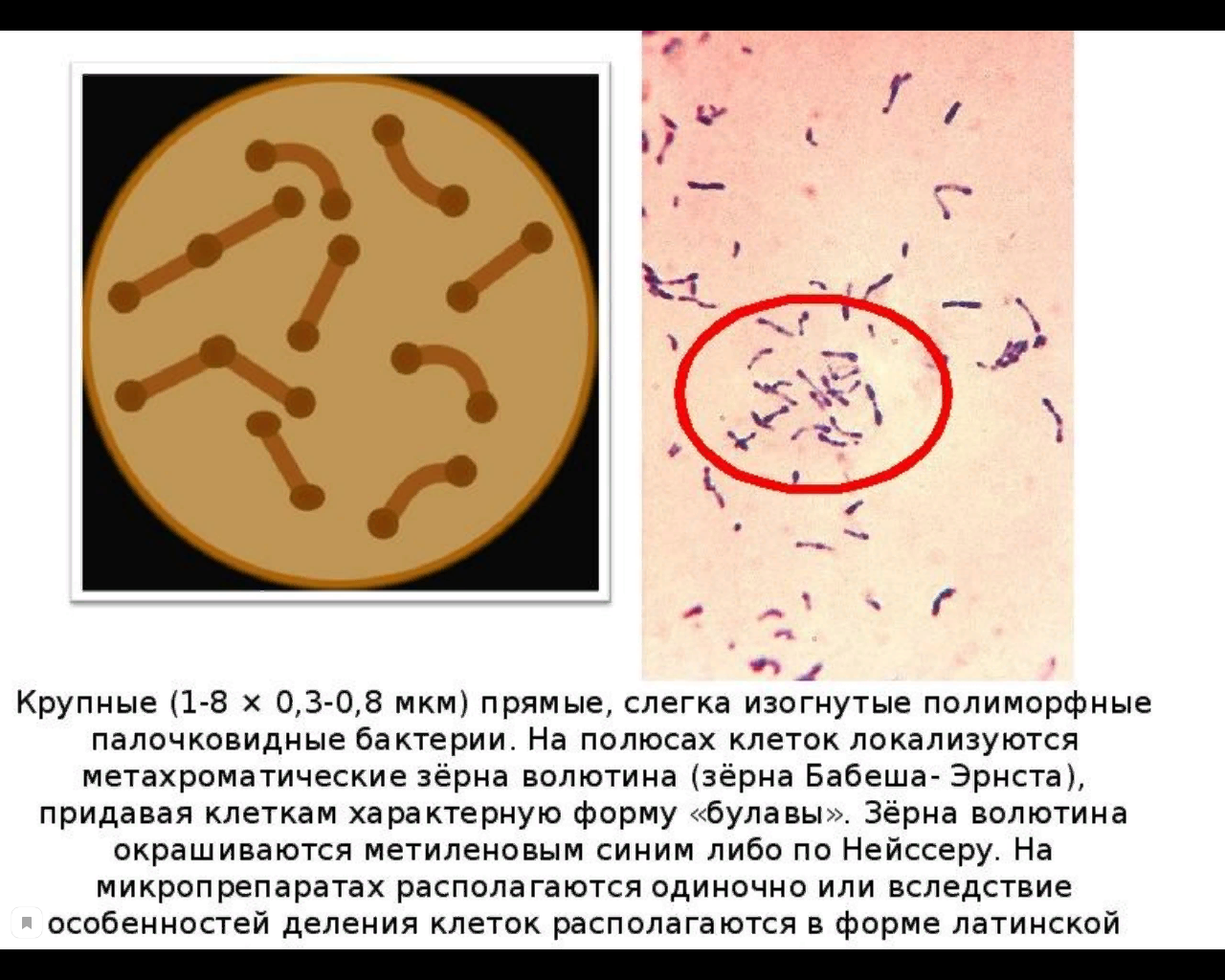
Коринебактерии — прямые или слегка изогнутые грамположительные неподвижные палочки, чаще с утолщениями на концах, напоминающими булаву (coryne — булава), т.к. имеют метахроматические гранулы (зерна волютина), которые являются запасами полифосфатов.
В мазках располагаются: одиночно или в парах, образуя конфигурацию в виде букв V, L, в виде стопки (палисад) из нескольких параллельно расположенных клеток. Не образуют спор и выраженных капсул.
Многие виды дифтероидов являются нормальными обитателями кожи, верхних дыхательных путей, ЖКТ и мочеполовых путей.
Культуральные свойства
Коринебактерии хемоорганотрофы, факультативные анаэробы. Растут на сложных («богатых») питательных средах, содержащих сыворотку крови, например на свёрнутой лошадиной сыворотке по Ру, смеси бычьей сыворотки с сахарным бульоном по Леффлеру.
Питательные среды должны содержать аминокислоты, витамины, ионы металлов (Са2+, Mg2+, Fe2+ и др.), играющие роль ростовых факторов.
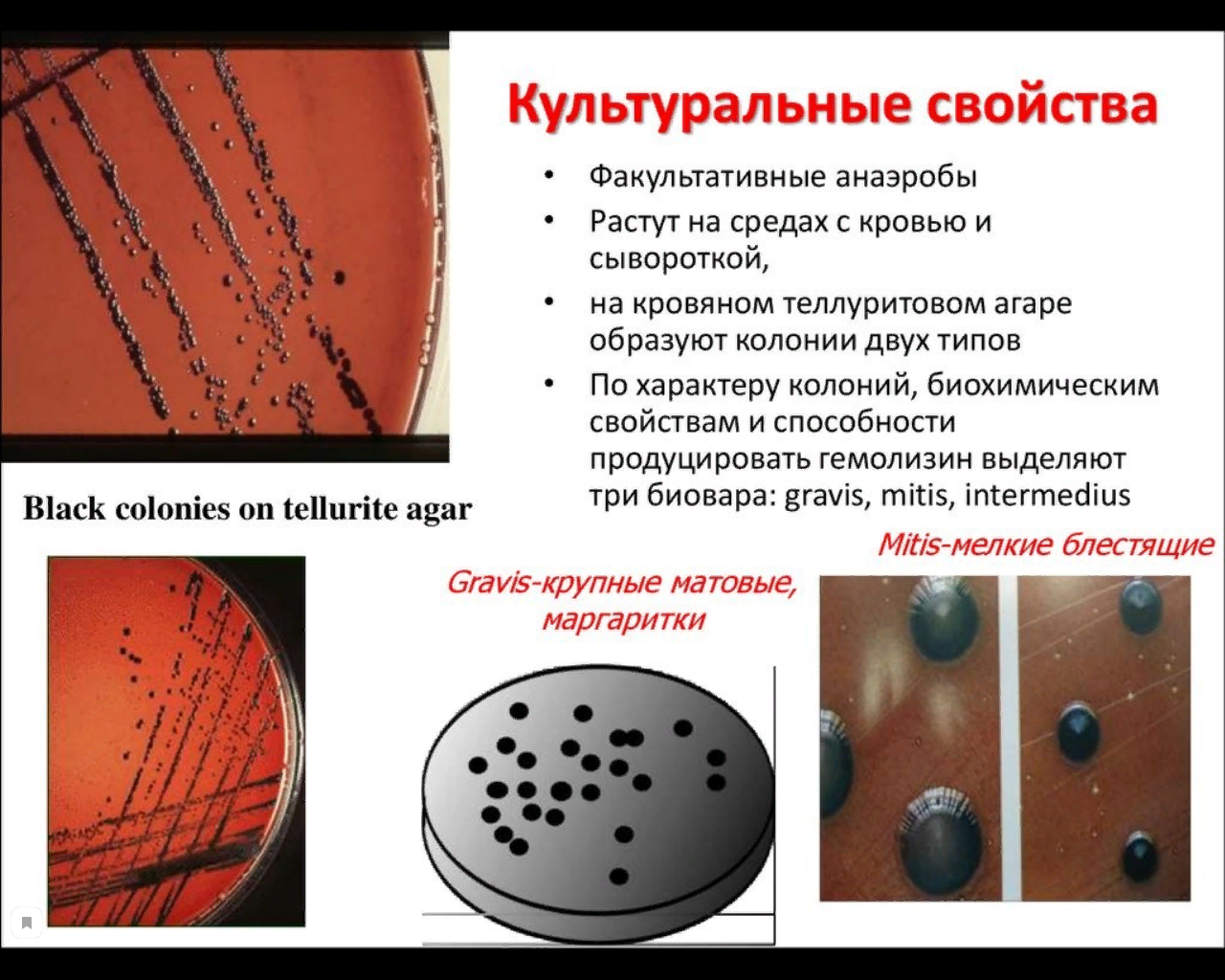
На кровяном агаре с теллуритом (среда Клауберга) колонии приобретают чёрный цвет вследствие восстановления теллурита.
Различают три биовара C. diphtheriae:
• gravis,
• mitis,
• intermedius.
Биовар gravis: являются R-формами C. diphtheriae, образуют крупные шероховатые колонии на плотных питательных средах, на среде с теллуром чёрного цвета. На жидких питательных средах — плёнка и зернистый осадок.
Биовар mitis: являются S- формами C. diphtheriae, образуют гладкие колонии с блестящей поверхностью на плотных питательных средах, на среде с теллуром чёрного цвета. На жидких питательных средах — диффузное помутнение.
Биовар intermedius: промежуточная форма между двумя вышеперечисленными, на плотных питательных средах —мелкие колонии, в жидких — помутнение и осадок.
Антигенная структура.
Выделяют О- и К- антигены.
Полисахаридные О-антигены клеточной стенки обладают межродовыми свойствами, обусловливая неспецифические перекрестные реакции с микобактериями, актиномицетами (нокардиями).
Поверхностные К-антигены — белки, обладают видовой. Выделяют 11 серотипов.
Серотипы 1-5 и 7 относятся к биовару gravis.
Факторы патогенности C. diphtheriae
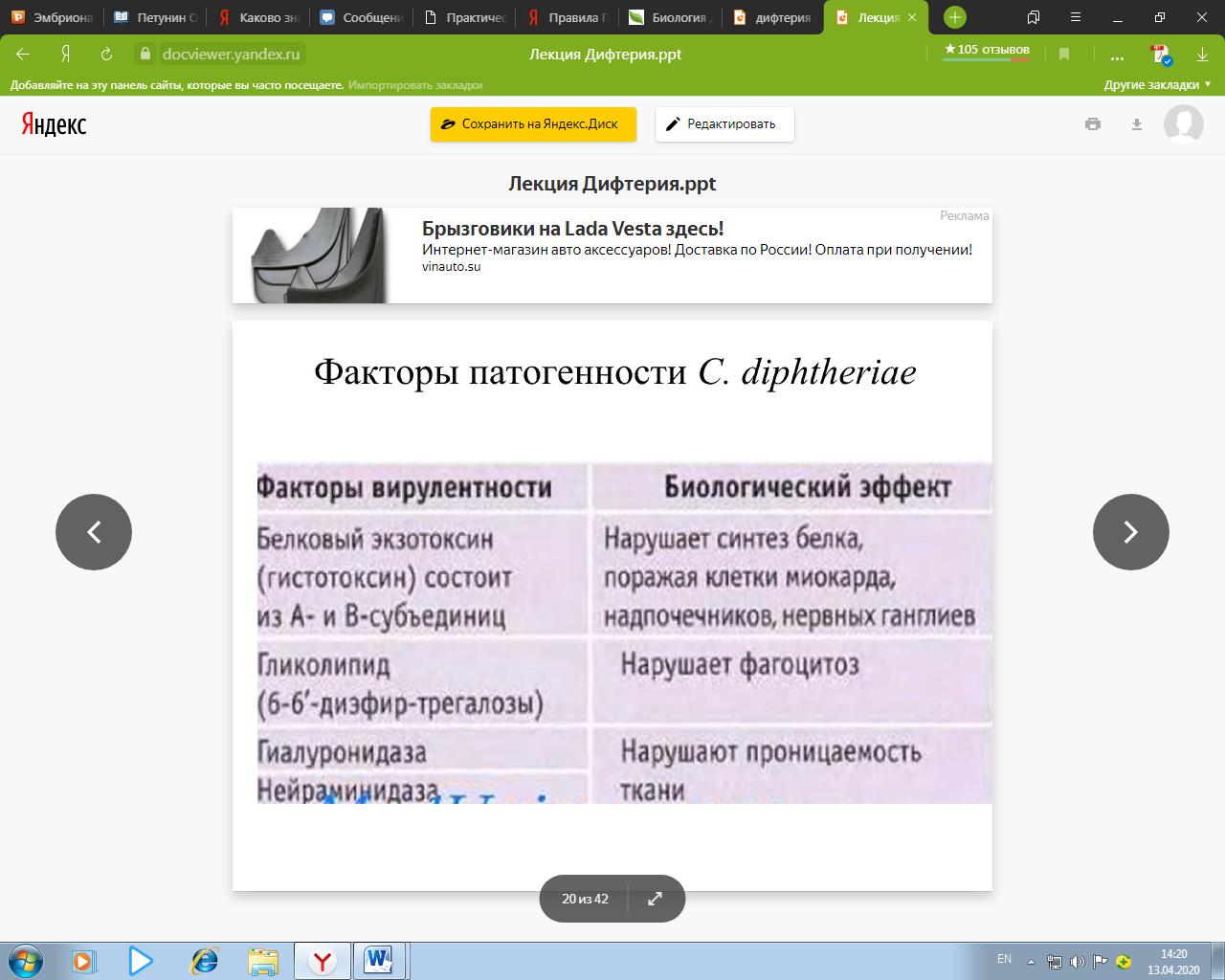
Основным фактором патогенности является экзотоксин (термолабильный высокотоксичный иммуногенный белок), поражающий мышцу сердца, надпочечники, почки, нервные ганглии.
Токсигенные штаммы (типа gravis) вызывают более сложные формы дифтерии. Токсигенность обусловлена наличием гена tox, источником которого является лизогенный бактериофаг в интегрированном состоянии. Имелись сообщения об эффектах действия противофаговой сыворотки на уровень вирулентности возбудителя дифтерии. Также имеется информация о действии бактериофага C. diphteriae на C. ulcerans и C.ovis.
Нативный токсин — полипептид; его образуют фрагменты А (проявляет ферментативную активность) и В взаимодействует с клеточными рецепторами, облегчая проникновение фрагмента А). Клетки всех чувствительных организмов способны рецептировать В-фрагмент и поглощать молекулу посредством эндоцитоза. В кислой среде эндосом (фаголизосом) дисульфидные связи, объединяющие оба компонента, разрушаются, фрагмент В взаимодействует с мембраной эндосомы,облегчая проникновение фрагмента А в цитоплазму.
Механизм цитотоксического действия токсина дифтерии связан с модификацией белков через АТФ-рибозилирование. Подобным свойством обладают многие токсины, но лишь дифтерийный токсин имеет специфичную мишень — фактор элонгации 2 — трансферазу, ответственную за наращивание (элонгацию) Полипептидной цепи на рибосоме.
Токсин дифтерии ингибирует белковый синтез, в том числе и в миокарде, приводя к структурным и функциональным нарушениям, способным вызвать смерть больного. Результат действия токсина дифтерии на нервную ткань — демиелинизация нервных волокон, частоприводящая к параличам и парезам.
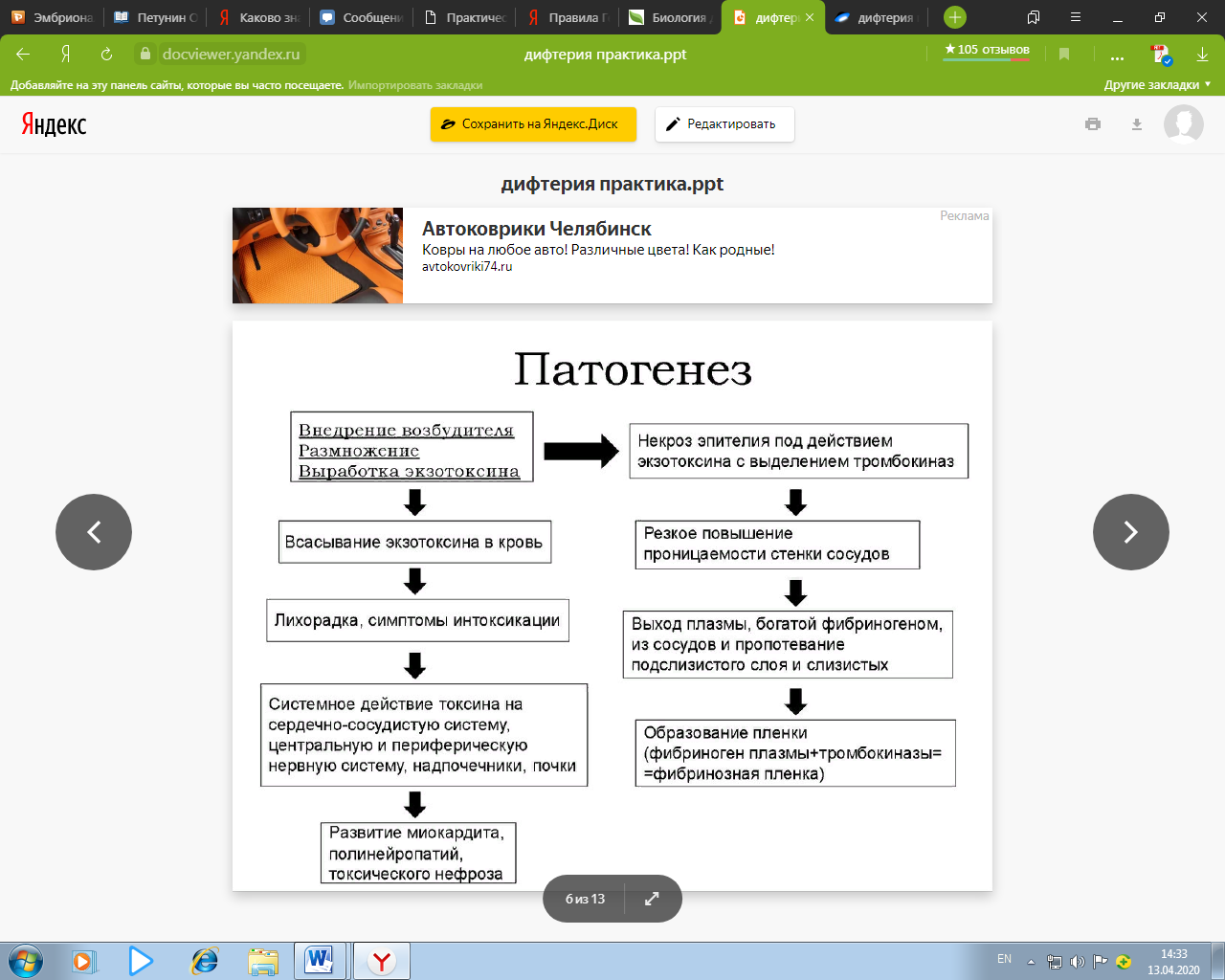
Патогенез и клиника
Дифтерия — инфекционная болезнь, характеризующаяся фибринозным воспалением в зеве, гортани, трахее, реже в других органах и явлениями интоксикации.
Дифтерия известна очень давно: ещё сирийский врач в I веке до н.э. (Аретей Каппадокийский) охарактеризовал его как «злокачественные язвы на миндалинах, ведущие к удушению». Последнее настолько характерно, что в Испании дифтерию называли «гаротильо», то есть маленькая гарота (устройство, рименяемое для удушения преступников).
Кроме дифтерии C. diphtheriae способна вызывать эндокардиты и поражения кожных покровов.
C. diphtheriae способна вызывать не только дифтерию зева, но и поражение кожных покровов.
Эпидемиология.
Единственный источник инфекции — человек – больной или бактерионоситель.
Механизм передачи – респираторный.
Основной путь передачи инфекции —воздушно-капельный, но возможен и контактно-бытовой — через белье, посуду, игрушки. Восприимчивость к дифтерии высокая, наиболее чувствительны к возбудителю дети, однако в последние годы наблюдается «повзросление» болезни. Заболевание чаще встречается осенью.
После перенесенного заболевания вырабатывается стойкий иммунитет.
Профилактика.
В настоящее время основу профилактики дифтерии составляют плановая вакцинация. Адсорбированная коклюшно-дифтерийно-столбнячная вакцина (АКДС-вакцина) состоит из взвеси убитых коклюшных микробов и очищенных дифтерийного и столбнячного анатоксинов, адсорбированных на гидроксиде алюминия. Прививки АКДС-вакциной проводят в возрасте от 3 месяцев до 3 лет. Курс вакцинации состоит из 3-х прививок с интервалом 45 дней. Ревакцинацию АКДС-вакциной проводят однократно через 1.5-2 года после законченного курса вакцинации.
Коринебактерии. Возбудитель дифтерии
Семейство: Corynebacteriaceae
Род: Corynebacterium
Вид: C. diphtheriae (токсиегнные/нетоксигенные)
Подвиды: gravis, mitis, intermrdius
Дифтероиды:
•C.ulcerans (дифтериоподобные заболевания)
•C.pseudodiphtheriticum (палочка Гофмана)– постоянный обитатель зева и носа
•C.xerosis (оппортунистические инфекции - конъюнктивит)
•C.urealyticum – нормальная микрофлора; воспаление мочевого пузыря.
Биохимические свойства

Антигенная структура
Соматические антигены: 11 серотипов (7 – основные, 4 - дополнительные)
Тип gravis серотипы: 1,2,3,4,5,7
Тип mitis серотипы: 6,8,9,10,11
Факторы патогенности
• Факторы адгезии, колонизации и инвазии (гиалуронидаза, нейраминидаза, протеаза)
• Токсический гликолипид клеточной стенки – разрушающее действие на клетки и ткани в месте размножения возбудителя
• ЭКЗОТОКСИН – белок, состоящий из двух субъединиц: А (разрушает фермент аминотрансферазу => остановка синтеза белка в клетке) и В (рецепция). Ген токсигенности находится в ДНК умеренного фага
• Корд-фактор – вещество, которое не дает микробам расходиться друг от друга (склеивание).
Лабораторная диагностика
• Бактериологический метод согласно МУК 4.2.3065-13. Лабораторная диагностика дифтерийной инфекции. Способы постановки пробы на токсигенность.
Проводят в трех случаях:
Для диагностики дифтерии у детей и взрослых с острыми воспалительными процессами в области зева, носа, Носоглотки
по эпидемическим показаниям лиц, находившихся в контакте с источником возбудителя инфекции;
Лиц, вновь поступающих в детские дома, ясли, школы- интернаты и др. с целью выявления бактерионостиелей.
Лечение
• Противодифтерийная антитоксическая сыворотка (вводят внитримышечно)
• Применение антибиотиков (пенициллины, тетрациклины, эритромицин) и сульфаниламидных препаратов.
ЛЕКЦИЯ 4
