
- •Генетически-кодируемые ак: структура и свойства
- •Пептидная связь. Первичная, вторичная, третичная структуры белка. Принципы упаковки белковой молекулы. Типы химических связей.
- •Биологическая роль белков.
- •Пептидная связь. Химический и химико-ферментативный методы синтеза пептидов.
- •Определение первичной последовательности полипептидов.
- •Нуклеозиды и нуклеотиды как компоненты нуклеиновых кислот: структура, физические и химические свойства
- •Олиго- и полинуклеотиды: структура, физические и химические свойства
- •Вторичная структура нуклеиновых кислот: рентгеноструктурные исследования днк, положения Чаргаффа, двойная спираль и ее биологическое значение, комплементарность и взаимная ориентация цепей
- •Рнк: строение, классификация, функции
- •Полимеразная цепная реакция
- •Определение первичной структуры нуклеиновых кислот. Методы химического (по Максаму-Гилберту) и ферментативного (по Сэнгеру) с еквенирования. Автоматизация секвенирования.
- •Химический синтез олигонуклеотидов: основные принципы, синтез на полимерном носителе
- •Олигосахариды: определение, номенклатура, примеры растительных олигосахаридов. Методы изучения строения олигосахаридов.
- •Полисахариды: определение, номенклатура, растительные полисахариды и полисахариды животного происхождения, биологическая роль.
- •Гетерополисахариды и гликопротеины
- •Биологическая роль углеводов
- •Липиды: классификация, роль в живом организме. Простые липиды, воска, жиры и масла: строение и функции.
- •Неомыляемые липиды: строение и функции. Холестерол, стероидные гормоны.
- •Жирные кислоты: насыщенные и ненасыщенные жирные кислоты, незаменимые жирные кислоты, строение и функции.
- •Сложные липиды: классификация, строение, функции.
- •Антибиотики: строение, принципы и направленность действия. Проблема антибиотической устойчивости микроорганизмов.
Рнк: строение, классификация, функции
Полимеры с рибонуклеозидами: аденонин, гуанозин, цитидин, уридин. 3'-5' связи. В отличие от ДНК не только в ядре, но и в цитозоле, рибосомах. Одноцепочечные, но есть дуплексы (двухцепочечные участки), образующие шпильки (комплементарность); в шпильках РНК антипараллельны.
2 класса: кодирующая белки мРНК и не кодирующие белки РНК (тРНК и рРНК), обслуживающие процесс синтеза белка, + митохондриальная РНК (свой генетический и белково-синтетический аппарат)
мРНК: синтезируется в ядре, последовательность (матрица) для синтеза белка, закодированного в гене. На 3'-конце 100-200 аденозинфосфатных остатов (поли(А)-фрагмент), на 5'-конце модифицированный нуклеотид 7-метилгуанозин-5'-трифосфат (кэп). Через несколько десятков нуклеотидов от кэпа инициирующий кодон — триплет AUG (Met). За кодирующим участком терминирующий или стоп-кодон UGA, UUA, UAG.
т РНК:
доставка АК к рибосоме при синтезе
белка. "Клеверный лист". На 3'-конце
участок C-C-A связывания АК, на противоположном
— антикодон-триплет, комплементарный
корону матричной РНК. Каждой АК
соответствуют тРНК с триплетом-кодоном,
благодаря чему информация реализуется
однозначно. В состав тРНК входят минорные
основания (10-12 на молекулу) — метилированные
основания, изомеры, аналоги пиримидинов;
делают молекулу устойчивой к расщеплению
нуклеазами и обеспечивают пространственную
структуру, так как комплементарных пар
не образуют и препятствуют спирализации
молекулы на участках.
РНК:
доставка АК к рибосоме при синтезе
белка. "Клеверный лист". На 3'-конце
участок C-C-A связывания АК, на противоположном
— антикодон-триплет, комплементарный
корону матричной РНК. Каждой АК
соответствуют тРНК с триплетом-кодоном,
благодаря чему информация реализуется
однозначно. В состав тРНК входят минорные
основания (10-12 на молекулу) — метилированные
основания, изомеры, аналоги пиримидинов;
делают молекулу устойчивой к расщеплению
нуклеазами и обеспечивают пространственную
структуру, так как комплементарных пар
не образуют и препятствуют спирализации
молекулы на участках.
рРНК: в рибосомах, до 60% массы. Рибосомы обеспечивают трансляцию. У рРНК много удвоенных спирализованных участков, встречаются минорные основания и производные рибозы.
+ малые интерференционные РНК (миРНК, siRNA) и другие короткоцепочечные РНК, циркулирующие в крови: регуляция процессов репликации ДНК, транскрипции, трансляции.
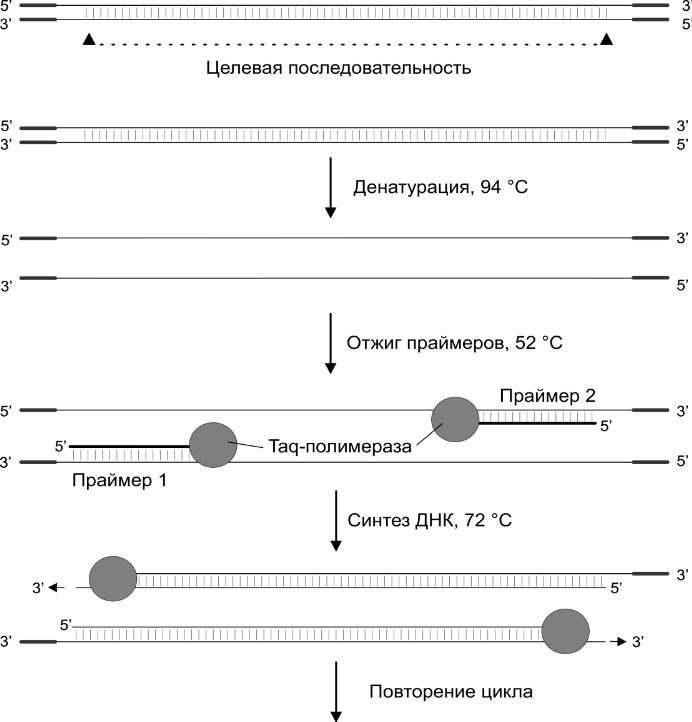
Полимеразная цепная реакция
ПЦР — метод амплификации (накопления) нужных небольших фрагментов ДНК. Нужно для идентификации, нахождения ДНК вирусов или бактерий.
Исходные компоненты: ДНК-матрица, праймеры, дезоксинуклеотидтрифосфаты, ДНК-полимераза. Контроль с помощью температуры.
ДНК-полимераза 1 двигается по одноцепочечной молекуле ДНК, катализирует образование фосфодиэфирных связей между 3' гидроксилом предыдущего нуклеозида и 5' фосфатной группой следующего, то есть рост новой цепи от 5' к 3'. В качестве стройматериала 5' нуклеозидтрифосфаты. Скорость велика, у прокариот 1000 оснований в секунду. Полученные цепи тоже распадаются и от них цикл повторяется.
1 этап: 95, денатурация ДНК.
2 этап: 50-65, отжиг праймеров к ДНК.
3 этап: 70-72, оптимально для полимеразы — достраивание цепей праймера (Taq-полимераза).
Открыл американец Артур Корнберг.
Определение первичной структуры нуклеиновых кислот. Методы химического (по Максаму-Гилберту) и ферментативного (по Сэнгеру) с еквенирования. Автоматизация секвенирования.
Секвенирование — определение последовательности.
ХИМИЧЕСКИЙ: прочтение коротких одноцепочечных олигонуклеотидов. Гидролиз олигонуклеотида и анализ фрагментов с помощью электрофореза.
Мечение олигонуклеотида введением радиоактивного остатка фосфорной кислоты по 5'-концу. Образец делят на 4 порции и в каждую пробирку разные реагенты.
Диметилсульфат расщепляет по гуаниновым звеньям — 4 фрагмента, но только 2 радиоактивно меченые (с радиоактивным фосфатом на 5'-конце)
Муравьиная кислота по пуриновым основаниям на 8 фрагментов, 4 радиоактивные.
Гидразин по пиримидиновым, радиоактивные 4.
Гидразин в присутствии NaCl только по цитидинам — 4 фрагмента, 2 радиоактивных.
4 смеси наносят в лунки геля и проводят электрофорез, радиоактивные метки проявляют на фотобумаге.
Сборка молекулы с самого короткого фрагмента (самый большой пробег на картинке фореза).
ФЕРМЕНТАТИВНЫЙ: способность полимеразы синтезировать новую цепь нуклеотида, комплементарную материнской.
В пробирку: молекулу ДНК (матрица); 2 праймера — олигонуклеотиды длиной 20-25 оснований, комплементарные крайним участкам цепей ДНК, которые будут размножены; набор 5'-нуклеозидтрифосфатов; фермент Pol1. Праймеры нужны, потому что полимераза не работает с "пустого" места, она катализирует конденсацию между 3' гидроксилом предыдущего нуклеотида.
Денатурация ДНК
Понижение температуры, присоединение праймеров с 3' каждой цепи ("отжиг праймеров")
ДНК-полимераза синтезирует на каждой материнской цепи комплементарную дочернюю, удлиняя праймеры 5' → 3'. Полученные 2 двойные молекулы плавят, обжигают праймеры, затем они "прирастают" уже на 4 копиях. С каждым циклом в смеси кол-во копий увеличивается в 2n раз.
Полимераза в ПЦР должна сохранять активность при высокой температуре длительное время, что для белков не характерно — спасибо термофильным бактериям с Taq-полимеразой, которая активна около 100 градусов.
С енгер
разработал способ секвенирования ДНК
на основе ПЦР: метод обрыва цепи или
метод дидезокситерминаторов.
Обрыв/терминация цепи происходит, когда
в дочернюю цепь включается нуклеозидтрифосфат
без 3'-гидроксильной группы —
дидезоксирибонуклеозидтрифосфат.
енгер
разработал способ секвенирования ДНК
на основе ПЦР: метод обрыва цепи или
метод дидезокситерминаторов.
Обрыв/терминация цепи происходит, когда
в дочернюю цепь включается нуклеозидтрифосфат
без 3'-гидроксильной группы —
дидезоксирибонуклеозидтрифосфат.
Все необходимые компоненты ПЦР
Делят на 4 части и дополнительно вносят везде ДДНКТФ
Каждый раз, когда при синтезе цепи в цепь включается остаток, синтез останавливается (нет гидроксила), поэтому в пробирке накапливаются олигонуклеотиды разной длины и заканчивающиеся либо на аденозине, либо на цитидине, либо на гуанозине, либо на тимидине.
Смеси анализируют с помощью гель-электрофореза в денатурирующих условиях. В зависимости от размера продукты ПЦР двигаются в геле с разной скоростью. Картинку проявляют радиоавтографией, для чего продукты метят изотопной меткой. Полученное изображение читают снизу-вверх по полоскам.
Итоговая последовательность комплементарна исходной матрице.
Автоматизация секвенирования: уже в автоматическом режиме, для анализа флуоресцентные метки, которые присоединяют к молекулам дидезокситрифосфатов. Каждая метка имеет свой спектр свечения. Для электрофореза используют капилляры с гелем. Свечение инициируется лазерным лучом и по цвету соотносится с основанием. Есть генный анализатор до 1000 нуклеотидов определяет, 16 образцов одновременно.
