
Bykov-_gistologia_obschaya
.pdfМорфологические характеристики плазматических клеток.
Плазматические клетки имеют сравнительно мелкие размеры (диаметр 9-20 мкм, в среднем - 14 мкм), круглую или овальную форму (рис. 8-8).
Ядро - округлое, расположено эксцентрично, содержит крупные глыбки гетерохроматина, которые располагаются в виде радиальных тяжей ("спиц колеса"). Ядрышко крупное, лежит в центре ядра или эксцентрично.
Цитоплазма окрашена резко базофильно вследствие высокого содержания в ней уплощенных цистерн грЭПС, располагающихся параллельно друг другу и занимающих большую часть ее объема (за исключением околоядерного "дворика" - участка вблизи ядра, в котором находится крупный комплекс Гольджи и некоторые другие органеллы). В отличие от других клеток, интенсивно вырабатывающих белок, продукты синтетической деятельности плазматических клеток (иммуноглобулины) в норме не накапливаются в цитоплазме в секреторных гранулах, а по мере образования транспортируется мелкими пузырьками к плазмолемме, где непрерывно выделяется механизмом экзоцитоза.
Тельца Русселя (правильнее - Рассела) - крупные сферические образования с плотным содержимым, иногда выявляемые в цитоплазме некоторых плазматических клеток. Они ярко окрашиваются фуксином и эозином, содержат гистохимически выявляемые белки и углеводы, дают иммуноцитохимическую реакцию па иммуноглобулины. На электронно-микроскопическом уровне им соответствуют значительные скопления гомогенного материала в резко растянутых цистернах грЭПС. Предполагают, что появление этих телец отражает нарушение взаимосвязи и равновесия процессов синтеза и выведения иммуноглобулинов.
Иммуноглобулины (антитела) представляют собой гликопротеины, которые являются секреторными продуктами В-лимфоцитов и плазматических клеток.
Структура молекулы иммуноглобулинов. Основная структурная единица
(мономер) иммуноглобулинов состоит из двух идентичных тяжелых полипептидных цепей и двух идентичных легких полипептидных цепей, ковалентно связанных дисульфидными мостиками. В молекуле различают связывающий антиген Fab-фрагмент (от англ. antigen-binding - связывающий антиген) и Fc-фрагмент (от англ. crystallizable - кристаллизуемый), который связывается с рецепторами на плазмолемме фагоцитов, тучных клеток, базофилов, В-лимфоцитов. Гены В-лимфоцитов, кодирующие участки тяжелых и легких цепей, которые определяют специфичность связывания антигена, подвергаются постоянной реаранжировке, в результате которой возникает огромное разнообразие антител.
- 241 -
Биологические свойства иммуноглобулинов. У человека имеется пять классов антител – IgA, IgD, IgE, IgC и IgM.
IgG - основной класс иммуноглобулинов, находящихся в сыворотке крови (составляет 75% всех иммуноглобулинов) и тканевых жидкостях. Имеет мономерное строение. Вырабатываются в большом количестве при вторичном иммунном ответе. Способен активировать систему комплемента и связываться с рецепторами на нейтрофилах и макрофагах. Является главным опсонизирующим иммуноглобулином при фагоцитозе и единственным, способным проходить через плацентарный барьер человека от матери к плоду (в течение последних 4-6 нед. беременности). Выработка собственного IgG начинается у ребенка лишь спустя несколько месяцев после рождения. По этой причине в период, предшествующий продукции собственного IgG, когда материнский уже исчез из его организма, наиболее высок риск развития инфекций.
IgM - (8-10% иммуноглобулинов сыворотки крови). Молекула образована комплексом из пяти связанных мономерных единиц (пентамером). Синтез IgМ начинается до рождения; они служат главным классом антител у плода. IgМ - первые антитела, продуцируемые развивающимися В-лимфоцитами и связанные с их плазмолеммой у взрослых. Они являются также основным классом антител, выделяемых в кровь на ранних стадиях первичного иммунного ответа. Связывание антигена с IgМ вызывает присоединение компонента комплемента и его активацию, что может обусловить гибель микроорганизма. Небольшая часть IgМ может поступать в секреты экзокринных желез (секреторный IgМ), связываясь с особым гликопротеином (секреторным компонентом).
IgA - имеется в двух формах: в сыворотке крови и в секретах экзокринных желез. Сывороточный IgA составляет 15-20% общего содержания иммуноглобулинов в крови. Существует в димерной форме (преобладает), а также в виде тримеров и тетрамеров. Связывает комплемент. Секреторный IgA (sIgA) - основной класс антител в секретах экзокринных желез и на поверхности слизистых оболочек. Представлен двумя мономерными единицами, связанными с особым гликопротеином - секреторным компонентом. Последний вырабатывается клетками железистого эпителия и обеспечивает его связывание и транспорт в секреты экзокринных желез. Секреторный блокирует прикрепление (адгезию) микроорганизмов к поверхности слизистых оболочек и ее колонизацию ими. Может играть роль опсонина.
Высокие уровни секреторного IgA в молоке матери защищают слизистые оболочки пищеварительного тракта младенца от кишечных инфекций. Из всех секретов человека максимальные уровни секретор-
- 242 -
ною IgA обнаружены в слезах, а наибольшие концентрации секреторного компонента - в слезных железах (интересно, что содержание этих веществ много выше у мужчин, чем у женщин).
IgE - в норме присутствует в крови в следовых количествах, составляя лишь 0.004% всех иммуноглобулинов в сыворотке крови. Имеет мономерное строение. Вырабатывается преимущественно плазмоцитами в слизистых оболочках пищеварительного тракта и воздухоносных путей. Значение IgE определяется его ролью в аллергических реакциях. IgE связывается с Fcрецепторами на поверхности тучных клеток и базофилов, а его Fab-фрагменты связывают антиген. Связывание антигена (аллергена) с молекулами IgE, фиксированными на этих клетках, вызывает их дегрануляцию с выделением биологически активных веществ, ответственных за клинические проявления аллергических реакций. Воз-можно, локальная выработка IgE способствует защите от гельминтов, так как IgE стимулируют цитотоксическое действие эозинофилов и макрофагов.
IgD - составляет менее 1% общего содержания иммуноглобулинов в сыворотке. Имеет мономерное строение. В больших количествах присутствует на мембране В-лимфоцитов, очевидно, выполняя функцию ан-игенного рецептора; его роль в сыворотке неясна.
Уровни иммуноглобулинов, характерные для взрослого, обеспечивающие полноценную иммунную защиту организма, достигаются лишь в подростковом возрасте.
Патологические процессы, связанные с аномалиями развития и функции В-лимфоцитов и плазматических клеток
Врожденная или приобретенная агаммаглобулинемия (гипогаммаглобулинемия) - иммунодефицитное состояние, связанное с нарушением образования плазмоцитов, которые отсутствуют или имеются в незначительном числе. При этом содержание иммуноглобулинов в крови, тканевых жидкостях и секретах резко снижено. Описаны заболевания, обусловленные избирательным нарушением дифференцировки клеток, продуцирующих IgA (реже - IgG, IgM), или выработкой аномальных иммуноглобулинов. Такие дефекты гуморального иммунитета предрасполагают к развитию рецидивирующих инфекций, тяжесть которых определяется степенью и характером угнетения реакций гуморального иммунитета. В некоторых случаях они сочетаются с дефектами клеточного иммунитета.
- 243 -
Миеломная болезнь (ппазмоцитома) - наиболее распространенное опухолевое заболевание, вызванное нарушением нормального развития плазматических клеток из В-лимфоцитов. Образующаяся в костном мозге и вне его крупная моноклональная популяция измененных плазматических (миеломных) клеток вытесняет остальные элементы миелоидной ткани, обусловливая развитие тяжелой анемии. Миеломные клетки продуцируют огромное количество иммуноглобулинов (М-белка, выявляемого в сыворотке крови), а также некоторые интерлейкины и лимфотоксин, который стимулирует деятельность остеокластов - клеток, разрушающих костную ткань (вызывая характерные деструктивные измененггя скелета).
НУЛЕВЫЕ ЛИМФОЦИТЫ
Нулевые лимфоциты (0-лимфоциты) не имеют маркеров Т- или В-
клеток и составляют 5-10% лимфоцитов крови. К этой категории относят NKклетки, а также стволовые клетки крови.
NK-клетки (натуральные, или естественные, киллеры, NK-лимфоциты - от англ. Natural Killer cells) составляют основную часть нулевых лимфоцитов. На них приходится 5-10% (по некоторым источникам - до 15%) лимфоцитов в периферической крови и 1-2% лимфоцитов в селезенке. В лимфатических узлах они единичны. Эти клетки имеют морфологические признаки больших гранулярных лимфоцитов (см. главу 7). Они развиваются в костном мозге из самостоятельного лимфоидного предшественника, отличного от предшественников В- и Т-лимфоцитов. После попадания в кровь NK-клетки циркулируют в ней и проникают в селезенку (механизмы рециркуляции NKклеток изучены слабо). Характерными маркерами NK-клеток служат CD16, CD56 и CD57. Продолжительность жизни NK-клеток составляет от нескольких дней до нескольких месяцев.
Функциональные свойства NK-клеток. NK-клетки способны осуществлять не опосредованный антителами контактный лизис клетокмишеней. Они активируются ИФН, ИЛ-2 и ИЛ-12, при активации продуцируют ряд цитокинов (ИФНα и ИФНγ, ИЛ-1, -2, -4 и ФНОβ). Клетками-мишенями NKклетки могут служить опухолевые клетки, клетки, зараженные вирусами, бактериями, грибами и простейшими, а также стареющие и поврежденные клетки.
- 244 -
Главными функциями NK-клеток являются:
1)Обеспечение противоопухолевого иммунитета. NK-клетки играют решающую роль в противоопухолевом иммунитете, так как они осуществляют иммунный надзор более активно, чем Т-лимфоциты. Отмечено, что у многих больных с опухолями активность NK-клеток снижена. Повышение их активности в организме больных или введение им собственных NK-клеток, активированных in vitro, служат новыми перспективными направлениями разработки методов лечения новообразований.
2)Обеспечение противоинфекционного иммунитета. NK-клетки эффективно распознают зараженные вирусами клетки и оказывают на них контактное цитотоксическое действие. Отмечена также их роль в обеспечении иммунитета при некоторых бактериальных, микотических и паразитарных инфекциях: они контактно элиминируют клетки, в цитоплазме которых находятся возбудители; на некоторые возбудители они метут оказывать непосредственное токсическое действие посредством секреции растворимых факторов (главным образом, ИФНγ).
3)Участие в регуляции гемопоэза путем стимулирующего и ингибирующего влияния продуктов NK-клеток на различные КОЕ.
Цитотоксические механизмы разрушения клеток мишеней NKклетками,
по-видимому, аналогичны используемым Тк, хотя некоторые авторы полагают, что главным из них является перфорин-зависимый. Для проявления цитотоксического эффекта NK-клеток не требуется распознавания ими молекул МНС на клетках-мишенях. Поскольку NKклетки обладают рецепторами к Fcфрагменту IgG, они способны обеспечивать антителозависимую клеточную цитотоксичность (которую ранее приписывали особой постулируемой субпопуляции нулевых лимфоцитов - К-клеткам). NK-клетки не обладают антигенной специфичностью и не приобретают иммунологическую память.
Стволовые клетки крови обладают морфологическими признаками малых лимфоцитов и вследствие рециркуляции метут обнару¬иваться в крови, где их количество чрезвычайно мало (см. главу 9). Так как они не располагают маркерами, свойственными Т- и В-лимфоцитам, при идентификации их включают в группу нулевых лимфоцитов.
РЕЦИРКУЛЯЦИЯ ЛИМФОЦИТОВ
Рециркуляция лимфоцитов - миграция лимфоцитов из крови в органы иммунной системы, периферические ткани и обратно в кровь. Она характерна для значительной части лимфоцитов; лишь, небольшая их часть относится к нерециркулирующему пулу.
- 245 -
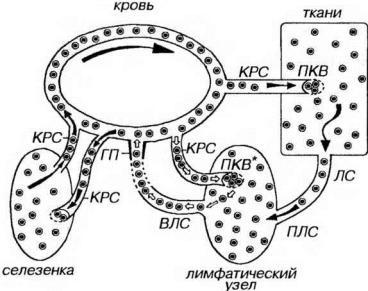
Цель рециркуляции лимфоцитов - постоянное патрулирование тканей организма иммунокомпетентными лимфоцитами (осуществление "иммунного надзора"), эффективное обнаружение чужеродных и измененных собственных антигенов (нативных и представляемых АПК), снабжение органов лимфоцитопоэза информацией об антигенах в различных тканях. Выделяют быструю рециркуляцию (осуществляется в течение нескольких часов) и медленную (периферическую) рециркуляцию (длится неделями), которые охватывают различные пути (рис. 8-9).
Рис. 8-9. Пути рециркуляции лимфоцитов. Быстрая рециркуляция лимфоцитов (белые стрелки) показана на примере лимфатического узла: лимфоциты поступают в него с кровью, приносимой кровеносными сосудами (КРС), и через стенку пост капиллярных венул с высоким эндотелием (ПКВ*) мигрируют в его Т- и В-зависимые зоны. Из лимфатического узла лимфоциты с током лимфы через выносящий лимфатический сосуд (ВЛС) попадают в грудной проток (ГП), возвращаясь в кровь. При медленной рециркуляции (черные стрелки) лимфоциты с кровью по КРС попадают в различные органы, где через стенку посткапиллярных венул с плоским эндотелием (ПКВ) мигрируют в периферические ткани. Из тканей лимфоциты с током лимфы по приносящему лимфатическому сосуду (ПЛС) попадают в лимфатический узел, после чего через ВЛС и ГП возвращаются в кровь. В селезенку и из нее лимфоциты направляются по КРС.
Пути быстрой рециркуляции:
кровь -> посткапиллярные венулы с высоким эндотелием (в органах иммунной системы) -> Т- и В-зависимые зоны периферических органов иммунной системы -> лимфоток -> грудной проток -> кровь.
- 246 -
Этим путем осуществляется миграция 90% лимфоцитов, имеющихся в лимфе грудного протока.
Пути медленной рециркуляции:
кровь -> посткапиллярные венулы с плоским эндотелием (в неиммунных органах) -> периферические ткани -> афферентные лимфатические сосуды -> лимфатические узлы -> лимфоток -> грудной лимфатический проток -> кровь. Этот путь проделывают 5-10% лимфоцитов, содержащихся в лимфе грудного протока.
- 247 -
Глава 9
КРОВЕТВОРНЫЕ ТКАНИ
Кроветворные (гемопоэтические) ткани обеспечивают физиологическую регенерацию форменных элементов крови (гемопоэз). Они образуются в течение внутриутробного развития и активно функционируют на протяжении всей жизни индивидуума.
КРОВЕТВОРЕНИЕ В ТЕЧЕНИЕ ВНУТРИУТРОБНОГО РАЗВИТИЯ
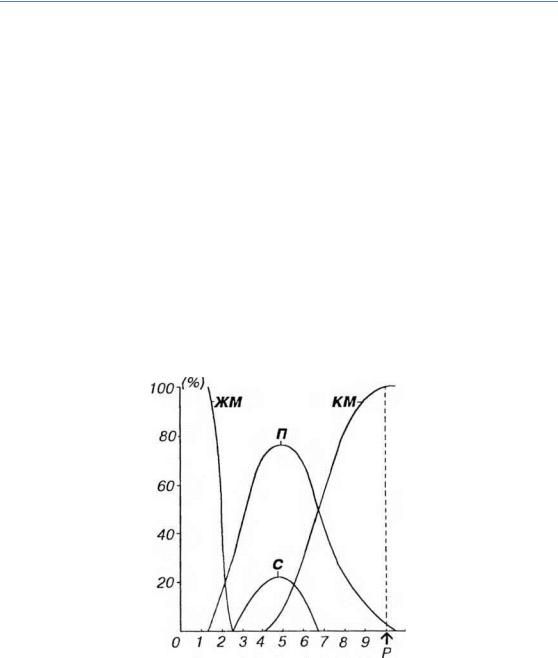
В течение внутриутробного развития место образования форменных элементов крови (гемопоэза) несколько раз изменяется. Наиболее ранним из них служит желточный мешок, а позднее его сменяют печень, селезенка, костный мозг и лимфоидные органы (рис. 9-1).
Рис 9-1. Локализация кроветворных тканей во внутриутробном периоде По оси ординат - доля участия органа в кроветворении (%), по оси абсцисс - срок внутриутробного развития (мес.); Р - момент рождения. ЖМ - желточный мешок, П - печень, С - селезенка, КМ - костный мозг. Пояснения в тексте.
- 248 -
Кроветворение в стенке желточного мешка (3-10-я нед.) является, по сути, вне зародышевым, поскольку он относится к внезародышевым провизорным органам. Оно тесно связано с развитием первых сосудов, которые появляются в мезенхиме стенки желточного мешка с возникновением кровяных островков.
Кровяные островки образуются в мезенхиме вследствие индуцирующего влияния энтодермы желточного мешка. Они имеют вид мелких компактных скоплений округлившихся мезенхимных клеток, превращающихся в стволовые клетки крови (СКК). Островки снаружи охватываются уплощающимися и образующими соединения клетками, которые формируют эндотелиальную выстилку. Сливаясь друг с другом, кровяные островки образуют в стенке желточного мешка сосудистую сеть.
СКК в кровяном островке делятся и дифференцируются в первичные эритробласты (называемые из-за своих больших размеров также мегалобластаии - от греч. megas - большой и blastos - росток). Мегалобласты - крупные клетки с базофильной цитоплазмой, которые по мере накопления гемоглобина (HbF - фетального) превращаются в полихроматофильные, а затем в оксифильные эритробласты, дающие начало крупным ядросодержащим или безъядерным первичным эритроцитам (мегалоцитам). Описанное мегалобластическое кроветворение свойственно эмбриональному периоду, но может возникать после рождения при тяжелом заболевании крови - злокачественной анемии (обусловленной недостаточностью витамина В12). Наряду с эритроцитопоэзом, происходящим внутри сосудов (интраваскулярно), вне сосудов (экстраваскулярно) образуются в небольшом числе гранулоциты. Из желточного мешка СКК мигрируют в печень и другие кроветворные органы. По некоторым представлениям, СКК в каждом из органов кроветворения имеют местное происхождение (образуются in situ).
Кроветворение в печени осуществляется, начиная примерно с 5-6-й нед. внутриутробного развития и достигает максимальной активности на 2-м месяце (когда кроветворение на 80% обеспечивается печенью и на 20% - селезенкой). Оно стихает с началом активной деятельности костного мозга и полностью завершается обычно в течение первых двух недель после рождения. В печени из СКК преимущественно экстраваскулярно дифференцируются эритроциты, гранулоциты и мегакариоциты. В ней на 7-й нед. впервые выявляются NKклетки, которые в крови обнаруживаются значительно позднее (на 27-28-й нед.).
Кроветворение в селезенке протекает экстраваскулярно и начинается позднее, чем в печени (с середины 3-го мес.), достигая наибольшей активности с 4-го по 6-й мес. Первоначально в селезенке образу-
- 249 -
ются все виды форменных элементов крови, а во второй половине внутриутробного развития начинает преобладать лимфоцитопоэз. При некоторых патологических изменениях системы крови (миелопролиферативных заболеваниях), когда красный костный мозг оказывается не в состоянии производить достаточного количества клеток крови, гемопоэз может вновь возникнуть в печени и селезенке (экстрамедуллярное кроветворение).
Кроветворение в тимусе начинается со 2-го мес. внутриутробного развития и протекает с образованием Т-лимфоцитов, которые в дальнейшем расселяются в лимфоидные органы - селезенку и лимфатические узлы (закладываются на 9-10-й нед.).
Кроветворение в костном мозге начинается с 3-го мес. внутриутробного развития. СКК заселяют полости в образующихся костях и дают начало всем видам форменных элементов крови. На 5-м мес. в нем образуются лейкоциты и тромбоциты, на 7-м - эритроциты. Костный мозг замещает печень и селезенку в качестве кроветворного органа и становится окончательным (дефинитивным) центральным органом гемопоэза в конце развития плода, оставаясь таковым у новорожденного, ребенка и взрослого.
КРОВЕТВОРЕНИЕ В ПОСТНАТАЛЬНОМ ПЕРИОДЕ
В постнатальном периоде кроветворение осуществляется в особых гемопоэтических тканях - миелоидной и лимфоидной. Эти ткани высоко специализированы в структурном и функциональном отношениях и обеспечивают интенсивную физиологическую регенерацию форменных элементов крови, большая часть из которых обладает коротким жизненным циклом.
Миелоидная ткань (от греч. myelos - костный мозг) является функционально ведущей тканью красного костного мозга, который с периода новорожденноcти и до 3-4 лет располагается во всех полостях трубчатых и плоских костей. В течение последующих нескольких лет по мере быстрого роста костей красный костный мозг занимает в них все меньше места. Ко времени созревания скелета он сохраняется только в плоских костях (позвонки, грудина, ключица, лопатка, ребра, кости черепа, таза) и эпифизах длинных трубчатых костей; все остальные участки замещаются жировой тканью (превращаясь в желтый костный мозг), хотя и сохраняют потенциальную способность к возоб-
- 250 -
