- •Параметри стану|достатку|
- •Рівняння стану|достатку| ідеального газа
- •I закон термодинаміки
- •3.1. Теплоємність
- •4. II закон термодинаміки
- •5. Термодинамічні процеси
- •Реальні гази
- •Пари, основні визначення
- •8. Вологе|вогке| повітря
- •9. Витікання газів і пари
- •10. Цикли двз
- •11. Цикли гту
- •12. Цикли парових установок
- •13. Цикли холодильних установок
- •14. Теорія теплообміну
- •15. Теплопровідність
- •15.1 Теплопровідність через плоску стінку
- •Теплопровідність через циліндрову стінку
- •16. Конвективний теплообмін
- •17.Теплопередача
- •17.1 Плоска стінка
- •17.2 Циліндрична стінка
- •18. Теплообмінні|теплообмін| апарати
- •18.1 Класифікація апаратів
- •18.2 Схеми руху теплоносіїв
- •18.3 Основні рівняння розрахунку теплообмінних|теплообмін| апаратів
- •19. Паливо|пальне|
- •20. Котельні агрегати
4. II закон термодинаміки
Формулювання:
1. Теплота не може довільно переходити від тіл менш нагрітих до тіл більш нагрітих.
2. Неможливо створити періодично діючу теплову машину, всі дії якої зводилися б до піднімання|підняття| вантажу|тягаря| і охолодження|охолодження| теплового джерела.(Вічний двигун II роду неможливий).
 - аналітичне вираз|вираз|
закону.
- аналітичне вираз|вираз|
закону.
Знак
«=»|
відноситься до протікання в системі
оборотних процесів, при цьому ентропія
системи не змінюється. Знак «>»|
відноситься до протікання в системі
необоротних|незворотних|
процесів, при цьому ентропія системи
досягає будь-якого максимального
значення. Якщо
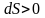 -
теплота підводиться, якщо
-
теплота підводиться, якщо
 - відводиться|відводить|.
- відводиться|відводить|.
5. Термодинамічні процеси
1.
Ізобарним
називається процес, що протікає з|із|
постійним тиском|тисненням|
.
Співвідношення між параметрами
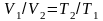 - закон Гей – Люсака.
- закон Гей – Люсака.
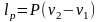 ;
;
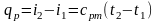
2.
Ізохорним
називається процес, що протікає з|із|
постійним об'ємом|обсягом|,
, ,
- закон Шарля;
,
- закон Шарля;
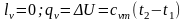
3.
Ізотермічним
називається процес, що протікає з|із|
постійною температурою,
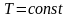 ,
,
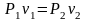 ,
закон Бойля – Маріотта.
,
закон Бойля – Маріотта.

4.
Адіабатним
називається процес, що протікає без
теплообміну з|із|
навколишнім середовищем при постійній
ентропії
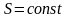 ,
,
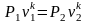 ,
,
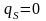 ;
;
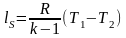
де - показник адіабати;
- показник адіабати;
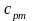 - середня теплоємність при постійному
тиску|тисненні|,
- середня теплоємність при постійному
тиску|тисненні|,
 - середня теплоємність при постійному
об'ємі|обсязі|.
- середня теплоємність при постійному
об'ємі|обсязі|.
5.
Політропним
називається процес, що протікає з|із|
постійною теплоємністю і підпорядковується
рівнянню
 ;
;
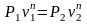 ;
п -
показник політропи
;
п -
показник політропи
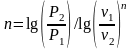
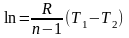 ;
;
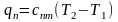 ;
;
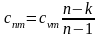
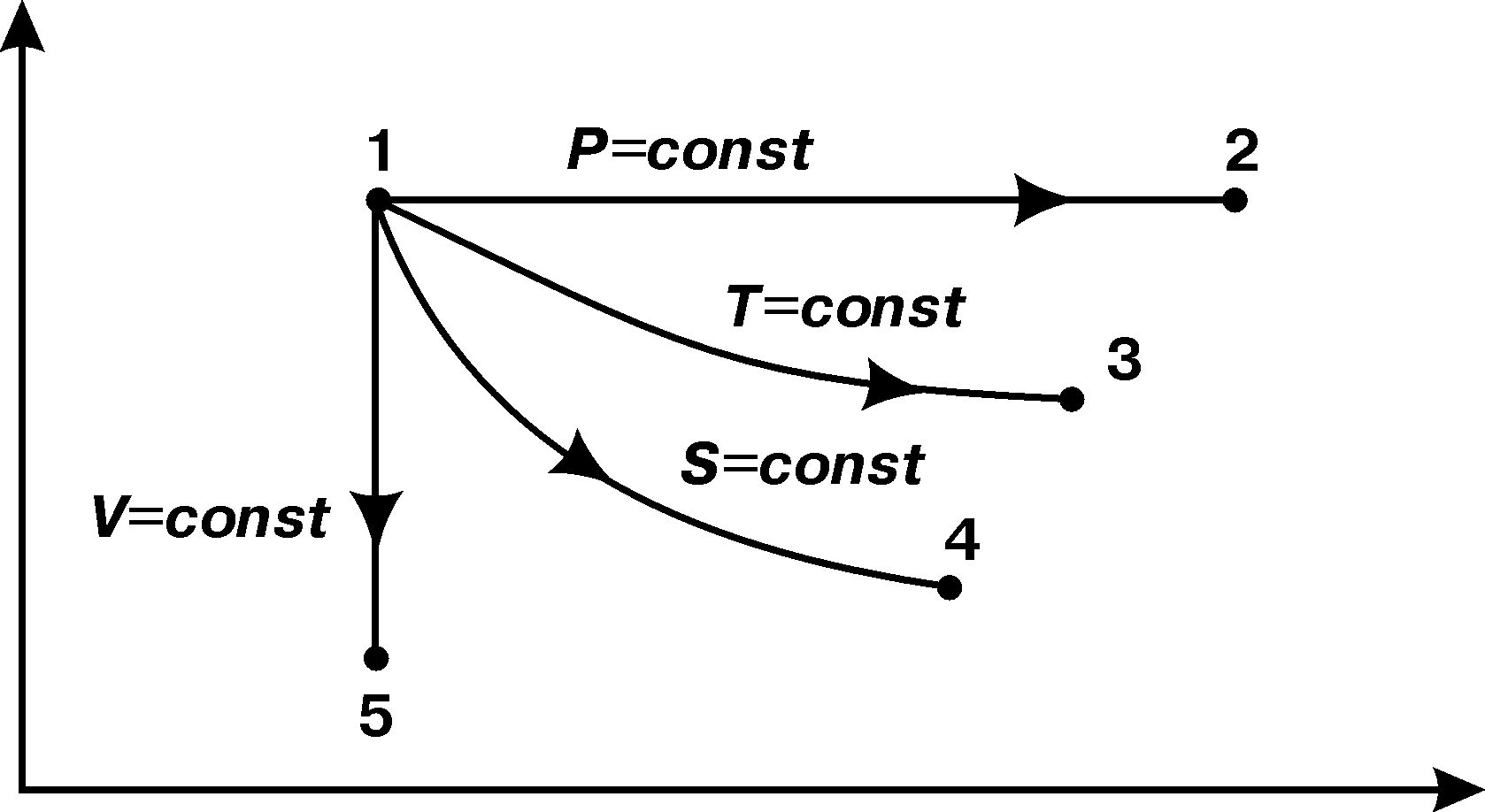
Процеси в P-| V координатах
|
Лінії на P – V діаграмі: 1-2 – ізобара, ; 1-3 – ізотерма, ; 1-4 – адіабата
,
1-5 – ізохора,
|
Реальні гази
Реальним газом називається газ, між молекулами якого існують сили тяжіння і відштовхування, а молекули і атоми газу мають масу і об'єм|обсягом|. Рівняння стану|достатку| реального газу Ван - дер-Ваальса
|
а, b – постійні коефіцієнти, які залежать від природи газу; v – власний об'єм молекул;
|
|
|
|Перехід речовини з|із| одного агрегатного стану|достатку| в інший називається фазовим переходом. Перехід з твердої фази в рідку – плавлення. Перехід з рідкої фази в пароподібну: випаровування – пароутворення з поверхні рідини, кипіння – бурхливе пароутворення в об'ємі з паровими міхурами. Перехід з пароподібного стану в рідкий – конденсація. Перехід з твердої фази у пароподібну – сублімація. Криві фазових переходів зображаються в P-t діаграмі.
|
Рівноважні криві: АВ – плавлення; АК – пароутворення; АС – сублімація. Точка, у якій речовина існує в трьох агрегатних станах, називається потрійною точкою (т.А). Лінія пароутворення закінчується критичною точкою К. Її параметри. У цій точці:
Ніяким зусиллям стиснення неможливо сконденсувати пару. |

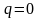 ,
;
,
;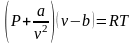
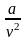 - внутрішній тиск.
- внутрішній тиск.