
- •1. Липиды, поступающими с пищей: триглицериды, фосфолипиды и холестерол. Насыщение и ненасыщенные жирные кислоты. Депонирование в организме. Роль в выработке энергии
- •2. Ожирение и его лечение. Лекарственные средства, влияющие на аппетит
- •Первичное ожирение
- •Принцип лечения
- •4.Эмульгирование жиров в жкт: фармакологическая регуляция.
- •5. Всасывание холестерола и лекарственные вещества, его ингибирующие
- •6. Биосинтез и эстерификация жирных кислот. Лекарственные средства, ингибирующие эти процессы.
- •Этерификация жирных кислот
- •7. Биосинтез и транспорт холестерола; лекарственные средства, влияющие на эти процессы
- •1. Синтез мевалоновой кислоты.
- •Липопротеины высокой плотности Функция
- •Метаболизм
- •Реакция этерификации холестерола при участии лецитин:холестерол-ацилтрансферазы
- •Транспорт холестерола и его эфиров в организме (цифры соответствуют пунктам метаболизма лпвп по тексту) Липопротеины низкой плотности Функция
- •Метаболизм
- •Синтез олеата холестерола при участии ацил-sKoA-холестерол-ацилтрансферазы
- •8. Метаболизм триглицеридов и лекарственные вещества, его стимулирующие
- •9. Всасывание липидов в кишечнике: фармакологическая регуляция (секвестранты желчных кислот)
- •11. Катаболизм липидов
- •12. Биосинтез и окисление кетоновых тел
- •13. Перекисное окисление липидов и лекарственные средства, его регулирующие.
- •14. Взаимопревращения жирных кислот
- •16. Эйкозаноиды: субстраты для синтеза эйкозаноидов, синтез лейкотриенов, липоксинов
- •17. Использование производных эйкозаноидов в качестве лекарственных средств
- •19. Регуляция липидного обмена
- •20. Абеталипопротеинемия
- •21. Биохимические изменения, приводящие к атеросклерозу
- •24. Метаболизм желчных кислот
14. Взаимопревращения жирных кислот
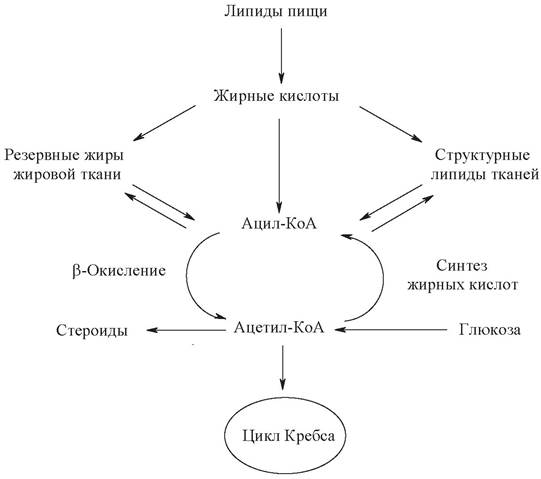
Жирные кислоты поступают с пищей или синтезируются в организме (кроме полиеновых кислот). Субстраты, необходимые для синтеза жирных кислот, образуются при катаболизме глюкозы и таким образом, часть глюкозы превращается сначала в жирные кислоты, а затем в жиры. Хотя специфический путь катаболизма жирных кислот заканчивается образованием ацетил-КоА, служащим исходным субстратом для синтеза жирных кислот, процессы синтеза и окисления жирных кислот необратимы. Они происходят в разных компартментах клеток (биосинтез протекает в цитозоле, а окисление - в митохондриях) и катализируются разными ферментами. Окисление жирных кислот как источников энергии увеличивается в постабсорбтивный период, при голодании и физической работе. В этих состояниях их концентрация в крови увеличивается в результате мобилизации из жировых депо, и они активно окисляются печенью, мышцами и другими тканями. При голодании часть жирных кислот в печени превращается в другие "топливные" молекулы - кетоновые тела. Они, в отличие от жирных кислот, могут использоваться нервной тканью как источник энергии. При голодании и длительной физической работе кетоновые тела служат источником энергии для мышц и некоторых других тканей.
Продуктами каждого цикла в-окисления являются FADH2, NADH и ацетил-КоА.
15. Обмен фосфолипидов: фармакологическая регуляция
Обмен фосфолипидов
Синтез фосфатидилхолинов, фосфатидилэтаноламинов и фосфатидилсеринов
Синтез фосфатидилхолинов, фосфатидилэтаноламинов и фосфатидилсеринов
Начальные этапы синтеза глицерофосфолипидов и жиров протекают одинаково до образования фосфатидной кислоты. Фосфатидная кислота может быть синтезирована двумя различными способами: через глицеральдегид-3-фосфат и через дигидроксиацетонфосфат.

-На следующем этапе фосфатидаза отщепляет от фосфатидной кислоты фосфатный остаток, в результате чего образуется диацилглицерол. Дальнейшие превращения диацилглицерола также могут идти разными путями. Один из вариантов - образование активной формы «полярной головки» фосфолипида: холин, серин или этаноламин превращаются в ЦЦФ-холин, ЦДФ-серин или ЦЦФ-этаноламин.
Синтез ЦДФ-холина. «Полярная головка» фосфатидилхолина превращается за счёт энергии АТФ в активную форму - фосфохолин, который присоединяется к ЦТФ с одновременным удалением РРi, что сдвигает равновесие реакции вправо. Образовавшийся ЦДФ-холин - донор холина для синтеза молекул фосфатидилхолинов. ЦДФ-холин - цитидилдифосфохолин; ЦМФ - цитидилмонофосфат; Р - остаток фосфорной кислоты.

- Далее диацилглицерол взаимодействует с ЦДФ-производными, при этом выделяется ЦМФ, образует соответствующий фосфолипид, например, фосфатидилхолин. Между глицерофосфоли- пидами возможны различные взаимопревращения. Фосфатидилхолин может поступать и другим путём: из фосфатидилэтаноламина, получая последовательно 3 метальные группы от SAM. Фосфатидилсерин может превращаться в фосфатид ил этаноламин путём декарбоксилирования. Фосфатидилэтаноламин может превращаться в фосфатидилсерин путём обмена этаноламина нан.
NB! Дипальмитоилфосфатидилхолин - основной компонент сурфактанта лёгких
Сурфактант - внеклеточный липидный слой с небольшим количеством гидрофобных белков, выстилающий поверхность лёгких альвеол и предотвращающий слипание стенок альвеол во время выдоха. Основной компонент сурфактанта - дипальмитоилфосфатидилхолин, составляющий до 80% от всех фосфолипидов, входящих в состав сурфактанта. Кроме того, в сурфактант входят гидрофобные белки, которых больше 10 - 20%.
Влияние сурфактанта на функцию альвеол.

- Синтез дипальмитоилфосфатидилхолина (лецитина) в пневмоцитах II типа происходит в процессе эмбрионального развития и увеличивается в период от 32 до 36 нед беременности.
Важным показателем нормального формирования сурфактанта служит соотношение фосфа- тидилхолин / сфингомиелин> 4. Это соотношение можно определить, исследуя состав амниотической жидкости. Недостаточное формирование сурфактанта у недоношенных детей после рождения приводит к развитию респираторного дистресс-синдрома - основной смерти у этой группы новорожденных. Соотношение фосфатидилхолин / сфингомиелин <2 указывает на высокий риск развития респираторного дистресс-синдрома. В случае необходимости лечения беременных кортикостероидами стимулирует синтез сурфактанта в лёгких плодах и снижает риск развития респираторного дистресс-синдрома.
