
- •Минобрнауки россии
- •1. Литературная часть
- •1.1Колориметрические методы
- •1.1.1 Буферный метод
- •1.1.2 Безбуферный метод
- •1.1.3 Недостатки колориметрических методов.
- •1.2 Потенциометрические методы.
- •1.2.1 Нормальный элемент Вестона
- •1.2.2 Электроды сравнения
- •1.2.2.1 Водородный электрод
- •1.2.2.2 Каломельный электрод
- •1.2.2.3 Хлореребрянный электрод
- •1.2.2.4 Индикаторные электроды
- •1.2.3 Преимущества и недостатки различных потенциометрических методов определения pH
- •2. Экспериментальная часть
- •2.2 Методика определения pH буферных раствор.
- •3. Обсуждение результатов
- •3.2 Определение pH c использованием двойной хингидронной цепи.
- •3.3 Определение pH при помощи стеклянного электрода.
2. Экспериментальная часть
2.1. Характеристика исходных веществ.
Натрий-ацетатный буфер (ацетатный буфер) — буферный раствор, содержащий ацетат натрия и уксусную кислоту. Значение pK ацетатного буфера составляет около 4,75, поэтому применение находят буферы со значениями рН от 3 до 6. Для приготовления буфера используют тригидрат ацетата натрия (136,09 г/моль) и раствор уксусной кислоты (например, 0,2 М раствор, который содержит 12,01 г/л уксусной кислоты). Натрий-ацетатный буфер используют в биохимии для растворения белков, при хроматографии, при осаждении ДНК для повышения ионной силы раствора.
Хингидрон – это интенсивно окрашенное, С6Н4О2 – С6Н4 (ОН)2 представляет собой молекулярное соединение хинона и – гидрохинона(1:1). Представляет собой систему, в которой взаимодействия с переносом заряда играют важную роль и водородные связи, по-видимому, оказывают влияние на кристаллическую структуру.
Хиноны
— полностью сопряжённые циклогексадиеноны
и их аннелированные аналоги. Существуют
два класса хинонов: пара-хиноны с
пара-расположением карбонильных групп
(1,4-хиноны) и орто-хиноны с орто-расположением
карбонильных групп (1,2-хиноны). Благодаря
способности к обратимому восстановлению
до двухатомных фенолов некоторые
производные пара-хинонов участвует в
процессах биологического окисления.
Общий метод синтеза хинонов — как
моноциклических бензохинонов и их
производных, так и полициклических
конденсированных хинонов, причём если
для окисления производных бензола
требуется, как правило, наличие
электродонорных заместителей, активирующих
ароматическое кольцо (например, гидрокси-
или аминогрупп), то в случае полициклических
ароматических углеводородов возможно
и прямое окисление до соответствующих
хинонов.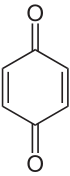
Гидрохинон
[6] (пара-дигидроксибензол, бензол-1,4-диол)
— ароматическое органическое соединение,
представитель двухатомных фенолов с
химической формулой C6H4(OH)2. Легко
окисляется (восстанавливает соли серебра
на холоде). Изначально был получен из
хинона. В промышленности получается
сплавлением бензолдисульфокислоты с
едкими щелочами (с применением KI в
качестве катализатора). Применяется в
фотографии как проявляющее вещество,
в синтезе органических красителей как
антиоксидант и др. В косметических
препаратах ранее использовался как
компонент для отбеливания кожи, но в
последние годы практически всюду
запрещён из-за высокой опасности для
кожи. В качестве ингибитора реакции
свободно-радикальной полимеризации
метилметакрилата входит в состав
стоматологических композиционных
материалов химического отверждения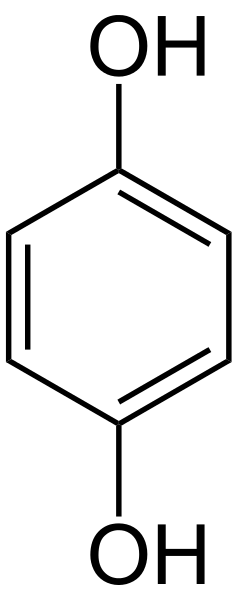
Ка́ломель Hg2Cl2 — редкий минерал из класса галогенидов, хлорид ртути(I).Каломель применяют для изготовления каломельных электродов, как катализатор органических реакций; ранее использовалась в медицине — как противомикробное средство, применяемое наружно в виде мази при заболеваниях роговицы, бленнорее, а также для предохранения от венерических заболеваний (местно). Иногда принимали внутрь как желчегонное средство. В настоящее время в медицине практически вытеснен более современными препаратами. Применялась в 19 веке. Попадая в кишечный тракт, распадается на опасные для здоровья вещества
