Травень В.Ф. - Органическая химия. В 3 т. Т. 2
..pdf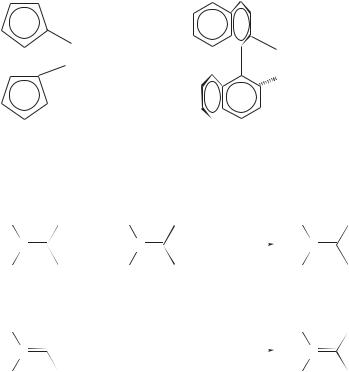
Реакции кросс-сочетания, катализируемые соединениями переходных металлов |
321 |
рости и равновесия отдельных стадий. В качестве лигандов в комплексах Pd(0), как правило, выступают фосфины. Часто это — трифенил- и три- (о-толил)фосфины. Некоторые из других фосфиновых лигандов показаны ниже.
(C6H5)2Р—CH2—CH2—Р2(C6H5)2 (dppe)
(C6H5)2Р—CH2—CH2—CH2—Р2(C6H5)2 (dppp)
(C6H5)2Р—CH2—CH2—CH2—CH2—Р2(C6H5)2 (dppb)
|
P(C6H5)2 |
P(C6H5)2 |
|
Fe |
P(C6H5)2 |
||
|
|||
|
P(C6H5)2 |
||
|
|
||
|
(dppf) |
(DINAP) |
Типичным примером реакций кросс-сочетания, катализируемых комплексами Pd(0), являются реакции сочетания галогеналкенов с реактивами Гриньяра [1] и литийорганическими соединениями [2]:
H |
|
H |
BrMg |
|
|
H |
|
H |
|
H |
||
|
|
|
|
|
|
|
|
Pd[P(C6H5)3]4 |
|
|
|
|
С |
|
С |
+ |
С |
|
С |
|
С |
|
С |
(75%) |
|
|
|
|
|
|
||||||||
С6H13 |
|
I |
H |
|
|
H |
|
С6H13 HC=СH2 |
||||
H |
|
H |
|
|
|
|
|
H |
|
H |
||
|
|
|
|
|
|
|
|
Pd[P(C6H5)3]4 |
|
|
|
|
С |
|
С |
|
+ С4H9Li |
С |
|
С |
(63%) |
||||
|
|
|
|
|||||||||
С4H9 |
|
Br |
|
С4H9 |
|
С4H9 |
||||||
|
|
|
|
|
|
|
||||||
Окислительное присоединение к Pd(0) лежит в основе ряда реакций кросс-сочетания.
Реакция Хека заключается во взаимодействии галогенаренов и галогеналкенов с алкенами в присутствии каталитических количеств Pd(0). В ряде
Реакции кросс-сочетания, катализируемые соединениями переходных металлов |
323 |
акциях кросс-сочетания с арил-, алкенил-, бензилгалогенидами и трифлатами [5–7]. Реакция протекает с сохранением конфигурации как алкенилстаннана, так и галогеналкена [8].
OSO2СF3 |
(H |
C) |
Sn |
|
|
H |
|
|
3 |
3 |
|
|
|
|
Pd[P(C6H5)3]4 |
|
|
|
|
|
|
|
|
|
+ |
|
С |
С |
|||
|
|
|
|
|
|||
|
|
|
|
|
|||
H Si(CH3)3
CH3
H
С
С Si(CH3)3
CH3H
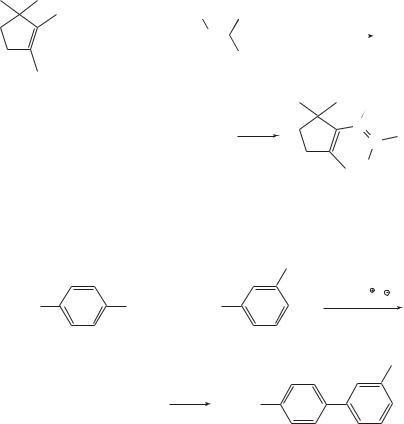
Реакция Сузуки протекает как кросс-сочетание арил- (или алкенил) борных кислот (или их производных) с галогенаренами (или галогеналкенами) или арил- (или алкенил) трифлатами [9, 10].
|
|
CF3 |
|
|
|
Pd(OCOCH3)2, |
|
H3СO |
Br + (HO)2B |
(C4H9)4NBr |
|
K2CO3 |
|||
|
|
||
|
|
CF3 |
|
|
H3СO |
(95%) |
При применении алкенов реакция протекает с сохранением конфигурации алкенильных фрагментов обоих компонентов реакции.
В целом, механизм реакции Сузуки аналогичен механизмам других реакций кросс-сочетания. Галогенарен или арилтрифлат реагируют с катализатором Pd(0) по типу окислительного присоединения. Борорганическое соединение служит источником второго органического фрагмента процесса кросс-сочетания. Дизамещенный Pd(+2)-интермедиат затем подвергается восстановительному элиминированию. Важным участником реакции является основание, задачей которого является нейтрализация кислоты, образующейся в ходе процесса, и удачный выбор которого часто определяет успех всей реакции [11].

324 |
Дополнения |
Дополнения!
ФЕМТОСЕКУНДНАЯ СПЕКТРОСКОПИЯ. МЕХАНИЗМЫ РЕАКЦИЙ В РЕАЛЬНОМ ВРЕМЕНИ
Ранее, в гл. 12, мы познакомились с возможностями молекулярной спектроскопии для целей идентификации органических веществ. В этом разделе мы узнаем, как современные спектральные методы позволяют изучать механизмы органических реакций. Последние достижения спектральной техники позволяют регистрировать процессы, происходящие в нано- (10–9), пико- (10–12) и фемто- (10–15) секундных интервалах времени. Применение соответствующих методик сделало возможным наблюдение процессов разрыва и образования ковалентных связей в режиме реального времени. Перемещения атомов при разрыве и образовании связей в реагирующих молекулах составляют всего лишь несколько ангстремов, а скорости, с которыми перемещаются атомы при их колебательных движениях, достигают 1 км/с. Необходимым разрешением, способным зарегистрировать соответ-
ствующие молекулярные движения, обладает в настоящее время лишь
фемтосекундная спектроскопия.
Втипичном фемтосекундном эксперименте на молекулы, находящиеся
ввакуумной камере, лазером направляют два импульса. Первый, более мощный импульс переводит исходные молекулы в возбужденное состояние. Второй, более слабый импульс, быстро направляемый вслед за первым, регистрирует изменения, происходящие в молекулах. Метод является универсальным. Имеются данные о его применении для изучения реакций
вгазах, жидкостях, кластерах, на поверхностях, а также в сложных биологических системах типа белков и ДНК.
Вчастности, Р. Бергман, Ч. Харрис и Х. Фрей (1997 г.) методом фемтосекундной ИК-спектроскопии наблюдали не только промежуточные соединения, но и переходные состояния каждой стадии в реакции комплекса родия с алканами в условиях комнатной температуры и атмосферного давления. Особую ценность этому наблюдению придает то обстоятельство, что аспекты механизма активирования С–Н-связей в целом весьма трудны для изучения из-за низких значений квантовых выходов.
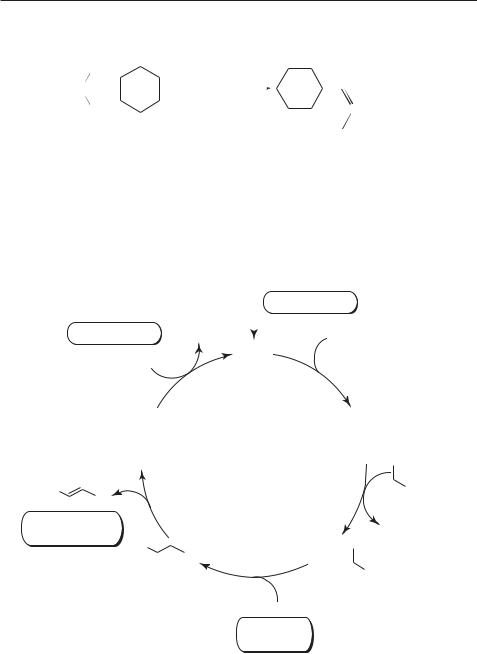
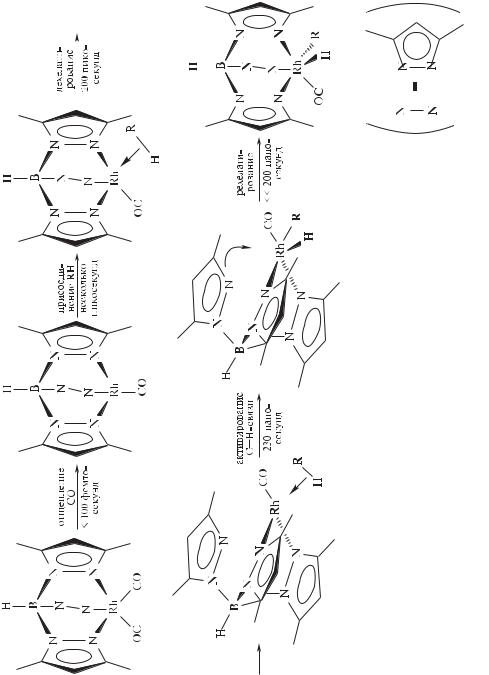
При активировании молекулы алкана комплексом родия обнаружена следующая схема превращений (рис. 15.1). На схеме под стрелками указаны интервалы времени, измеренные методом фемтосекундной ИК-спектро- скопии. Возбуждение УФ-лучами комплекса родий(I)(трипиразолилборато)дикарбонила ведет к отщеплению молекулы CO. Уже через несколько пикосекунд после этого молекула алкана включается в координационную сферу родия.
326 |
Дополнения |
Вслед за этой стадией исследователи ожидали увидеть разрыв С–Н-свя- зи в молекуле алкана. Однако, как видно из схемы, до этого одна из пиразольных групп разрывает свою связь с атомом родия. Затем следуют разрыв С–Н-связи и повторное образование связи пиразолильной группы с атомом родия.
Работа Бергмана и его коллег — лишь один из наглядных примеров, демонстрирующих принципиально новый этап в изучении механизмов химических, в том числе и органических, реакций.
Среди других работ в области фемтохимии следует упомянуть исследования А. Зевейля по наблюдению фундаментальных химических реакций в фемтосекундной шкале времени. Эти работы в 1999 г. были отмечены Нобелевской премией.

328 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Глава 16. Спирты |
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH3 |
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
OH |
|
CH |
|
CH2 |
|
CH |
|
CH3 |
OH |
|||||
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|
|
OH |
|
||||||||
2-метил-2-пропанол |
|
4-метил-2-пентанол, |
циклогексанол, |
||||||||||||||
(трет-бутиловый спирт), |
|
|
вторичный спирт |
вторичный спирт |
|||||||||||||
третичный спирт |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Далее приведены дополнительные примеры названий спиртов по номенклатуре ИЮПАК.
|
|
|
|
|
|
1 |
|
|
|
|
|
1 |
|
2 OH |
||||
|
|
|
|
CH2I CH2OH |
|
|||||||||||||
|
|
|
|
|
|
HC 3 |
|
4 Cl |
||||||||||
5 |
|
4 |
|
CH3 |
|
|||||||||||||
|
3 |
|
2 |
|
|
|
|
|
|
|
||||||||
CH3 |
|
CH2 |
|
CH |
|
CH |
|
CH |
|
CH3 |
|
|
C |
|
C |
|||
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
H |
|
H |
||||||
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2-изопропил-3-иодметил-1-пентанол |
(Z)-4-хлор-3-бутен-2-ол |
|||||||||||||||||
H OH
 1
1
2
3
HO CH2 H2C H
2' 1'
транс-3-(2'-гидроксиэтил)- 1-циклопентанол
Как видим, при нумерации атомов главной цепи гидроксигруппа имеет преимущество перед алкильными группами, атомами галогенов и кратной связью.
Вторичные и третичные спирты сложного строения называют по рациональной номенклатуре.
|
|
(C6H5)3COH |
C6H5 |
|
CH2 |
|
|
CH |
|
|
C6H5 |
|||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
трифенилкарбинол |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
OH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
бензилфенилкарбинол |
||||||||||||
|
|
|
|
CH3 |
|
|
CH3 |
|||||||||||||||
CH3 |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
C |
|
CH2 |
|
CH3 |
|
|
C |
|
CH2 |
|
CH3 |
|||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
OH |
|
|
OH |
||||||||||||||||
метилдиэтилкарбинол |
метилэтилциклогексилкарбинол |
|||||||||||||||||||||
Задача 16.1. Назовите по систематической номенклатуре следующие спирты:
a) |
OH |
б) |
CH3 |
|
|
H |
|
|
(CH3)2CH |
|
C(CH3)3 |
|
|
HO |
|
|
|
|
Задача 16.2. Напишите структурные формулы следующих соединений: а) (Z)-2-пентен-1-ол; б) 2-хлор-3-пентин-1-ол.