
Травень В.Ф. - Органическая химия. В 3 т. Т. 2
..pdf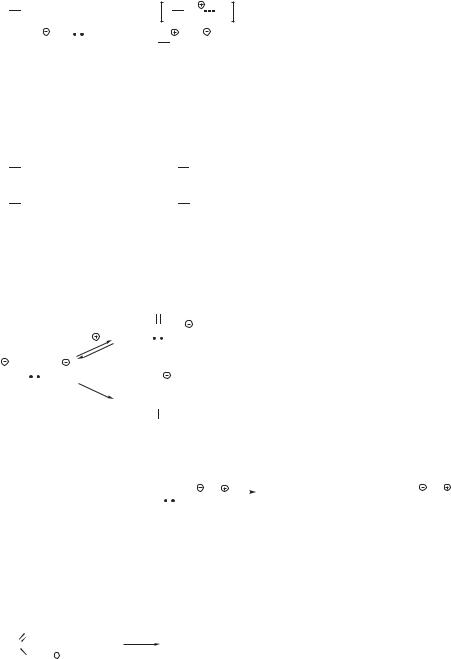
Амбидентные нуклеофилы |
251 |
го катализатора, облегчая ионизацию связи С—Br и способствуя тем самым протеканию реакции SN1 с образованием изонитрила:
R Br + Ag
 R Br Ag
R Br Ag  R
R + AgBr,
+ AgBr,
R +
+  C
C N
N  R N
R N C
C
изонитрил
В реакциях SN2 нитрит-ион и цианид-ион реагируют с субстратами своими мягкими реакционными центрами — соответственно атомами азота и углерода. В согласии с этим, применение диметилсульфоксида и диметилформамида в указанных реакциях способствует протеканию реакций SN2 с образованием нитросоединений и алкилцианидов.
R Br + NaNO2  R NO2 + NaBr
R NO2 + NaBr
нитросоединение
R Br + NaCN  R C
R C N + NaBr
N + NaBr
алкилцианид
Амбидентными являются и некоторые другие ионы, например сульфит- и гидросульфит-ионы, цианат-ион NCO. В частности, сульфит-ион протонируется по более основному центру — атому кислорода, а в реакциях с галогеналканами реакция идет по более нуклеофильному центру — атому серы.
O
|
|
|
|
|
|
|
HO |
|
S |
|
|
O |
гидросульфит-ион |
|||
|
|
|
|
|
|
|
|
|
|
|||||||
|
O |
H |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
S |
|
CH3I |
O |
|
|
||||||||||
|
|
|
|
|||||||||||||
сульфит-ион |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
O |
|
|
S |
|
|
|
O |
метансульфонат-ион |
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||||
CH3
Аналогично проявляет себя и гидросульфит-ион:
|
O |
|
|
O |
||||||||||
(CH3)2CHCH2CH2Br + HO |
|
|
|
|
|
O Na |
|
(CH3)2CHCH2CH2 |
|
|
|
|
|
O Na |
|
S |
|
S |
|||||||||||
|
|
|
|
|||||||||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
O |
|||||
|
|
|
|
|
|
|
|
3-метилбутансульфонат натрия |
||||||
Общепринятые концепции амбидентности нуклеофилов в реакциях нуклеофильного замещения у алифатического атома углерода обсуждаются в [2].
Задача 13.8. Na-соль метилсульфиновой кислоты реагирует с метилиодидом в метаноле с образованием двух изомеров. Напишите их структурные формулы.
O
CH3 |
|
S |
+ CH3I |
|
O Na
Na
252 |
Для углубленного изучения |
УЧАСТИЕ СОСЕДНИХ ГРУПП.
СОХРАНЕНИЕ КОНФИГУРАЦИИ В РЕАКЦИЯХ SN
По смешанным SN2/SN1-механизмам реагируют часто и субстраты, в которых в процессе нуклеофильного замещения возможно участие соседних групп. Речь идет о субстратах, в которых атом или группа, расположенные рядом с атакуемым атомом углерода, имеют свободную пару электронов и могут использовать эту пару, чтобы экранировать «с тыла» реакционный центр. Это экранирование обеспечивает стереоспецифичное протекание реакции. Атака субстрата нуклеофильным реагентом оказывается возможной только «спереди», что приводит к сохранению конфигурации. Такой
эффект соседней группы, проявляющийся в скоростьлимитирующей стадии, получил название анхимерное содействие [3, 4].
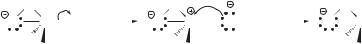
Одним из наиболее очевидных примеров анхимерного содействия является гидролиз аниона 2-бромпропаноата при низких концентрациях гидро- ксид-иона или в воде в присутствии иона серебра.
Отрицательно заряженный атом кислорода карбоксилатной группы приближается с тыльной стороны по отношению к разрывающейся связи C—Br и «выталкивает» бромид-ион. По существу, первая медленная стадия этой реакции представляет собой внутримолекулярное нуклеофильное замещение SN2 с образованием трехчленного цикла в переходном состоянии
O |
|
O |
|
O |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
медленно |
C |
быстро |
C |
||||||||||
O C |
|
Br |
O C + OH |
O C |
|
OH |
||||||||
|
|
|
|
|||||||||||
Me H |
|
Me H |
|
Me H |
||||||||||
(R)-2-бромпропаноат |
|
|
|
(R)-2-гидроксипропаноат |
||||||||||
Во второй быстрой стадии гидроксид-ион атакует атом углерода «спереди» (т. е. со стороны ушедшего бромид-иона) и раскрывает промежуточно образовавшийся «эпоксидный» цикл. При этом имеет место еще один акт реакции SN2. Сохранение конфигурации в конечном продукте — карбоксилат-ионе молочной кислоты — оказывается, таким образом, результатом двух последовательных реакций SN2, в каждой из которых конфигурация обращается.
При увеличении концентрации гидроксид-иона увеличивается доля обычной атаки «с тыла» по механизму SN2 с обращением конфигурации исходного субстрата.
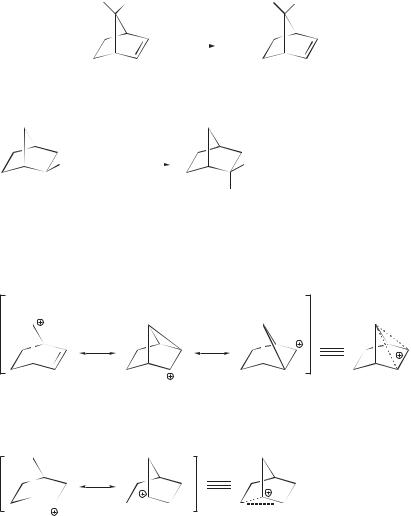
Анхимерное содействие нуклеофильному замещению способны оказывать и другие группы, ключевые нуклеофильные атомы в которых имеют НЭП. Ниже перечислены некоторые группы, способные к анхимерному содействию [3, 5].
COO , OCOR, COOR, COAr, O , OR, OH, NH2, NHR, NR2, NHCOR, S , SH, SR, I, Br, Cl.

Участие соседних групп. Сохранение конфигурации |
255 |
— ацетолиз L-трео-3-фенил-2-бутилтозилата в уксусной кислоте на 96% идет с сохранением трео-конфигурации (D и L-энантиомеры при этом образуются в равных количествах); в трифторуксусной кислоте трео-конфи- гурация сохраняется на 100%:
Me |
H |
|
Me |
H |
Ph |
|
|
||||
|
OTs |
|
|
OAc |
Me H |
Ph |
CF3COOH |
Ph |
+ |
||
|
|
|
|
|
Me H |
Me H |
|
Me |
H |
|
OAc |
|
|
|
|
|
|
L-трео-3-фенил- |
L-трео-3-фенил- |
D-трео-3-фенил- |
|||
2-бутилтозилат |
2-бутилацетат (50%) |
2-бутилацетат (50%) |
|||
 ОБРАТИТЕ ВНИМАНИЕ!
ОБРАТИТЕ ВНИМАНИЕ!
Эффекты анхимерного содействия наиболее часто проявляются в растворителях, обладающих минимальной нуклеофильностью (CH3COOH, HCOOH, CF3COOH).
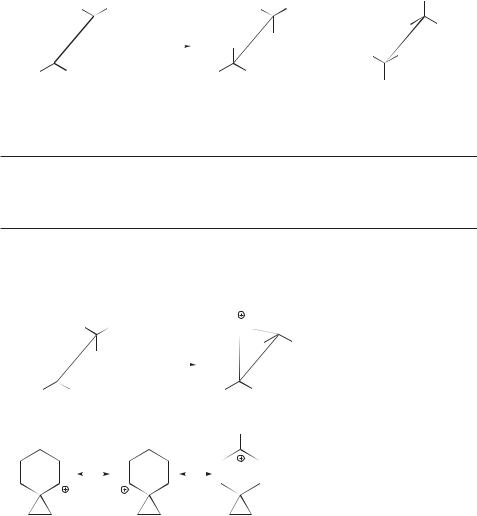
Указанные результаты получают адекватное объяснение только при предположении, что в ходе ацетолиза показанных этил- и бутилтозилатов промежуточно образуются фенониевые ионы мостиковой структуры:
Me H |
Ph |
Me H
Ph |
|
OTs |
CH3COOH |
|
|
|||||
Me |
H |
|
|
Me |
H |
|||||
X |
|
|
|
X |
X |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Соответственно этому электроотрицательные заместители Х в фениле замедляют реакцию сольволиза, затрудняя образование фенониевого иона, а электронодонорные заместители, напротив, ускоряют эту реакцию, поскольку облегчают образование циклического интермедиата [12, 13].

256 |
|
|
|
|
|
Дополнения |
Незначительное образование эритро-изомера |
||||||
|
OAc |
|
|
|
AcO |
H |
|
|
|
|
|
||
Me |
H |
|
|
|
|
Me |
Ph |
|
|
|
|
Ph |
|
|
|
|
|
|||
Me H |
|
|
|
|
Me H |
|
D-эритро-3-фенил-2-бутилацетат
при ацетолизе L-трео-3-фенил-2-бутилтозилата объясняется малым содержанием открытой формой промежуточного карбокатиона, образующегося при ионизации субстрата.
 ОБРАТИТЕ ВНИМАНИЕ!
ОБРАТИТЕ ВНИМАНИЕ!
Перегруппировки в ходе реакциий нуклеофильного замещения, протекающие с участием карбокатионных интермедиатов, в том числе и обусловленные анхимерным содействием, относят к группе перегруппировок Вагнера–Меервейна (см. т. I, гл. 4, разд. «Для углубленного изучения»).
Дополнения!
ИММУННАЯ СИСТЕМА ЖИВОГО ОРГАНИЗМА. АНТИГЕНЫ И АНТИТЕЛА
Иммунная система — важнейшая часть нормально развивающегося орга-
низма. Ее основная задача состоит в борьбе со всеми инородными телами — антигенами, попадающими в организм. Речь при этом не идет, конечно,
о продуктах питания, для переработки которых в организме имеются генетически присущие ему надежные биохимические циклы.
Антигенами следует считать самые различные структуры — от уже знакомых нам ксенобиотиков до пересаженного в результате той или иной операции постороннего органа, содержащего «чужие» клетки.
Химическим оружием иммунной системы являются антитела. Антитела — это сложные биоорганические структуры белковой природы, которые производятся иммунной системой и которые имеют каталитические свойства, определяющие способность узнавать структуру антигена, специфически связывать его и удалять из организма. Например, антитела
Иммунная система живого организма. Антигены и антитела |
257 |
образуются в организме животного в ответ на введение в него чужеродных клеток, которые в этом случае выступают в качестве антигенов. По механизму своего действия антитела похожи на ферменты.
Вместе с тем в отличие от ферментов, производимых организмом для стандартных биохимических циклов, антитела синтезируются им для отдельных специфических органических реакций как ответ на антиген, попавший в организм.
Связывание каждого антитела с его мишенью (антигеном) является высокоспецифичным. Один из способов, который был применен для изучения «работы» антител, заключается в том, чтобы вызвать иммунный ответ на структуру, специально синтезированную для имитации переходного состояния (transition state analog) некоторой модельной реакции между антителом и антигеном. При этом исследователи полагали, что если антитело производится организмом для предпочтительного связывания со стабильной молекулой, имеющей структуру, подобную переходному состоянию соответствующей реакции, то другие молекулы, способные реагировать через такое переходное состояние, должны реагировать быстрее в результате связывания с произведенным таким способом антителом. Облегчая связывание реагирующих субстратов и формирование соответствующего переходного состояния, антитело действует, таким образом, подобно ферменту. Поразительно, но изложенная схема генерации антител показала свою эффективность на многих примерах.
Химики «заставили» иммунную систему вырабатывать антитела для ряда реакций: некоторых реакций Дильса–Альдера, перегруппировок Клайзена, гидролиза сложных эфиров. Были синтезированы стабильные молекулы, которые имитировали переходные состояния перечисленных реакций. Их назвали имитаторами переходных состояний (английский термин «hapten»). Имитатор «сажали» на стандартный белок, например альбумин свиньи, и вводили его в живой организм, чтобы вызвать иммунную реакцию, после чего выделяли и изучали соответствующие вырабатываемые организмом антитела.
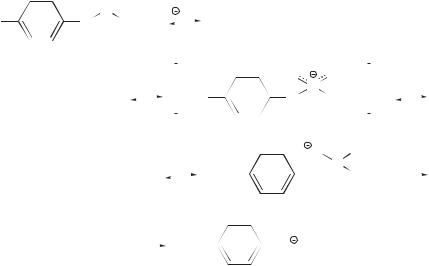
В качестве примера ниже приведены структура имитатора, моделирующего переходное состояние реакции гидролиза карбоната, и собственно реакция гидролиза, катализируемая антителом, полученным как указанно выше.
Имитатор переходного состояния:
|
|
O |
O |
||
|
|
P |
|
|
OH |
|
|
||||
O2N |
|
O |
C |
||
|
|
|
|
||
|
|
|
O |
||
258 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дополнения |
||||||
Гидролиз метил-4-нитрофенилкарбоната: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
O2N |
|
O |
OCH3 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
OH |
|
≠ |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O2N |
|
|
|
|
O |
OCH3 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
C |
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O2N |
|
|
|
|
O |
OCH3 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O + CO2 + CH3OH |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O2N |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
Вобщем, полагают, что в организме человека возможна генерация от 108 до 1012 различных антител, способных распознать от 1012 до 1014 разных молекул. Доказано, что в генерации антител важную роль играют иммуноглобулины. Антитела начинают вырабатываться, как только иммуноглобулин, связанный с мембраной клетки, «узнает» специфические структурные фрагменты антигена. Появление антигена и образование соответствующего комплекса с иммуноглобулином инициируют в клетке целый ряд биологических и биохимических процессов, которые способствуют развитию клеток, производящих антитело. В результате резко увеличивается количество этих антител в организме.
Взаключение следует отметить, что принцип имитации переходного состояния в настоящее время лежит в основе нового направления конструирования эффективных лекарственных препаратов. Это направление определяется тем, что многие имитаторы оказались пригодными к специфическому связыванию с реакционноспособными участками ферментов и коферментов. Такое связывание препятствует ферментативной активности, существенно влияет на соответствующие биохимические реакции и оказывает, в конечном счете, выраженный фармакологический эффект.
260 |
Глава 14. Галогеналкены и галогенарены |
Реакции галогенидов этой группы, в том числе галогенидов аллильного и бензильного типов, следует рассматривать как частный случай реакций галогеналканов (гл. 13).
Галогенпроизводные со связью Csp2–Х
К этой группе соединений относят винилгалогениды и галогенарены. И в тех, и в других галогенпроизводных атом галогена непосредственно связан с sp3-гибридизованным атомом углерода.
CH2=CH–Cl CH2=C–CH3 Cl–CH=CH–CH2–CH3
винилхлорид |
|
Br |
|
|
1-хлор-1-бутен |
||
|
|
2-бром-1-пропен |
|
|
|
|
|
Cl |
|
Br |
CH3 |
Br |
|||
|
|
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|
хлорбензол |
1-бромнафталин |
|
|
1-бром-2-нитробензол |
|||
Cl
4-хлортолуол
Реакции галогенидов этой группы отличаются значительным своеобразием и, в частности, крайне низкой подвижностью атома галогена в процессах нуклеофильного замещения.
14.2.СПОСОБЫ ПОЛУЧЕНИЯ
Получение аллил- и бензилгалогенидов
Галогеналкены, содержащие атомы хлора или брома у Csp3-атома в α-положе- нии к двойной связи, получают аллильным галогенированием (см. разд. 5.4.3):
CH2=CH–CH3 + Cl2 |
500 °C |
CH2=CH–CH2–Cl + HCl |
||||||||
|
|
|
||||||||
пропен |
|
|
|
|
|
|
аллилхлорид |
|||
|
|
O |
|
|
|
Br |
O |
|||
|
|
|
|
|
|
|
||||
|
+ |
N |
|
Br |
|
t° |
|
+ |
NH |
|
|
|
|
||||||||
|
|
|
CCl4 |
|
||||||
циклогексен |
O |
|
3-бром- |
O |
||||||
|
|
|
||||||||
|
|
|
|
|
циклогексен |
|||||
|
|
N-бром- |
|
|
|
|
|
сукцинимид |
||
сукцинимид

 ОБРАТИТЕ ВНИМАНИЕ!
ОБРАТИТЕ ВНИМАНИЕ! CH
CH
 C
C ОБРАТИТЕ ВНИМАНИЕ!
ОБРАТИТЕ ВНИМАНИЕ!