
- •Расчёт плотности и вязкости Задача 1
- •Решение
- •Задача 2
- •Решение
- •Задача 3
- •Решение
- •Задача 4
- •Решение
- •Задача 5
- •Решение
- •Задача 6
- •Решение
- •Гидростатическое давление Задача 7
- •Решение
- •Задача 8
- •Решение
- •Задача 9
- •Решение
- •Задача 10
- •Решение
- •Гидравлическое сопротивление трубопровода Задача 11
- •Решение
- •Задача 12
- •Решение
- •Задача 13
- •Решение
- •Местные сопротивления
- •Задача 14
- •Решение
- •Гидравлическое сопротивление теплообменника Задача 15
- •Решение
- •Местные сопротивления кожухотрубчатого теплообменника
- •Задача 16
- •Решение
- •Расчёт цетробежного насоса Задача 17
- •Решение
- •Задача 18
- •Решение
- •Задача 19
- •Решение
- •Задача 20
- •Решение
- •Работа насоса на гидравлическую сеть Задача 21
- •Решение
- •Задача 22.
- •Решение
- •Задача 23
- •Решение
- •Тепловой баланс Теплообменного аппарата Задача 25
- •Решение
- •Задача 26
- •Решение
- •Задача 27
- •Решение
- •Движущая сила процесса теплопередачи Задача 28
- •Решение
- •Задача 29
- •Решение
- •Задача 30
- •Решение
- •Задача 31
- •Решение
- •Ориентировочный расчёт теплообменника Задача 34
- •Решение
- •Задача 35
- •Решение
- •Поверочный расчёт теплообменника типа «труба в трубе» Задача 36
- •Решение
- •Поверочный расчёт пластинчатого теплообменника Задача 37
- •Решение
- •Подбор и расчёт кожухотрубчатого испарителя Задача 38
- •Решение
- •Расчёт толщины тепловой изоляции Задача 39
- •Решение
- •Задача 40
- •Решение
- •Литература
Задача 4
Определить плотность и вязкость азота, при температуре 25 °C и давление 0,2 МПа.
Решение
Молярная масса, вязкость при нормальных условиях и константа Сазерленда для газов [1, с. 513, табл. V; 2, с. 12]:
![]() ,
,
![]() ,
,
![]() .
.
Считая газ идеальным, определяем плотность через молярный объём:
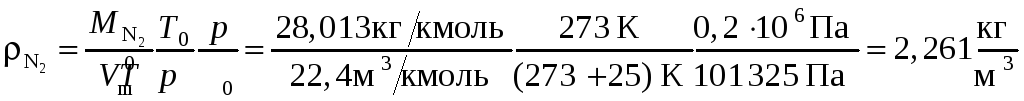 ,
,
или через универсальную газовую постоянную:
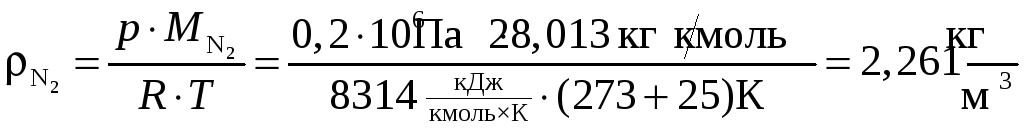 .
.
Вязкость газа рассчитываем, пренебрегая влиянием давления:
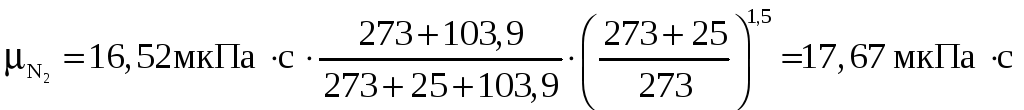 .
.
Задача 5
Определить плотность и вязкость дымовых газов, полученных при сжигании углерода. Температура дымовых газов 300°С, давление 745 мм рт. ст. Коэффициент избытка воздуха 1,2.
Решение
Уравнение реакции сгорания: С + О2 → СО2
Задаваясь количеством углерода равным 1 моль, получаем:
![]() .
.
Исходное количество кислорода с учётом коэффициента избытка:
![]() .
.
Конечное количество кислорода (за вычетом прореагировавшего):
![]() .
.
Количество азота не меняется в процессе реакции и определяется соотношением азота и кислорода в исходном воздухе:
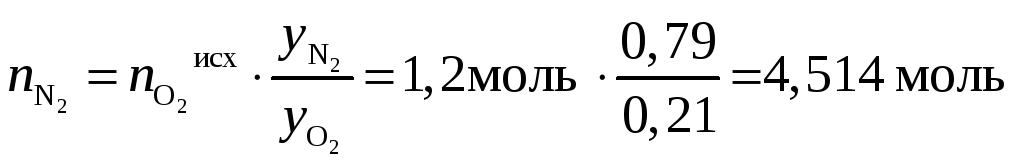 .
.
Суммарное количество вещества дымовых газов:
![]() .
.
Рассчитаем молярные (объёмные) доли компонентов дымовых газов:
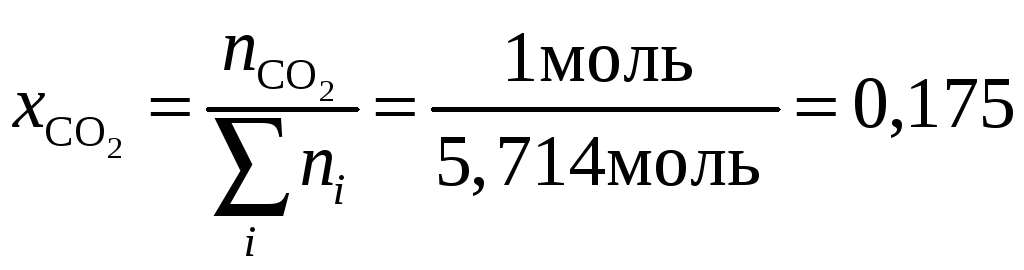 ;
;
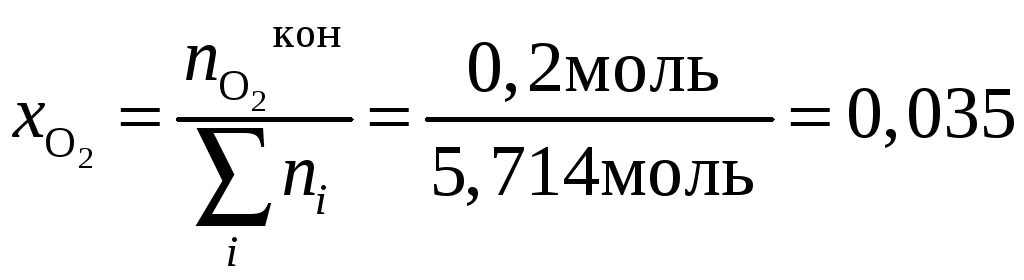 ;
;
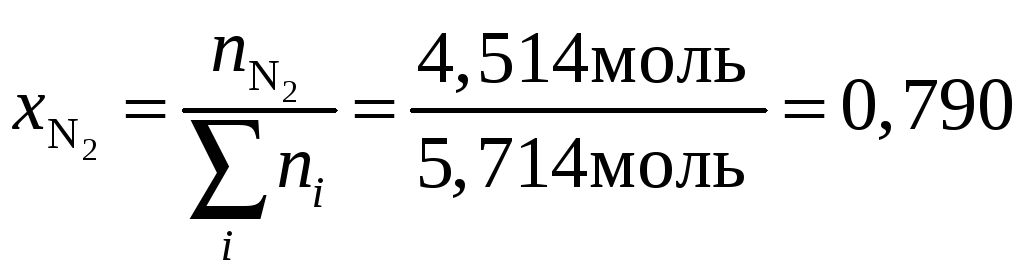 .
.
Рассчитаем молярную массу дымовых
газов:
![]()
![]() .
.
Рассчитаем плотность дымовых газов:
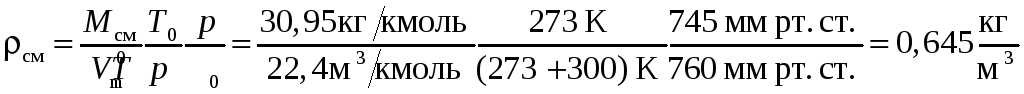 .
.
Рассчитаем вязкость компонентов:
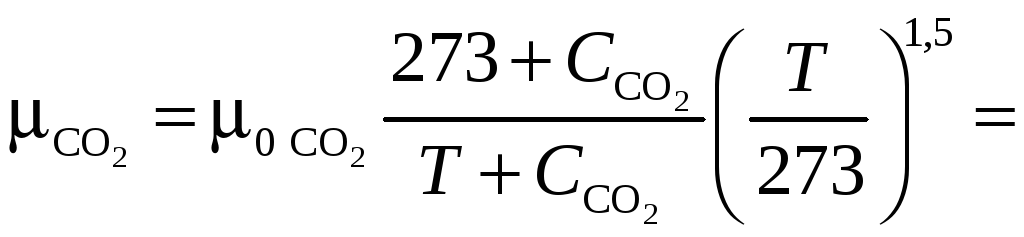
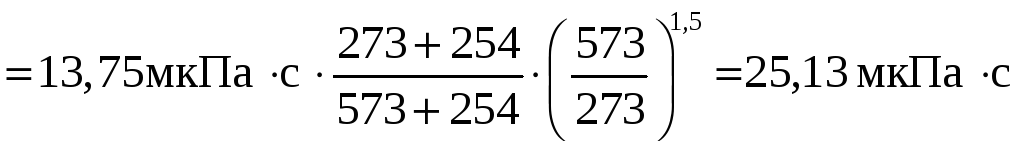 ;
;
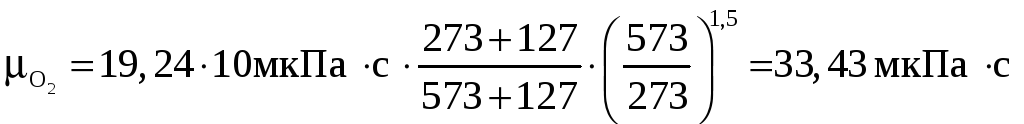 ;
;
 .
.
Значения вязкости при нормальных условиях μ0 и константы Сазерленда взяты из [2, c. 12].
Рассчитаем вязкость дымовых газов,
воспользовавшись двумя различными
формулами и сравнив полученные результаты
(значения
![]() см. [1, табл. XI]):
см. [1, табл. XI]):
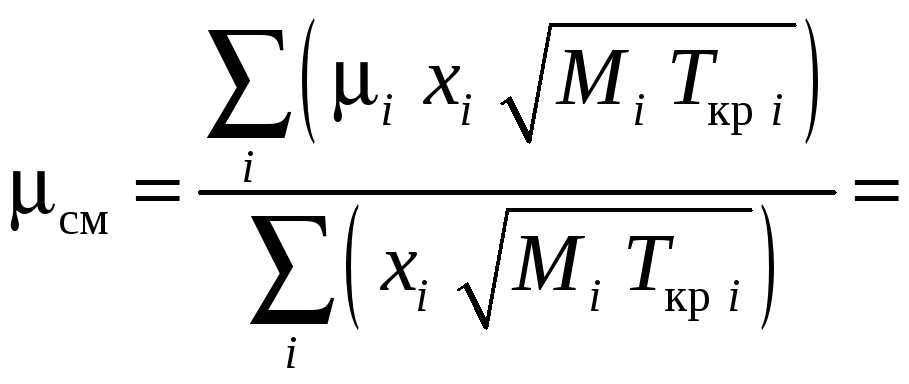
![]()
![]() ;
;


![]() .
.
Задача 6
Определить плотность и вязкость паров, полученных испарением 43 %-го (массовые %) раствора этанола. Температура паров 100°С, давление нормальное атмосферное.
Решение
Пересчитываем массовые доли в молярные:
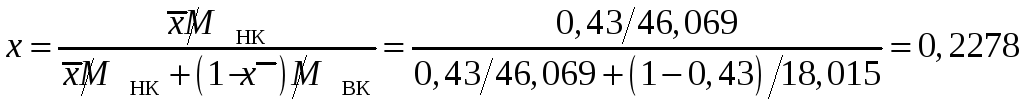 .
.
При испарении не происходит изменения массовых и молярных долей вследствие закона сохранения массы. Кроме того, для паров молярные доли являются также и объёмными, поскольку молярный объём примерно одинаков для любого газообразного вещества и зависит только от температуры и давления.
Следовательно, объёмная доля спирта в
паровой фазе:
![]() .
.
Молярная масса паровой смеси:
![]()
![]() .
.
Плотность паров:
 .
.
Вязкость паров органических веществ
при нормальном атмосферном давлении и
температуре 100 °С [2, с. 22]:
![]() .
.
Вязкость водяного пара при нормальном атмосферном давлении и температуре 100 °С:
либо находим по справочнику [3, с. 1001]
![]() ,
,
либо рассчитываем через константу Сазерленда
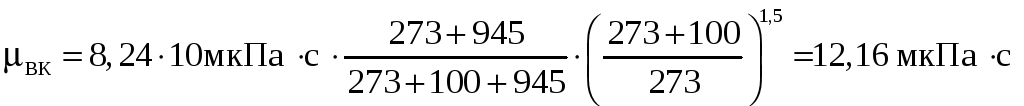
Вязкость паровой смеси:
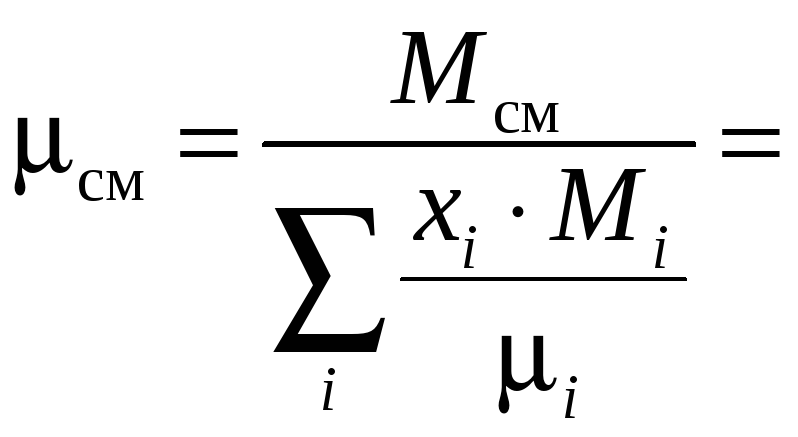
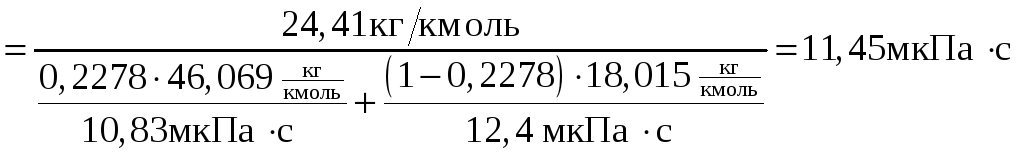 .
.
Гидростатическое давление Задача 7
Атмосферное давление составляет 750 мм рт. ст. Определите абсолютное давление в реакторе, если:
а) реактор работает под избыточным давлением, а показания установленного на реакторе манометра составляют 2 кгс/см2;
б) реактор работает под вакуумом, а показания установленного на реакторе вакуумметра составляют 500 мм рт. ст.
Решение
Соотношения между единицами измерения давления:
1 мм рт. ст. = 133,32 Па,
1 бар = 105 Па = 0,1 МПа ≈ 750 мм рт. ст.,
1 атм = 760 мм рт. ст. = 101 325 Па,
1 кгс/см2 = 1 ат = 735,6 мм рт. ст. = 98 100 Па ≈ 10 м. вод. ст.
Переводим атмосферное давление в Па:
![]() .
.
Переводим избыточное давление в реакторе и вакуум в Па:
а) ![]() ;
;
б) ![]() .
.
Рассчитываем абсолютное давление в реакторе:
а) ![]()
![]() ;
;
б) ![]()
![]() .
.
