Ответы на Билеты к Коллоквиуму № 3
.doc
|
№ 6 Острая и хроническая кровопотеря: нарушение функций и адаптивные реакции организма, их стадии; последствия, принципы терапии.
Кровопотеря — состояние, характеризующееся утратой организмом части крови. Кровопотеря является следствием кровотечения (геморрагии) — излияния крови из кровеносных сосудов и/или полостей сердца во внешнюю среду (внешнее кровотечение) или в полости организма (внутреннее, полостное кровотечение). Причины кровопотери: 1. Нарушение целостности стенок сосудов или сердца при механическом воздействии, гнойном расплавлении стенки сосудов или разрушении её растущей опухолью, разрыве стенок желудочков или предсердий в зоне инфаркта миокарда или аневризмы. 2. Значительное повышение проницаемости стенок сосудов, особенно микроциркуляторного русла. 3. снижение свёртываемости крови. Условия, влияющие на течение и исходы кровопотери: 1. Объем кровопотери (менее 20% - не опасно, 30% - значительные расстройства, более 50% - летально). 2. Скорость кровопотери. 3. Соотношение активности факторов свертывающей, противосвертывающей систем. Патогенез:
Адаптивные реакции: 1. Активацию свёртывающей системы крови и процесса тромбообразования. 2. Реакции сердечно-сосудистой компенсации кровопотери: сужение просвета резистивных сосудов, выброс крови из депо, повышение сердечного выброса. 3. Восстановление белкового состава крови— реакция белковой компенсации кровопотери. 4. Устранение дефицита форменных элементов крови вследствие активации гемопоэза — клеточная, костномозговая компенсация. 5. Активация механизмов экстренной и долговременной адаптации к гипоксии. Стадии компенсации: 1. Сердечно-сосудистая компенсация. Развивается уже в первые секунды после начала кровотечения. Стадия сердечно-сосудистой компенсация заключается в стимуляции работы сердца и в изменениях тонуса и просвета артериол. 2. Гидремическая компенсация. В первые же минуты после кровопотери активируются механизмы, обеспечивающие активацию тока жидкости из тканей в сосудистое русло. Инициальный фактор — снижение ОЦК. 3. Белковая компенсация. Реализуется благодаря активации протеосинтеза в печени и выявляется уже через несколько часов после кровотечения. 4. Клеточная компенсация – гипоксия, физико-химические изменения в тканях и биологических жидкостях (увеличение содержания Н, Na. Принципы терапии: 1. этиотропный - восстановить целостность стенки сосуда или сердца, повысить свёртываемость крови. 2. патогенетический - Для восстановления ОЦК уменьшают степень расстройств центрального и органотканевого кровообращения (переливание крови, плазмы). Для нормализации транскапиллярного обмена следует устранить или уменьшить степень расстройств микроциркуляции (вливание плазмозаменителей). Для устранения сдвигов или уменьшения степени водного, белкового и ионного дисбаланса надо вводить растворы, содержащие белки и ионы в количестве и соотношении, устраняющих их дисбаланс в организме. 3. Симптоматический принцип - мероприятия, направленные на нормализацию функций органов и их систем, нарушенных в результате кровопотери и гипоксии (ССС, дыхательная система, почки, печень). |
№ 11 Тромбогеморрагические состояния. Диссеминированное внутрисосудистое свёртывание (ДВС) крови: характеристика понятия, причины, патогенез, стадии развития, проявления, последствия, принципы терапии.
Тромбогеморрагические состояния характеризуются мозаичной (во времени и по месту преимущественной локализации в организме) сменой фазы гиперкоагуляции и тромбоза фазой гипокоагуляции, фибринолиза и геморрагического синдрома. ДВС — патогенетически сложное состояние, возникающее при различных заболеваниях и при терминальных состояниях. ДВС характеризуется рассеянным внутрисосудистым свёртыванием белков крови, агрегацией её форменных элементов, активацией и истощением компонентов свёртывающей и фибринолитической систем, блокадой сосудов микроциркуляции в органах с последующим микротромбообразованием. Причины: 1. Повреждение тканей и высвобождение ими факторов, стимулирующих гемостаз (Акушерские синдромы: преждевременная отслойка, предлежание и разрывы плаценты, эмболия околоплодными водами. Онкологические заболевания. Массивные повреждения тканей) 2. Повреждение эндотелия сосудов (запускает внутренний механизм свёртывания) — расслаивающая аневризма аорты, прогрессирующий атеросклероз сосудов. 3.Инфекции. Бактериальные токсины повреждают эндотелий. Патогенез: Массивное поступление в кровь тканевого тромбопластина активирует свёртывание белков крови и тромбоцитарный гемостаз, что приводит к множественному тромбообразованию (гиперкоагуляционная стадия ДВС-синдрома), а затем — к истощению факторов свёртывания (гипокоагуляционная стадия ДВС-синдрома). Внутрисосудистое свёртывание крови сменяется гипокоагуляцией и тяжёлым геморрагическим синдромом. Пусковой механизм ДВС-синдрома — активация коагуляционного гемостаза. Стадии: 1. Стадия гиперкоагуляции и тромбообразования - активируются оба пути свёртывания крови — внутренний, активируемый повреждением эндотелия, и внешний, запускаемый тканевыми факторами (тромбопластиноподобными веществами, продуктами протеолиза). Внутрисосудистое свёртывание белков крови (включая фибринообразование), а также адгезия и агрегация тромбоцитов приводят к возникновению микротромбов. Тромбообразование обусловливает нарушение микроциркуляции в тканях, что сопровождается развитием гипоксии и нарушением их трофики. Характерны активация свёртывающей системы крови, высвобождение прокоагулянтов и проагрегантов, повреждение клеток эндотелия, генерализованная повышенная коагуляция, образование тромбов рыхлой консистенции, формирование тромбов, фиксированных на стенках сосудов, нарастающее потребление факторов свёртывающей, противосвёртывающей и фибринолитической системы, а также тромбоцитов. 2. Стадия коагулопатии потребления: Интенсивное потребление факторов системы гемостаза; Нарастающее потребление тромбоцитов; рогрессирующая активация факторов фибринолиза. Проявления: гипофибриногенемия; снижение концентрации в крови антитромбина III; нарастание уровня продуктов деградации фибрина в крови; значительная тромбоцитопения; кровотечение из повреждённых сосудов; кровоизлияния. 3. Стадия гипокоагуляции проявляется геморрагическим синдромом. 3 основных процесса: быстрое истощение компонентов свёртывающей системы крови (протромбина и фибриногена), физиологических антикоагулянтов; снижение содержания тромбоцитов вследствие их потребления тромбами; усиленный фибринолиз. Проявления: На первой стадии – признаки полиорганной недостаточности вследствие тромбозов (цианоз, одышка, кашель, олигурия, анурия, желтуха). На гипокоагуляционной стадии ДВС выявляются петехии и экхимозы (в местах инъекций, трения одеждой), кровотечения из операционных ран, метроррагии, носовые и ЖК кровотечения, кровоизлияния в кожу, слизистые оболочки, паренхиматозные органы. В результате кровоизлияния в надпочечники может развиться острая надпочечниковая недостаточность. При выраженной кровопотере - гиповолемический шок, усугубляющий тканевую гипоксию и ацидоз. Проявления: нарушение сознания; бледные, холодные кожные покровы, их мраморность; приглушённость сердечных тонов, брадикардия. При нарастании расстройств может развиться кома. Принципы терапии: 1.Этиотропная терапия - устранение или снижение патогенного действия причинного фактора. 2. Патогенетическое лечение: коррекция гомостаза; восстановление объема крови физиологическим раствором, компонентами крови; коррекция газового состава крови; нормализация почечного кровотока. 3. Симптоматическое лечение - облегчение состояния пациента. Устраняют неприятные ощущения (болевые, психоэмоциональные), мероприятия по устранению недостаточности функции органов и физиологических систем. |
№ 12 Эритроцитозы: виды, причины, механизмы развития, проявления, последствия.
Эритроцитозы (эритремии, полицитемии) — состояния, характеризующиеся увеличением количества эритроцитов в единице объёма крови выше нормы (более 4,7*1012/л у женщин и 5,0*1012/л у мужчин). Различают первичные и вторичные эритроцитозы. К первичным эритроцитозам (самостоятельные формы болезни) относят истинную полицитемию (болезнь Вакеза) и семейные (наследуемые) формы. Среди вторичных эритроцитозов (симптомы других болезней, патологических состояний или процессов) различают абсолютные (вследствие усиления эритропоэза и/или поступления эритроцитов в сосудистое русло из костного мозга) и относительные формы. Последние могут быть гемоконцентрационными (гиповолемическими) и перераспределительными. ПЕРВИЧНЫЕ ЭРИТРОЦИТОЗЫ Наиболее часто встречается болезнь Вакеза Патогенез. В основе механизма развития эритроцитоза при болезни Вакеза лежат: • Увеличение в гемопоэтической ткани количества пролиферирующих опухолевых клеток-предшественниц миелопоэза. • Усиление миелопролиферативного процесса. Это отмечается не только в костном мозге, но также нередко в селезёнке и печени, колонизируемых клетками-предшественницами миелопоэза. Проявления. Эритремия сопровождается существенными изменениями в костном мозге, периферической крови, а также нарушениями функций ССС и других систем
Помимо болезни Вакеза, к первичным эритроцитозам относят ряд семейных наследуемых немиелопролиферативных (т.е. не обусловленных опухолевой трансформацией клеток эритроидного ряда) заболеваний с мало изученными на сегодняшний день этиологией и патогенезом. Все эти заболевания характеризуются увеличением числа эритроцитов в единице объёма крови, гиперволемией и другими признаками истинной полицитемии. ВТОРИЧНЫЕ ЭРИТРОЦИТОЗЫ Вторичные эритроцитозы — состояния, являющиеся симптомами других болезней или патологических процессов. Устранение причин этих болезней или процессов приводит к ликвидации вторичных эритроцитозов без проведения специального лечения. Вторичные эритроцитозы подразделяют на абсолютные и относительные. Вторичные абсолютные эритроцитозы Вторичные абсолютные эритроцитозы — состояния, характеризующиеся увеличением числа эритроцитов в единице объёма крови в результате активации эритропоэза и выхода избытка эритроцитов из костного мозга в сосудистое русло. Причина Непосредственная причина вторичного абсолютного эритроцитоза — повышенное образование эритропоэтина и/или повышение чувствительности к нему эритроидных клеток. Проявления
Вторичные относительные эритроцитозы Вторичные относительные эритроцитозы характеризуются увеличением количества эритроцитов в единице объёма крови без активации их продукции в костном мозге и без повышения их абсолютного числа в крови. Причины 1. Снижение объёма плазмы крови (гемоконцентрация) при потере организмом жидкости (диарея, рвота, плазморрагия при ожоговой болезни, лимфоррагия). Это обусловливает развитие полицитемической гиповолемии. 2. Выброс в циркулирующую кровь эритроцитов из органов и тканей, депонирующих их (при стресс-реакции, острой гипоксии, гиперкатехоламинемии), с развитием полицитемической гиперволемии. Проявления Повышение Ht (что свидетельствует о гемоконцентрации), нормо- или гиповолемическая полицитемия (в основном за счёт эритроцитоза), повышение вязкости крови. |
|
|
|
|
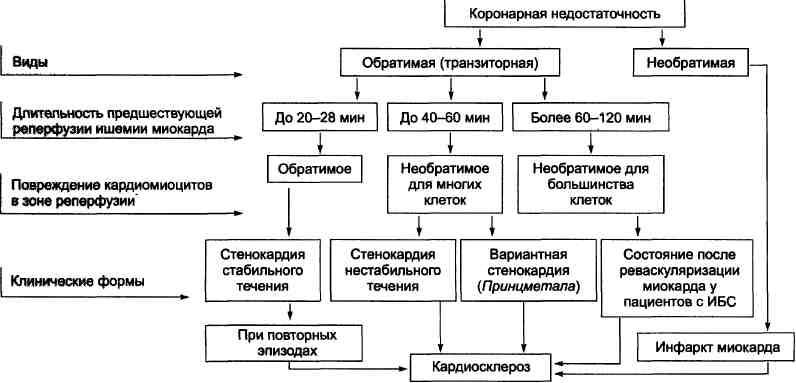
№ 13 Коронарная недостаточность: характеристика понятия, виды, причины возникновения, последствия, механизмы.
Коронарная недостаточность — типовая форма патологии сердца, характеризующаяся превышением потребности миокарда в кислороде и субстратах метаболизма над их притоком по коронарным артериям, а также нарушением оттока от миокарда продуктов обмена веществ, БАВ, ионов и других агентов. Ведущий патогенетический фактор коронарной недостаточности — ишемия миокарда. Клинически коронарная недостаточность проявляется как ишеми-ческая болезнь сердца (ИБС). При поражении венечных артерий может развиться стенокардия, инфаркт миокарда или внезапная сердечная смерть. ВИДЫ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ Все разновидности коронарной недостаточности подразделяют на обратимые и необратимые.
Обратимые нарушения коронарного кровотока. Обратимые (транзиторные) нарушения коронарного кровотока клинически проявляются различными формами стенокардии и состояниями после реперфузии (реваскуляризации) миокарда. Необратимые нарушения коронарного кровотока. Необратимое прекращение или длительное значительное уменьшение притока крови по коронарной артерии в каком-либо регионе сердца завершается, как правило, инфарктом миокарда. ПРИЧИНЫ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ Многочисленные состояния и факторы, способные вызвать коронарную недостаточность, объединяют в три основные, как правило, взаимосвязанные и взаимозависимые группы.
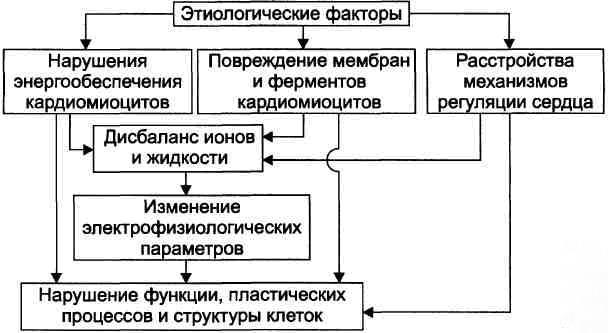
МЕХАНИЗМЫ ПОВРЕЖДЕНИЯ СЕРДЦА ПРИ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ Недостаток кислорода и субстратов обмена веществ в миокарде, а также нарушение оттока продуктов нарушенного метаболизма, ионов, БАВ в условиях коронарной недостаточности приводят к включению ряда типовых механизмов повреждения миокарда
|
№ 14 Артериальные гипертензии: характеристика понятия, виды, этиология, патогенез, проявления, осложнения, принципы лечения.
Артериальная гипертензия — состояние, при котором систолическое АД составляет 140 мм рт.ст. и выше и/или диастолическое АД 90 мм рт.ст. и выше (при условии, что эти значения получены в результате как минимум трёх измерений, произведённых в различное время на фоне спокойной обстановки, а больной за сутки до измерений не принимал ЛС, изменяющих АД). Виды
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ АРТЕРИАЛЬНЫХ ГИПЕРТЕНЗИЙ Основные факторы, определяющие уровень АД, — сердечный выброс и общее периферическое сосудистое сопротивление (ОПСС). Увеличение сердечного выброса и/или ОПСС ведёт к увеличению АД, и наоборот. В развитии артериальных гипертензий имеют значение как гуморальные и нейрогенные (ренин-ангиотензиновая система, симпатическая нервная система, баро- и хеморецепторы), так и экзогенные факторы (чрезмерное потребление поваренной соли, алкоголя, ожирение). К вазопрессорным гормонам относят ренин, ангиотензин II, вазопрессин, эндотелии. Вазодепрессорными считают натрийуретические пептиды, калликреин-кининовую систему, адреномедуллин, оксид азота, простагландины (ПгI2 — простациклин). Нейрогенные артериальные гипертензии. Эти гипертензии характеризуются либо повышением гипертензивных нейро-генных влияний, либо ослаблением гипотензивных нейрогенных эффектов, либо (чаще) сочетанием того и другого. Эти гипертензии ориентировочно составляют половину всех артериальных гипертензии. Их подразделяют на рефлекторные (рефлексогенные) и центрогенные. Эндокринные артериальные гипертензии. Эти гипертензии составляют до 1% всех артериальных гипертензии (по данным специализированных клиник — до 12%) и развиваются в результате гипертензивного эффекта ряда гормонов. Артериальные гипертензии, вызванные гипоксией органов. Артериальные гипертензии, развивающиеся в результате гипоксии органов (особенно мозга и почек), нередко встречаются в клинической практике. Они обозначаются как «гипоксические» (метаболические, органоишемические). К ним относят артериальные гипертензии, в основе патогенеза которых лежат нарушения метаболизма веществ с гипо- и гипертензивным действием. Возникают эти гипертензии в результате расстройств кровообращения и последующей гипоксии различных внутренних органов. Гипертензия артериальная вазоренальная. Вазоренальная (реноваскулярная, почечно-ишемическая) артериальная гипертензия — симптоматическая артериальная гипертензия, вызванная ишемией почки (почек) вследствие окклюзии почечных артерий. Гипертензия артериальная ренопаренхиматозная. Ренопаренхиматозная артериальная гипертензия — симптоматическая (вторичная) артериальная гипертензия, вызванная врождённым или приобретённым заболеванием почек. Гемические артериальные гапертензии. Изменения состояния крови (увеличение её массы и/или вязкости) нередко приводят к развитию артериальной гапертензии. Так, при полицитемиях (истинной и вторичных), гиперпротеинемии и других подобных состояниях в 25— 50% случаев регистрируется стойкое повышение АД. Смешанные артериальные гапертензии. Помимо указанных выше, артериальные гипертензии могут развиваться в результате одновременного включения нескольких механизмов. Например, артериальные гипертензии при повреждении мозга или развитии аллергических реакций формируются с участием нейрогенного, эндокринного и почечного патологических факторов. Лекарственные артериальные гипертензии. В патогенезе артериальной гапертензии, вызванной ЛС, могут иметь значение вазоконстрикция из-за стимуляции симпатико-адреналовой системы или прямого воздействия на ГМК кровеносных сосудов, увеличение вязкости крови, стимуляция ренин-ангиотензиновой системы, задержка ионов натрия и воды, взаимодействие с центральными регуляторными механизмами. ОСЛОЖНЕНИЯ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ К наиболее частым и опасным осложнениям артериальной гипертензии относятся инфаркт миокарда, инсульт мозга, сердечная недостаточность, почечная недостаточность, гипертоническая энцефалопатия, ретинопатия, расслаивающая аневризма аорты, гипертонический криз. ПРИНЦИПЫ ЛЕЧЕНИЯ АРТЕРИАЛЬНЫХ ГИПЕРТЕНЗИЙ План лечения артериальной гипертензии у каждого конкретного больного включает контроль АД и факторов риска, изменение образа жизни, лекарственную терапию. Немедикаментозное лечение. Немедикаментозное лечение показано всем больным. У 40—60% пациентов с начальной стадией артериальной гипертензии при невысоких значениях АД оно нормализуется без применения ЛС. При выраженной артериальной гипертензии немедикаментозная терапия в комбинации с лекарственной способствует снижению дозы принимаемых ЛС и тем самым уменьшает риск их побочного действия. Лекарственная терапия. Основные принципы лекарственного лечения формулируются в виде трёх тезисов. • Начинать лечение мягкой артериальной гипертензии необходимо с малых доз ЛС. • Следует применять комбинации препаратов для увеличения их эффективности и уменьшения побочного действия. • Нужно использовать препараты длительного действия (12—24 ч при однократном приёме). |
№ 15 Гемолитические анемии: виды, причины, патогенез, проявления, особенности картины периферической крови, принципы терапии
Гемолитические анемии — большая группа заболеваний, характеризующихся снижением средней продолжительности жизни эритроцитов (в норме 120 дней) и преобладанием интенсивности гемолиза эритроцитов в сравнении с их образованием. Гемолиз (разрушение эритроцита) может быть внесосудистым (в селезёнке, печени или костном мозге) и внутрисосудистым. Классификация гемолитических анемий. В зависимости от степени замещения разрушенных клеток новыми эритроцитами говорят о компенсированных и некомпенсированных гемолитических анемиях. Гемолитические анемии классифицируют также по этиологическомуфактору — идиопатические (причина не известна) и вторичные (например, вызванные приёмом ЛС), по форме течения — острые, подострые, хронические, по типу дефекта. Этиология гемолитических анемий. Гемолитические анемии возникают при дефектах эритроцитов (внутриклеточные факторы) либо под воздействием внешних по отношению к эритроцитам причин (внеклеточные факторы). Обычно внутриклеточные факторы — наследуемые, а внеклеточные — приобретённые. Внеклеточные факторы. Микроокружение эритроцитов представлено плазмой и эндотелием сосудов. Присутствие в плазме ауто- или изоантител, токсичных веществ или инфекционных агентов вызывает изменения стенки эритроцита, что приводит к его разрушению. Внутриклеточные факторы. Внутриклеточные дефекты включают аномалии мембран эритроцитов, НЬ или ферментов. Эти дефекты наследуемы (исключая пароксизмальную ночную гемоглобинурию). По происхождению все гемолитические анемии подразделяют на первичные (наследственные и врождённые) и на вторичные (приобретённые). Приобретённые гемолитические анемии. Причинами приобретённых (вторичных) гемолитических анемий являются многочисленные агенты физического, химического и биологического характера, вызывающие повышенный гемолиз эритроцитов. Патогенез гемолитических анемий. Общий механизм лизиса эритроцитов заключается в дезорганизации фосфолипидно-белковой структуры их мембраны.
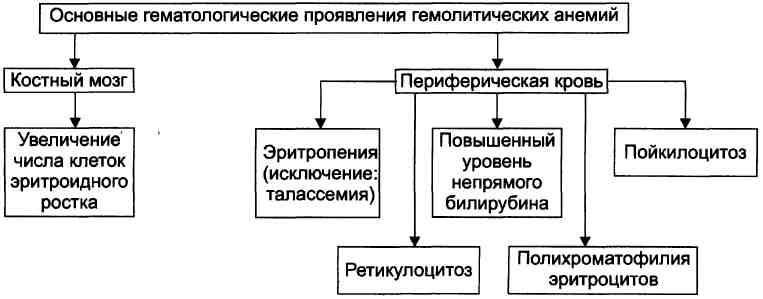
Механизмы повреждения мембраны Масштаб повреждений мембраны эритроцита может колебаться в широком диапазоне — от микроразрывов до декомпозиции макромолекул и образования пор. В двух последних случаях развивается каскад нижеперечисленных реакций. Мембранопатии. Первичные гемолитические анемии, обусловленные мемб-ранопатиями, характеризуются нарушением белково-липидной структуры и физико-химического состояния мембран эритроидных клеток. Ферментопатии. Первичные гемолитические анемии, обусловленные фермен-топатиями, характеризуются нарушением белково-липидной структуры и физико-химического состояния мембран эритроидных клеток и развиваются при генных мутациях ряда ферментов. Гемоглобинопатии. Известны сотни гемоглобинопатии, сопровождающихся проявлениями гемолитической анемии. Проявления гемолитических анемий разнообразны и в значительной степени определяются конкретным заболеванием.
Лечение гемолитических анемий Ниже приведены принципы, цели и методы лечения гемолитических анемий. Этиотропный принцип. Необходимо устранить (прекратить действие) гемолитические факторы или ввести в организм агенты, дефицит которых вызвал гемолиз эритроцитов (например, рибофлавин, глутатион, флавинат). Патогенетический принцип. При гемолитических анемиях развиваются эритропения, гемосидероз, гипоксия, нарушения КЩР. Симптоматический принцип. Для нормализации функций органов и их систем, нарушения которых были вызваны гемолизом эритроцитов и гемосидерозом, корректируют деятельность ССС, почек, печени и других органов и тканей. |
|
|
||
|
|
|
№ 16 Почечные артериальные гипертензии (вазоренальная и ренопривная): виды, их этиология и патогенез
Вазоренальная (реноваскулярная, почечно-ишемическая) артериальная гипертензия — симптоматическая артериальная гипертензия, вызванная ишемией почки (почек) вследствие окклюзии почечных артерий. Распространённость составляет 1-2% (до 4-16% по данным специализированных клиник) среди всех видов артериальных гипертензий. Из них 60-70% возникают при атеросклерозе почечных артерий, 30-40% — при фибромускулярной дисплазии, менее 1% обусловлены редкими причинами (аневризма почечной артерии, тромбоз почечных артерий, почечные артериовенозные фистулы, тромбоз почечных вен). Проявления. Клиническая картина определяется симптомами артериальной гипертензий и основного заболевания почек. Патогенез.
Ренопаренхиматозная артериальная гипертензия — симптоматическая (вторичная) артериальная гипертензия, вызванная врождённым или приобретённым заболеванием почек. Заболевания почек: двусторонние (гломерулонефрит, диабетическая не-фропатия, тубулоинтерстициальный нефрит, поликистоз) и односторонние поражения почек (пиелонефрит, опухоль, травма, одиночная киста почки, гипоплазия, туберкулёз). Наиболее частая причина — гломерулонефрит. Распространённость. Ренопаренхиматозная артериальная гипертензия составляет 2-3% (4-5% по данным специализированных клиник) среди всех видов артериальных гипертензий. Проявления определяются симптомами артериальной гипертензии и основного заболевания почек. Основные признаки этой формы артериальной гипертензии: заболевания почек в анамнезе, изменения в анализах мочи (протеинурия более 2 г/сут, цилиндрурия, гематурия, лейкоцитурия, высокая концентрация креатинина крови), УЗИ-симптомы поражения почек. Обычно изменения в анализах мочи предшествуют повышению АД. Патогенез. В патогенезе ренопаренхиматозной артериальной гипертензии имеют значение гиперволемия, гипернатриемия (из-за уменьшения количества функционирующих нефронов и активации ренин-ангиотензиновой системы), увеличение ОПСС при нормальном или сниженном сердечном выбросе.
|
№ 17 Тромбоцитозы, тромбоцитопении, тромбоцитопатии: виды, причины, механизмы развития, проявления, последствия, принципы терапии.
Тромбоцитозы — состояния, характеризующиеся увеличением числа тромбоцитов в единице объёма крови выше 320—340109/л. Виды. По механизму развития различают абсолютные и относительные тромбоцитозы, а среди последних выделяют перераспределительные и гемоконцентрационные. Абсолютные тромбоцитозы. Абсолютные (истинные, пролиферативные) тромбоцитозы характеризуются возрастанием числа тромбоцитов в крови в результате их повышенного образования. Причины. 1. Генные дефекты. Классический пример: миелопролиферативный идиопати-ческий тромбоцитоз. 2. Увеличение концентрации и/или активности стимуляторов тромбоцито-поэза: тромбоспондина, тромбопоэтина, FAT, ИЛЗ, ИЛ6, ИЛИ. 3. Опухолевая трансформация мегакариобластов под влиянием канцерогенов с последующей интенсификацией тромбоцитопоэза при гемобластозах. Относительные тромбоцитозы. Относительные (ложные, непролиферативные) тромбоцитозы не сопровождаются увеличением общего числа тромбоцитов в крови. Причины. 1. Перераспределение тромбоцитов в различных регионах сосудистого русла. 2. Гемоконцентрация — увеличение относительной массы тромбоцитов при неизменном или сниженном объёме плазмы крови. Тромбоцитопении — состояния, характеризующиеся уменьшением количества тромбоцитов в единице объёма крови ниже нормы, как правило, менее 180-150*109/л. К тромбоцитопениям относятся также самостоятельные заболевания и некоторые синдромы, сопутствующие другим болезням. Причины. Тромбоцитопении могут быть вызваны различными факторами физической, химической и биологической природы. Механизм развития. Механизм развития тромбоцитопении заключается в реализации одного или нескольких из следующих процессов: Подавление тромбоцитопоэза, Повышенное разрушение тромбоцитов, Массированное «потребление» тромбоцитов, Избыточное депонирование тромбоцитов в селезёнке. Проявления. Гиперплазия костного мозга; Гипоплазия костного мозга; Снижение содержания гликогена и активности ряда ферментов в мегакариобластах и мегакариоцитах, что уменьшает продолжительность жизни тромбоцитов; Периферическая кровь: уменьшение числа тромбоцитов и увеличение их размеров при обычно нормальном количестве эритроцитов, НЬ, лейкоцитов. При выраженном геморрагическом синдроме возможно развитие анемии; Система гемостаза. Терапия. Этиотропный принцип. Нужно прекратить (уменьшить степень) патогенное действие факторов, вызывающих тромбоцитопению. Для этого проводят спленэктомию и удаляют гемангиомы, необходимы также защита от лучистой энергии; замена вызывающих тромбоцитопению Л С, предупреждение попадания в организм веществ, обусловливающих тромбоцитопению, инактивация и элиминация противотромбоцитарных AT и др. Патогенетический принцип. Для уменьшения потребления и/или разрушения тромбоцитов, активации тромбоцитопоэза, нормализации содержания и активности в крови про- и антиагрегантов, факторов свёртывающей, противосвёртывающей и фибринолитической систем проводят трансфузию тромбоцитов, пересадку костного мозга, лимфо- и/ или плазмаферез (удаление из крови антитромбоцитарных AT и лимфоцитов), а также применяют иммунодепрессанты, антикоагулянты, антиагреганты. Симптоматический принцип. Для нормализации функций органов и их систем, нарушенных вследствие тромбоцитопений, необходимы вливания цельной крови и тромбоцитной массы, а также лечение постгеморрагических состояний. Тромбоцитопатии — состояния, характеризующиеся нарушением свойств тромбоцитов (адгезивного, агрегационного, коагуляционного) и, как правило, расстройствами гемостаза. Тромбоцитопатиям (в отличие от тромбоцитопений) свойственны стабильные, длительно сохраняющиеся функциональные, биохимические и морфологические изменения в тромбоцитах. Они наблюдаются даже при нормальном количестве тромбоцитов и не исчезают при устранении тромбоцитопении (если таковая имелась). Виды. Тромбоцитопатии подразделяют на первичные (наследственные и врождённые) и вторичные (приобретённые). • Первичные тромбоцитопатии. Развиваются при генных дефектах. • Вторичные тромбоцитопатии. Развиваются при воздействии химических и биологических факторов. Патогенез.
Проявления. Геморрагический синдром; Различные расстройства микрогемоциркуляции: изменения объёма и скорости кровотока в сосудах микроциркуляторного русла, турбулентный его характер и др.; Значительные изменения функциональных свойств тромбоцитов (адгезивного, агрегационного, прокоагуляционного); Дефекты гранул тромбоцитов: отсутствие или уменьшение их числа, нарушение высвобождения их содержимого; Отклонения от нормы размера и формы мегакариоцитов и тромбоцитов. Лечение. Этиотропный принцип. Нужно прекратить (уменьшить степень) патогенное действие факторов, вызывающих тромбоцитопатию. Патогенетический принцип. Для предотвращения (уменьшения степени) нарушений адгезивной, агрегационной и прокоагулянтной активности тромбоцитов необходимо введение проагрегантов, инъекции прокоагулянтов и/или антифибринолитических препаратов, применение веществ, стимулирующих «реакцию высвобождения», а также переливание цельной крови, тромбоцитной массы, белковых препаратов крови. Симптоматический принцип. Для нормализации функций органов и тканей, нарушенных вследствие расстройств микрогемоциркуляции, кровотечений и кровоизлияний при тромбоцитопатии, следует вводить растворы, нормализующие реологические свойства крови (плазмозаменители, плазма), останавливать кровотечение, лечить постгеморрагические состояния. |
№ 18 Гипертоническая болезнь: характеристика понятия, этиология, стадии, механизмы развития, принципы лечения.
Диагноз гипертонической болезни (эссенциальной, первичной артериальной гипертензии) устанавливают методом исключения вторичных (симптоматических) артериальных гипертензии. Определение «эссенциальная» означает, что стойко повышенное АД при гипертонической болезни составляет сущность (главное содержание) этой артериальной гипертензии. Каких-либо изменений в других органах, которые могли бы привести к артериальной гипертензии, при обычном обследовании не находят. Этиология. Основная причина: повторный, как правило, затяжной психоэмоциональный стресс. Стресс-реакция носит выраженный отрицательный эмоциональный характер. Главные факторы риска
Классификация.
Формы: пограничная, гиперадренергическая, гипергидратационная, злокачественная Патогенез. Стадия I. Инициальный фактор патогенеза гипертонической болезни — развитие невротического состояния. Характеризуется активацией центрогенного нейрогенного звена патогенеза гипертонической болезни. Центрогенный нейрогенный механизм включает: 1. Формирование корково-подкоркового комплекса устойчивого возбуждения. 2. Усиление прессорных (гипертензивных) влияний на ССС. 3. Артериолы. Происходит длительное сужение их просвета и повышение ОПСС. Уровень АД в этих условиях существенно увеличивается. 4. Венулы и вены. Симпатические нервные влияния приводят к сужению просвета ёмкостных сосудов, увеличению притока венозной крови к сердцу и в связи с этим повышению ударного и сердечного выбросов. 5. Сердце. Катехоламины реализуют свои положительные хроно- и инотропные эффекты. Это потенцирует увеличение сердечного выброса и повышение АД. 6. Реализацию действия указанных выше гуморальных агентов. 7. Нарастающая гипертрофия ГМК артериол и миокарда и развитие атеросклероза. Стадия II 1. Стабилизация АД на повышенном уровне. 2. Рефлексогенный (барорецепторный). Заключается в нарастающем снижении (или даже прекращении) афферентной депрессорной импульсации от бароре-цепторов дуги аорты, синокаротидной и других зон в адрес сосудодвигательно-го (прессорного) центра. 3. Эндокринный фактор. Характеризуется стимуляцией продукции и инкреции в кровь гормонов с гипертензивным действием. 4. Метаболический (гипоксический, органоишемический). Включает почечные гипертензивные механизмы (вазоренальный и ренопаренхиматозный) и органоишемические. Они проявляются появлением избытка БАБ с гипертензивным действием, уменьшением образования БАВ с гипотензивным эффектом. 5. Гемический. Заключается в развитии в связи с хронической гипоксией поли-цитемии (в основном за счёт значительного эритроцитоза) и повышенной вязкости крови (в связи с полицитемией и диспротеинемией). Стадия III Наиболее часто наблюдаются: 1. Выраженный атеро- и артериосклероз, приводящие к инфарктам в различных органах (наиболее часто — миокарда) и инсультам. 2. Кардиомиопатии. Одной из причин является нарушение сбалансированности роста структур миокарда — комплекс изнашивания гипертрофированного сердца. 3. Склеротическое поражение почек (первично-сморщенная почка). Это название указывает на первично-гипертензивный генез патологии почек при гипертонической болезни. 4. Дистрофические и склеротические изменения в других органах (мозге, эндокринных железах, сетчатке, сердце). План лечения артериальной гипертензии у каждого конкретного больного включает контроль АД и факторов риска, изменение образа жизни, лекарственную терапию. Лечение. Немедикаментозное лечение. Немедикаментозное лечение показано всем больным. У 40—60% пациентов с начальной стадией артериальной гипертензии при невысоких значениях АД оно нормализуется без применения ЛС. При выраженной артериальной гипертензии немедикаментозная терапия в комбинации с лекарственной способствует снижению дозы принимаемых ЛС и тем самым уменьшает риск их побочного действия. Лекарственная терапия. Основные принципы лекарственного лечения формулируются в виде трёх тезисов. • Начинать лечение мягкой артериальной гипертензии необходимо с малых доз ЛС. • Следует применять комбинации препаратов для увеличения их эффективности и уменьшения побочного действия. • Нужно использовать препараты длительного действия (12—24 ч при однократном приёме). |
|
|
||
|
|