
- •Передмова
- •Елементи спеціальної (окремої) теорії відносності
- •Основи молекулярної фізики і термодинаміки
- •Електростатика
- •Постійний електричний струм
- •Електромагнетизм
- •Механічні коливання і хвилі в пружних середовищах
- •Електромагнітні коливання і хвилі
- •Хвильова оптика
- •Квантова природа випромінювання
- •Елементи атомної фізики і квантової механіки
- •Елементи квантової статистики і фізики твердого тіла
- •Елементи фізики атомного ядра й елементарних частинок
- •Література
- •Загальні методичні вказівки
- •Відомості про наближені обчислення
- •Навчальні матеріали до розділів курсу фізики
- •1. Фізичні основи механіки Пояснення до робочої програми
- •Основні закони і формули
- •Приклади розв’язку задач
- •Контрольна робота № 1
- •Питання для самоперевірки
- •2. Молекулярна фізика і термодинаміка Пояснення до робочої програми
- •Основні закони і формули
- •Приклади розв’язку задач
- •Контрольна робота № 2
- •Питання для самоперевірки
- •3. Електростатика. Постійний струм Пояснення до робочої програми
- •Основні закони і формули
- •Приклади розв’язку задач
- •Контрольна робота № 3
- •Питання для самоперевірки
- •4. Електромагнетизм. Коливання і хвилі Пояснення до робочої програми
- •Основні закони і формули
- •Приклади розв’язку задач
- •Контрольна робота № 4
- •Питання для самоперевірки
- •5. Квантова оптика. Елементи атомної та ядерної фізики і фізики твердого тіла Пояснення до робочої програми
- •Основні закони і формули
- •Приклади розв’язку задач
- •Контрольна робота № 5
- •Питання для самоперевірки
- •Додатки
- •Одиниці фізичних величин
- •Приставки до одиниць величин
- •Деякі астрономічні величини
- •Основні фізичні константи
- •Густина речовини
- •Ефективний діаметр молекули (м)
- •Питомий опір і температурний коефіцієнт провідників
- •Діелектрична проникність
- •Показник заломлення
- •Маса й енергія спокою деяких елементарних і легких ядер
- •Робота виходу електронів з металу
- •Маси деяких ізотопів (в а.О.М.)
- •Періоди піврозпаду радіоактивних ізотопів
- •Навчальне видання
- •Рудакова Галина Олександрівна
- •Методичні вказівки та
- •Контрольні завдання з фізики
Питання для самоперевірки
Які рівняння визначають рух тіла, яке рухається з: 1)
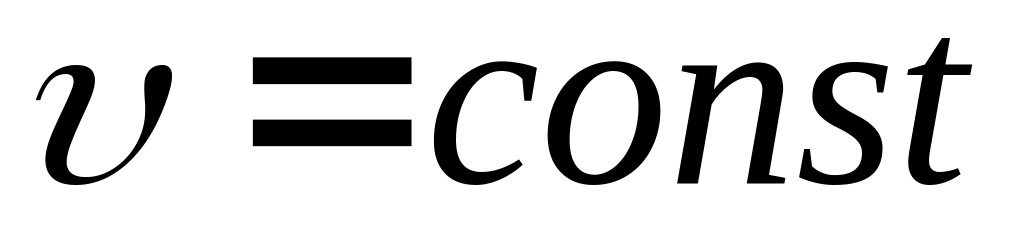 ,
2)
a
=
const.
,
2)
a
=
const.Яку зміну швидкості характеризує тангенціальне прискорення? Як визначається його чисельне значення та напрям?
Яку зміну швидкості характеризує нормальне прискорення? Його напрям та чисельне значення.
При якому русі : 1)
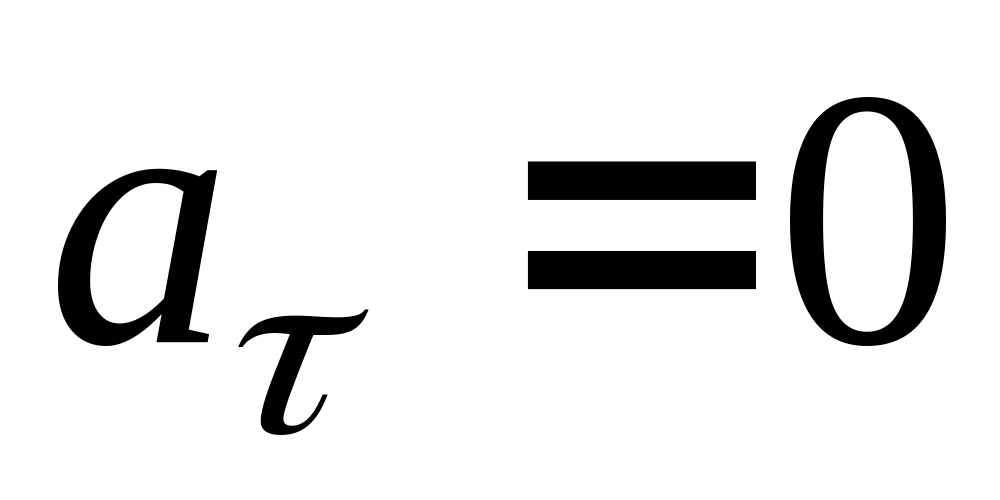 ,
,
 ;
2)
;
2)
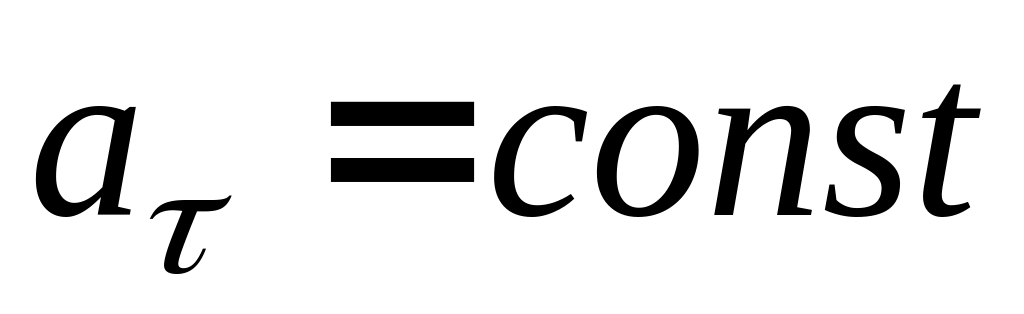 ,
;
3)
,
,
;
3)
,
 .
.Cформулюйте закони Ньютона. Як називається система відліку, у якій вони виконуються?
Дайте визначення маси, імпульсу тіла, сили. Сформулюйте принцип незалежності сил (принцип суперпозиції).
Сформулюйте закон збереження імпульсу.
Як визначається робота сталої та змінної сили? Що таке потужність? Запишіть формули для середньої та миттєвої потужності.
Яка енергія називається кінетичною? Запишіть формули для потенціальної енергії тіла у полі тяжіння Землі, а також потенціальної енергії стислої пружини. Сформулюйте закон збереження механічної енергії.
Що називається кутовою швидкістю та кутовим прискоренням? Як вони пов’язані з кінетичними характеристиками поступального руху?
Що таке момент сили, момент інерції, імпульс моменту? Сформулюйте закон збереження моменту імпульсу тіла.
Основний закон динаміки обертального руху.
Робота та кінетична енергія тіла, що обертається.
Сформулюйте закон всесвітнього тяжіння. Вага і сила тяжіння. Невагомість. Що називається першою та другою космічними швидкостями?
Сформулюйте постулати Ейнштейна. Відносність довжин і проміжків часу. Взаємозв’язок маси і енергії.
2. Молекулярна фізика і термодинаміка Пояснення до робочої програми
Приступаючи до вивчення розділу «Основи молекулярної фізики і термодинаміки», студенти повинні усвідомити, що існують два якісно різні і взаємодоповнюючі методи дослідження фізичних властивостей макроскопічних систем – статистичний (молекулярно-кінетичний) і термодинамічний. Молекулярно-кінетичний метод дослідження лежить в основі молекулярної фізики, термодинамічний – в основі термодинаміки. Молекулярно-кінетична теорія є найважливішою теорією, що дозволяє з однієї точки зору розглянути найрізноманітніші явища в усіх станах речовини, розкрити фізичну сутність цих явищ і теоретичним шляхом вивести численні закономірності, відкриті експериментально, ті, що набули великого практичного значення.
При вивченні молекулярно-кінетичної теорії слід усвідомити, що властивості величезної сукупності молекул відмінні від властивостей кожної молекули окремо, і властивості макроскопічної системи в кінцевому рахунку визначаються властивостями частинок системи, особливостями їхнього руху і середніми значеннями кінематичних характеристик руху частинок, тобто їхніми швидкостями, енергіями і т.п.
На відміну від молекулярно-кінетичної теорії, термодинаміка не вивчає конкретно молекулярні взаємодії, що відбуваються з окремими атомами або молекулами, а розглядає взаємоперетворення і зв’язок різних видів енергії, теплоти і роботи. Термодинаміка базується на двох дослідних законах, що дозволяють описувати фізичні явища, пов’язані з перетворенням енергії макроскопічним шляхом.
При вивченні основ термодинаміки студент повинен чітко засвоїти такі поняття, як термодинамічна система, термодинамічні параметри (параметри стану), рівноважний стан, рівняння стану, термодинамічний процес, внутрішня енергія, ентропія і т.д.
Контрольна робота № 2 побудована таким чином, що вона дає можливість перевірити знання студентів з основних питань цього розділу.
У задачах на тему «Основи молекулярно-кінетичної теорії» увагу приділено таким питанням програми, як рівняння Менделєєва-Клапейрона, рівняння молекулярно-кінетичної теорії, середні кінетичні енергії поступального й обертального руху молекул, середня довжина вільного пробігу й середнє число зіткнень, явища переносу.
Задачі на тему «Основи термодинаміки» охоплюють такі важливі співвідношення і поняття, як перший закон термодинаміки, внутрішня енергія, робота при різних ізопроцесах і адіабатичному процесі. Включені також задачі, що дозволяють вивчити і зрозуміти такі питання, як другий закон термодинаміки і ентропія ідеального газу, що є, на відміну від кількості теплоти, функцією стану. У роботі представлені задачі на визначення ККД циклу Карно, зміну ентропії, на рівняння Ван-дер-Ваальса, що пояснює відмінність властивостей реальних газів від ідеальних.
