
- •Вопрос 1
- •Вопрос 2
- •Вопрос 3
- •Вопрос 4
- •Вопрос 5
- •Вопрос 6
- •Вопрос 7
- •Вопрос 8
- •Вопрос 9
- •Вопрос 10
- •Вопрос 11
- •Вопрос 12
- •Вопрос 13
- •Вопрос 14
- •Вопрос 15
- •Вопрос 16
- •Вопрос 17
- •Вопрос 18
- •Вопрос 19
- •Вопрос 20
- •Вопрос 21
- •Вопрос 22
- •Вопрос 23
- •Вопрос 24
- •Вопрос 25
- •Вопрос 26
- •Вопрос 27
- •Вопрос 28
- •Вопрос 29
- •Вопрос 30
- •Вопрос 31
- •Вопрос 32
- •Вопрос 33
- •Вопрос 34
- •Вопрос 35
- •Вопрос 36
- •Вопрос 37
- •Вопрос 38
- •Вопрос 39
- •Вопрос 40
- •Вопрос 41
- •Вопрос 42
- •Вопрос 43
- •Вопрос 44
- •Вопрос 45
- •Вопрос 46
- •Вопрос 47
- •Вопрос 48
- •Вопрос 49
- •Вопрос 50
- •Вопрос 51
Вопрос 35
Химическое равновесие. Истинное (устойчивое) и кажущееся (кинетическое) равновесие, их признаки. Приведите примеры.
Равновесным называют такое состояние системы, которое не изменяется во времени, и эта неизменность не обусловлена протеканием какого-либо внешнего процесса. Равновесие остается неизменным, пока не изменяются внешние условия. Различают истинное (устойчивое) и кажущееся (кинетическое) равновесие.
Истинное равновесие сохраняется неизменным не вследствие отсутствия процессов, а в силу протекания их одновременно в двух противоположных направлениях с одинаковой скоростью. Истинное равновесие имеет следующие признаки:
1. Если нет внешнего воздействия, то система неизменна во времени.
2. Система следует за любыми изменениями во времени внешних условий, сколь угодно малыми они бы ни были, а если воздействие снято, то система возвращается в исходное состояние равновесия.
3. Состояние системы будет одинаковым независимо от того, с какой стороны она подходит к равновесию.
Кажущееся равновесие также неизменно во времени при отсутствии внешнего воздействия, однако второй и третий признаки для него не характерны. Примером системы в кажущемся равновесии является пересыщенный раствор: достаточно попадания соринки в такой р-р или встряхивания и начинается выделение из р-ра избыточного растворенного вещества.
При изменении внешних условий равновесие изменяется сообразно новым условиям, или, как говорят, «смещается».
Вопрос 36
Химическое равновесие. Принцип Ле-Шателье – Брауна и смещение равновесия. Рассмотрите на примере реакции ……
Смещение равновесия подчиняется закономерности, называемой принципом Ле-Шателье: “если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя одно из условий, определяющих состояние равновесия, то в системе усилится течение того процесса, который будет ослаблять оказываемое воздействие, а равновесие сместится в соответствующую сторону”.
Смещение равновесия:
1) Повышение температуры равновесной системы усиливает течение эндотермического процесса, охлаждение – наоборот.
2) изменение давления существенно сказывается лишь на равновесиях газовых систем. Увеличение давления для них ведет к смещению равновесия в сторону меньшего объёма, падение давления – в сторону большего объёма.
3) увеличение концентрации исх. в-в ведет к смещению равновесия вправо (в сторону продуктов).
Вопрос 37
Константа
химического равновесия. Соотношение
величин Кр и Кс для газовых
равновесий. Связь
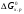 и константы равновесия.
и константы равновесия.
Равновесным называют такое состояние системы, которое не изменяется во времени, и эта неизменность не обусловлена протеканием какого-либо внешнего процесса. Равновесие остается неизменным, пока не изменяются внешние условия.
За стандартное состояние р-ров (в смысле растворенного вещества) принят р-р с активностью раств. вещества равной 1 и свойствами бесконечно разбавленного. Газ – летучесть 1, бесконечно разреженный. Это гипотетические системы.
Концентрационная зависимость энергии Гиббса k-компонента газовой смеси или р-ра имеет вид:
Gk=gk (T) + RTlnCk (идеальный р-р). Сk→ak (реальный р-р).
Gk=gk (T) + RTlnРk (идеальный газ). Рk→fk (реальный газ).
Именно ф-ции g(T) неизвестны, поэтому неизвестны абсолютные значения G. А из-за логарифмической зависимости нельзя принять за стандартное состояние нулевые значения.
Опираясь на приведенные соотношения, выведем выражение для константы равновесия. Возьмем для примера систему с идеальными газами:
ΔGхим.реакции = ∑niGi (продуктов) − ∑njGj (исх.в-в) , где ni, nj – числа молей. (коэфф. в ур.)
 ΔGхим.реакции
=
∑ni[gi
(T)
+ RTlnРi]
− ∑nj[gj
(T)
+ RTlnРj]
= ∑nigi
(T)
− ∑njgj
(T)
+ RT(∑ni.lnРi
−
∑ nj.lnРj)
= Ф(Т) + RT.
ΔGхим.реакции
=
∑ni[gi
(T)
+ RTlnРi]
− ∑nj[gj
(T)
+ RTlnРj]
= ∑nigi
(T)
− ∑njgj
(T)
+ RT(∑ni.lnРi
−
∑ nj.lnРj)
= Ф(Т) + RT. .
.
При
равн. ΔGх.р
= 0



 при данной температуре, наз. константой
равновесия. В случае реальных газов
вместо давлений будут фигурировать
фугитивности.
при данной температуре, наз. константой
равновесия. В случае реальных газов
вместо давлений будут фигурировать
фугитивности.
Аналогично
для константы равн. идеального раствора:
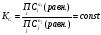 . В случае реальных растворов концентрации
должны быть заменены на активности.
. В случае реальных растворов концентрации
должны быть заменены на активности.
Для
газовых равновесий величины
Кр
и Кс
связаны:


 .
.
Выражение
энергии Гиббса имеет вид:
 (газы);
(газы);
или:
 (растворы).
(растворы).
При
стандартном состоянии Pi,
Pj,
Ci,
Cj
= 1

 .
.
