
- •Вопрос 1
- •Вопрос 2
- •Вопрос 3
- •Вопрос 4
- •Вопрос 5
- •Вопрос 6
- •Вопрос 7
- •Вопрос 8
- •Вопрос 9
- •Вопрос 10
- •Вопрос 11
- •Вопрос 12
- •Вопрос 13
- •Вопрос 14
- •Вопрос 15
- •Вопрос 16
- •Вопрос 17
- •Вопрос 18
- •Вопрос 19
- •Вопрос 20
- •Вопрос 21
- •Вопрос 22
- •Вопрос 23
- •Вопрос 24
- •Вопрос 25
- •Вопрос 26
- •Вопрос 27
- •Вопрос 28
- •Вопрос 29
- •Вопрос 30
- •Вопрос 31
- •Вопрос 32
- •Вопрос 33
- •Вопрос 34
- •Вопрос 35
- •Вопрос 36
- •Вопрос 37
- •Вопрос 38
- •Вопрос 39
- •Вопрос 40
- •Вопрос 41
- •Вопрос 42
- •Вопрос 43
- •Вопрос 44
- •Вопрос 45
- •Вопрос 46
- •Вопрос 47
- •Вопрос 48
- •Вопрос 49
- •Вопрос 50
- •Вопрос 51
Вопрос 29
Закон Гесса, условия его выполнения. Энтальпии образовании, сгорания, атомизации (определение).
Закон Гесса: энтальпия (внутренняя энергия) химической реакции не зависит от пути перехода от начальных веществ к продуктам реакции, а определяется только видом и состоянием этих исходных веществ и продуктов.
Закон Гесса справедлив для хим. процессов, происходящих при V = const или при Р = const. Предполагается также, Т = const и что система не совершает никакой работы, кроме работы против внешнего давления, связанной с изменением объёма при Р = const.
Энтальпия образования – энтальпию процесса образования 1 моль данного вещества из простых в-в при данной температуре. При этом безразлично – осуществим процесс или нет. Обозначение: ΔНобр.
Энтальпия сгорания – это энтальпия сгорания 1 моль данного вещества при данной температуре с образованием СО2(г) и Н2О(ж); состав остальных в-в указывают специально.
Энтальпия атомизации или энергия ионизации – это наименьшая энергия, необходимая для удаления электрона от свободного атома в его низшем энергетическом (основном) состоянии на бесконечность.
Вопрос 30
Закон Гесса. Следствия из закона Гесса. При каких условиях выполняется этот закон?
Закон Гесса: энтальпия (внутренняя энергия) химической реакции не зависит от пути перехода от начальных веществ к продуктам реакции, а определяется только видом и состоянием этих исходных веществ и продуктов.
Закон Гесса справедлив для хим. процессов, происходящих при V = const или при Р = const. Предполагается также, Т = const и что система не совершает никакой работы, кроме работы против внешнего давления, связанной с изменением объёма при Р = const.
Следствия из закона Гесса:
Следствие
1.
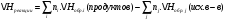 , где ni
и nj
– числа молей (коэффициенты в уравнении).
, где ni
и nj
– числа молей (коэффициенты в уравнении).
Следствие
2.
 , где ni
и nj
– числа молей (коэффициенты в уравнении).
, где ni
и nj
– числа молей (коэффициенты в уравнении).
Следствие 3. ∆Нпрямого процесса = −∆Нобратного порцесса
Стандартная энтальпия химической реакции равна разности стандартных энтальпий образования продуктов реакции и реагентов (с учетом стехиометрических коэффициентов).
Вопрос 31
Стандартные термодинамические характеристики. Понятие о стандартном состоянии индивидуальных жидких и кристаллических в-в, газов и растворов. Закон Гесса.
Раздел химии, занимающийся изучением тепловых эффектов процессов – термохимия.
Закон Гесса: энтальпия (внутренняя энергия) химической реакции не зависит от пути перехода от начальных веществ к продуктам реакции, а определяется только видом и состоянием этих исходных веществ и продуктов.
Особое значение имеют стандартные величины, т.е. такими, где все участники процесса находятся в стандартных состояниях. Для индивидуальных жидких и кристаллических в-в за стандартное состояние принимают реальное состояние этого вещества при данной т-ре и давлении 1 атм.
Со станд. состоянием газов и жидкостей (р-ры несколько сложнее), эти понятия восходят к понятиям “идеальный газ” и “идеальный р-р”. Любой идеальный газ описывается уравнением pV = vRT. Для каждого реального газа уравнение состояния своё и его крайне сложно установить. Поэтому все проблемы отклонения св-в реальных газов от идеальных “прячут” в эффективную величину f (аналог давления). Этот путь используют для реальных газов fV=vRT. Фугитивностью (летучестью) называют такую величину, которая связана с другими термодинамическими характеристиками реального газа так же, как с ним связано давление в случае идеального газа.
За стандартное состояние газообр. вещества принимают состояние гипотетически идеального газа, летучесть которого равна единице, а энтальпии реального газа при той же температуре и давлении, стремящейся к нулю. Т.е. за станд. сост. принимается бесконечно разряженный газ.
Та же самая ситуация и с растворами, только вместо летучести берут активность, которая связана с другими хар-ками реального р-ра так, как связана с ними концентрация в случае идеального ра-ра.
Осталась одна проблема – аллотропные модификации. Какую из них брать за стандарт? Берут наиболее устойчивую форму, искл.: фосфор берут белый, а не более устойчивый красный, т.к. он более реактивный; S (к.ромб.), а не S (к. моноклин.); С (к. графит), а не С (к. алмаз). Если все участники процесса наход. в стандарт. состоянии, тогда реакция – стандартная и обозначается верхним правым “ноликом”.
