
- •Вопрос 1
- •Вопрос 2
- •Вопрос 3
- •Вопрос 4
- •Вопрос 5
- •Вопрос 6
- •Вопрос 7
- •Вопрос 8
- •Вопрос 9
- •Вопрос 10
- •Вопрос 11
- •Вопрос 12
- •Вопрос 13
- •Вопрос 14
- •Вопрос 15
- •Вопрос 16
- •Вопрос 17
- •Вопрос 18
- •Вопрос 19
- •Вопрос 20
- •Вопрос 21
- •Вопрос 22
- •Вопрос 23
- •Вопрос 24
- •Вопрос 25
- •Вопрос 26
- •Вопрос 27
- •Вопрос 28
- •Вопрос 29
- •Вопрос 30
- •Вопрос 31
- •Вопрос 32
- •Вопрос 33
- •Вопрос 34
- •Вопрос 35
- •Вопрос 36
- •Вопрос 37
- •Вопрос 38
- •Вопрос 39
- •Вопрос 40
- •Вопрос 41
- •Вопрос 42
- •Вопрос 43
- •Вопрос 44
- •Вопрос 45
- •Вопрос 46
- •Вопрос 47
- •Вопрос 48
- •Вопрос 49
- •Вопрос 50
- •Вопрос 51
Список теоретических Вопросов к экзамену
Вопрос 1

 Свойства
волновой функции. Понятие об уравнении
Шредингера. Квантовые числа как
характеристики состояния электрона в
атоме. Напишите значения квантовых
чисел для каждого из d-электронов
атома … в основном состоянии.
Свойства
волновой функции. Понятие об уравнении
Шредингера. Квантовые числа как
характеристики состояния электрона в
атоме. Напишите значения квантовых
чисел для каждого из d-электронов
атома … в основном состоянии.
Законы движения микрочастиц в квантовой механике выражают волновым уравнением Шредингера. Как и законы Ньютона, это уравнение невозможно вывести из каких-либо более фундаментальных положений. Оно было получено Шредингером на основании анализа аналогии между закономерностями классической механики и оптики.
Уравнение Шредингера явл. дифференциальным уравнением второго порядка в частных производных. Для стационарного состояния одной частицы массой m оно имеет вид:
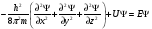 ,
,
где: h – постоянная Планка; Ψ – переменная величина; U – потенциальная энергия частицы; Е – полная энергия частицы; x, y, z – координаты.
Часто
уравнение Шредингера записывают в
компактной форме:
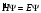 ,
где
,
где
 - оператор полной энергии или оператор
Гамильтона (гамильтониан), он обозначает
все те математические действия, которые
производят в левой части над величиной
Ψ.
- оператор полной энергии или оператор
Гамильтона (гамильтониан), он обозначает
все те математические действия, которые
производят в левой части над величиной
Ψ.
Переменная Ψ называется волновой функцией. Её Ψ2 имеет определенный физ. смысл: Ψ2.dv = вероятности рассматриваемой частицы в элементе объёма dv. Величина Ψ2 наз. плотностью вероятности, или электронной вероятности.
Ψ должна быть конечной, непрерывной, однозначной, и обращаться в нуль в тех местах пространства, где частица не может находиться.
Ψ – функция зависит не только от трех координат, но и от трех целочисленных параметров, названных квантовыми числами. Их обозначение n, l и ml .
n – главное квантовое число в значительной степени определяет значение энергии электрона в атоме и размеры электронного облака. Оно принимает значения от +1→+∞. С ростом n возрастают размеры электронного облака и энергия электронов. Кроме цифрового обозначения n используется и буквенная индексация: n=1↔K, n=2↔L, n=3↔M, n=4↔N, ….
l – орбитальное (побочное) кв. число, характеризует энергию электрона внутри слоя и определяет форму электронного облака. Оно принимает значения от 0→+(n−1). На практике l чаще обозначается буквами: l=0↔s, l=1↔p, l=2↔d, l=3↔f, l=4↔g, …, l=n−1.
ml − магнитное кв. число, определяет ориентацию орбитали в пространстве. Орбиталь же образуется совокупностью электронов с одним и тем же значением магнитного квантового числа, её традиционно обозначают □. При данном значении l, ml принимает значения: 0, ±1→±l . Общее число значений ml : (2l+1).
У
электрона есть и 4-ая кв. характеристика
– спинное кв. число ms,
отражающее 4-ую координату нашего мира
– время. ms
принимает (в единицах атомного мира)
два значения:
 .
Договоримся считать
.
Договоримся считать
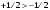 и будем обозначать электроны с
и будем обозначать электроны с
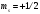 ↑,
↑,
 ↓.
↓.
Принцип Паули: в атоме не может быть двух электронов с одинаковым набором 4-х квантовых чисел.
Правило Хунда: суммарный спин электронов оболочки должен быть максимальным.
Вопрос 2
Свойства волновой функции Понятие об уравнении Шредингера. Что такое узловые поверхности? Охарактеризуйте квантовыми числами следующее состояние электронов (в основном состоянии): ….
Узловой
поверхностей
орбитали наз. геометрическое место
точек, где волновая функции
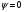 (
(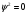 ).
Узловые поверхности могут быть
сферическими, плоскими и коническими.
По определению каждая орбиталь имеет
сферическую узловую поверхность с
бесконечным радиусом. Главное кв. число
равно общему числу узловых поверхностей
данной орбитали.
).
Узловые поверхности могут быть
сферическими, плоскими и коническими.
По определению каждая орбиталь имеет
сферическую узловую поверхность с
бесконечным радиусом. Главное кв. число
равно общему числу узловых поверхностей
данной орбитали.
