- •Билет n1
- •1.Кинематические характеристики
- •Билет №2
- •Билет № 3
- •Билет №4
- •1.Сила трения
- •Сила упругости
- •Сила тяжести и ускорение свободного падения
- •Вес тела.
- •2. .Статистическое распределение Максвелла для молекул газа по скоростям и энергиям их хаотического движения
- •Билет №5
- •1.Уравнение движения тела с переменной массой. Реактивное движение.
- •2.Распределение Больцмана.
- •Билет n6
- •1.Работа и мощность. Коэффициент полезного действия. Кинетическая энергия. Консервативные силы. Потенциальная энергия.
- •Работа при вращательном движении:
- •2.Энтропия и термодинамическая вероятность
- •Билет n7
- •Билет №8
- •2) Среднее число столкновений и средняя длина свободного пробега молекул
- •Билет n9
- •Билет n10
- •Билет n11
- •Билет n12
- •Билет №13
- •1. Дифференциальное уравнение затухающих колебаний. Коэффициент затухания. Логарифмический коэффициент затухания.
- •2.Адиабатический процесс Политропические процессы.
- •Билет n14
- •Билет n15
- •Билет №16
- •Экзаменационный билет №17.
- •1.Вынужденные колебания. Дифференциальное уравнение вынужденных колебаний. Резонанс.
- •2.Диффузия. Закон Фика. Коэффициент диффузии.
- •Билет n18
- •Билет n19
- •Билет n20
- •1.Корпускулярно – волновой дуализм. Гипотеза де-Бройля. Дифракция электронов.
- •2.Идеальная жидкость. Уравнение Бернулли.
- •21. 1. Уравнение Шредингера. Волновая ф-ция и ее физический смысл.
- •Билет №22.
- •1.Частица в одномерной прямоугольной яме. Стационарные состояния. Туннельный эффект.
- •2.Основное уравнение мкт. Уравнение состояния идеального газа Закон Дальтона.
- •Билет №23.
- •1.Постулаты теории относительности. Преобразования Лоренца.
- •2.Фазовые переходы первого рода. Фазовые диаграммы. Тройная точка. Уравнение Клапейрона Клаузиуса.
- •Билет n24
- •1.Поверхностное натяжение. Давление под изогнутой поверхностью жидкости
- •2.Неинерциальные системы отсчета. Силы инерции.
- •Билет n25
Билет n10
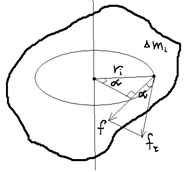
1)Рассмотрим вращение тв. тела под действием силы F:
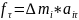
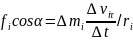
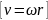
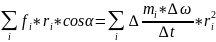
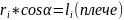
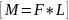
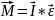
2)Термодинамика-раздел физики, в котором изучаются явления с энергетической точки зрения.Теплота-микроскопический способ передачи эн-ии.
1-ое начало термодинамики: тепло, полученное системой , идет на изменение его внутренней энергии
Тепло идет на изменение внутренней энергии системы и на совершение работы над телами
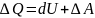
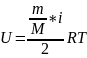
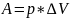
Невозможно построить вечный двигатель первого рода.(двигатель, который совершал бы работу большую, чем кол-во затраченного тепла)
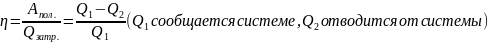
Теплоемкость системы-кол. теплоты, кот. нужно сообщить телу либо системе , чтобы его t изм. на 1 С.
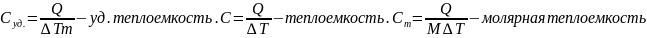
Билет n11
1. Кинетическая энергия тела, движущегося произвольным образом, равна сумме кинетических энергий всех n материальных точек па которые это тело можно разбить:
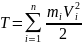 .
.
Если тело вращается вокруг неподвижной оси с угловой скоростью w , то линейная скорость i-ой точки равна
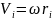 ,
где
,
где
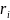 ,
- расстояние от этой точки до оси вращения.
,
- расстояние от этой точки до оси вращения.
Следовательно:
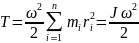 ,
где J-
момент инерции тела относительно оси
вращения. В общем случае движение
твердого тела можно представить в виде
суммы двух движений - поступательного
со скоростью, равной скорости
,
где J-
момент инерции тела относительно оси
вращения. В общем случае движение
твердого тела можно представить в виде
суммы двух движений - поступательного
со скоростью, равной скорости
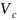 центра инерции тела, и вращения с угловой
скоростью ω вокруг мгновенной оси,
проходящей через центр инерции. При
этом выражение для кинетической энергии
тела преобразуется к виду
центра инерции тела, и вращения с угловой
скоростью ω вокруг мгновенной оси,
проходящей через центр инерции. При
этом выражение для кинетической энергии
тела преобразуется к виду
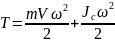 ,
где
,
где
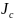 - момент инерции тела относительно
мгновенной оси вращения, проходящей
через центр инерции.
- момент инерции тела относительно
мгновенной оси вращения, проходящей
через центр инерции.
За
время dt
вращающееся тело совершит работу dA,
равную произведению момента силы M
на угол поворота
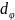 ,
сделанный радиусом этого тела, то есть
dA=M
.
Работу,
совершенную вращающимся телом за единицу
времени, называют мощностью вращающегося
тела N,
то есть
,
сделанный радиусом этого тела, то есть
dA=M
.
Работу,
совершенную вращающимся телом за единицу
времени, называют мощностью вращающегося
тела N,
то есть
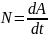 ,
,
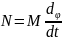 ,
где
,
где
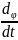 – мгновенное значение угловой скорости
ω.
Поэтому
N=Mω.
– мгновенное значение угловой скорости
ω.
Поэтому
N=Mω.
2. .Адиабатический процесс - это такое изменение состояний газа, при котором он не отдает и не поглощает извне теплоты. Следовательно, адиабатический процесс характеризуется отсутствием теплообмена газа с окружающей средой. Адиабатическими можно считать быстро протекающие процессы. Так как передачи теплоты при адиабатическом процессе не происходит, то уравнение I начала термодинамики принимает вид:
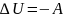 ,
где
∆U-изменение
внутренней энергии тела, A-работа,
совершаемая системой. Внешняя работа
газа может производиться вследствие
изменения его внутренней энергии.
Адиабатное расширение газа (dV>0)
сопровождается положительной внешней
работой, но при этом внутренняя энергия
уменьшается и газ охлаждается (dT<0).
Изменения энтропии S системы в обратимом
адиабатическом процессе вследствие
передачи тепла через границы системы
не происходит:
,
где
∆U-изменение
внутренней энергии тела, A-работа,
совершаемая системой. Внешняя работа
газа может производиться вследствие
изменения его внутренней энергии.
Адиабатное расширение газа (dV>0)
сопровождается положительной внешней
работой, но при этом внутренняя энергия
уменьшается и газ охлаждается (dT<0).
Изменения энтропии S системы в обратимом
адиабатическом процессе вследствие
передачи тепла через границы системы
не происходит:
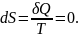 Здесь T-температура
системы, δQ-теплота,
полученная системой. Благодаря этому
адиабатический процесс может быть
составной частью обратимого цикла.Работа
газа при адиабатическом процессе равна:
Здесь T-температура
системы, δQ-теплота,
полученная системой. Благодаря этому
адиабатический процесс может быть
составной частью обратимого цикла.Работа
газа при адиабатическом процессе равна:
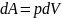 ,где
p-давление
газа, dV-малое
приращение объема. Основное уравнение
термодинамики примет вид: dU=-pdV.
Уравнение Пуассона для идеального
газа:
,где
p-давление
газа, dV-малое
приращение объема. Основное уравнение
термодинамики примет вид: dU=-pdV.
Уравнение Пуассона для идеального
газа:
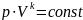 ,где
V-объем
газа,
,где
V-объем
газа,
 -показатель
адиабаты,
-показатель
адиабаты,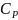 и
и
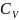 -теплоёмкости
газа соответственно при постоянном
давлении и постоянном объёме. С учётом
уравнения состояния идеального газа
уравнение адиабаты может быть преобразовано
к виду:
-теплоёмкости
газа соответственно при постоянном
давлении и постоянном объёме. С учётом
уравнения состояния идеального газа
уравнение адиабаты может быть преобразовано
к виду:
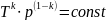 ,где
T-абсолютная
температура газа. Или к виду:
,где
T-абсолютная
температура газа. Или к виду:
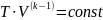 .
Поскольку k
всегда больше 1, из последнего уравнения
следует, что при адиабатическом сжатии
(то есть при уменьшении V)
газ нагревается (T
возрастает), а при расширении —
охлаждается, что всегда верно и для
реальных газов. Нагревание при сжатии
больше для того газа, у которого больше
коэффициент k.При
адиабатическом процессе показатель
адиабаты равен
.
Поскольку k
всегда больше 1, из последнего уравнения
следует, что при адиабатическом сжатии
(то есть при уменьшении V)
газ нагревается (T
возрастает), а при расширении —
охлаждается, что всегда верно и для
реальных газов. Нагревание при сжатии
больше для того газа, у которого больше
коэффициент k.При
адиабатическом процессе показатель
адиабаты равен
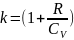 .
3.Задача:В
закрытом сосуде находится 20г азота и
32г кислорода. Найти изменение внутренней
энергии этой смеси при охлаждении её
на 280.
.
3.Задача:В
закрытом сосуде находится 20г азота и
32г кислорода. Найти изменение внутренней
энергии этой смеси при охлаждении её
на 280.