
- •Э. Т. Крутько
- •Пленкообразующих веществ
- •Предисловие
- •Введение
- •Часть первая теоретические основы химической технологии пленкообразующих
- •Глава 1. Молекулярная структура и основные свойства пленкообразующих веществ
- •Надмолекулярные структуры
- •Глава 2. Реакции образования пленкообразующих полимеров
- •2.1. Радикальная полимеризация
- •1 Без добавок; 2 0,1% бензохинона (ингибитор); 3 0,2% нитробензола (ингибитор); 4 0,5% нитробензола (замедлитель)
- •2.2. Ионная полимеризация
- •2.3. Стереоспецифическая полимеризация
- •2.4. Сополимеризация
- •2.5. Ступенчатая полимеризация и поликонденсация
- •2.6. Молекулярная масса полимеров. Понятие о молекулярно-массовом распределении
- •2.7. Химические реакции полимеров и возможности химической модификации
- •2.8. Полимераналогичные и внутримолекулярные превращения
- •2.9. Межмолекулярные реакции полимеров. Образование сетчатых («сшитых») структур
- •Глава 3. Физические состояния пленкообразующих полимеров при нанесении покрытий
- •3.1. Агрегатные и фазовые состояния полимеров
- •Аморфное состояние
- •Кристаллическое состояние
- •3.2. Реология растворов и расплавов пленкообразователей
- •Влияние температуры на вязкость расплавов и растворов полимеров. Энергия активации вязкого течения
- •Энергия активации течения.
- •Методы измерения вязкостных свойств концентрированных растворов и расплавов полимеров. Структура концентрированных растворов и расплавов полимеров
- •Метод капиллярной вискозиметрии
- •Методы ротационной вискозиметрии
- •Метод падающего шарика
- •Метод сдвига параллельных плоскостей
- •3.3. Термомеханический метод изучения физических состояний пленкообразователей
- •1 Гибкая нить; 2 жесткая нить; 3 жесткая проволока
- •Глава 4. Теоретические основы пленкообразования
- •4.1. Общие сведения о пленкообразовании
- •4.2. Пленкообразование, осуществляемое без химических превращений
- •4.2.1. Формирование покрытий из растворов пленкообразующих Особенности свойств растворов полимеров
- •Химическое строение полимера и его способность к растворению
- •Характеристика процесса
- •I испарение из жидкой пленки, контролируемое поверхностными явлениями;
- •II испарение из сформировавшейся твердой пленки, определяемое диффузионными процессами в массе полимерного материала
- •Влияние условий пленкообразования на свойства покрытий
- •4.2.2. Формирование покрытий из водных дисперсий полимеров
- •Характеристика процесса
- •Условия пленкообразования
- •Свойства покрытий
- •4.2.З. Формирование покрытий из органодисперсий полимеров
- •4.2.4. Формирование покрытий из порошковых пленкообразователей
- •Характеристика процесса
- •4.3. Пленкообразование, осуществляемое в результате химических превращений
- •4.3 1. Полимеризация на поверхности субстрата Характеристика процесса
- •Способы проведения процесса
- •4.3.2. Поликонденсация на поверхности субстрата
- •4.4. Структурные превращения пленкообразователей в процессе формирования покрытий
- •Структура покрытий из аморфных полимеров
- •Структура покрытий из кристаллических полимеров
- •Надмолекулярная структура.
- •Часть вторая химико-технологические принципы получения и использования пленкообразующих веществ
- •Глава 5. Пленкообразующие поликонденсационного типа
- •5.1. Поли- и олигоэфирные пленкообразователи
- •5.2. Немодифицированные насыщенные полиэфиры
- •5.3.Модифицированные олигоэфиры
- •Олигоэфиры, модифицированные растительными маслами и их жирными кислотами
- •1, 2, 10 Теплообменники; 3, 18 конденсаторы; 4, 16 жидкостные счетчики;
- •5.3.1. Лакокрасочные материалы на основе органорастворимых алкидных олигомеров
- •5.3.2. Водоразбавляемые олигоэфиры
- •5.3.3. Олигоэфиры, модифицированные синтетическими жирными кислотами с линейной и -разветвленной цепью
- •5.3.4. Олигоэфиры, модифицированные бензойными кислотами
- •5.3.5. Олигоэфиры, модифицированные канифолью
- •5.4. Алкидно-стирольные олигоэфиры
- •5.5. Уралкиды
- •6 Обогреваемый весовой мерник; 8 вакуум-приемник; 9 – разделительный сосуд; 10 теплообменник; 11 реактор с электроиндукционным oбогревом;
- •15 Шестеренчатый насос; 16 – весы; 17 тapa
- •17, 18 Шестеренчатые насосы; 19 патронный фильтр
- •5.6. Ненасыщенные олигоэфиры
- •5.6.1.Олигоэфирмалеинаты
- •5.6.2. Олигоэфиракрилаты
- •5.6.3. Ненасыщенные олигоэфиры, отверждаемые
- •5.7. Расчет рецептур органорастворимых алкидов
- •5.8. Лакокрасочные материалы на основе олигоэфирмалеинатов и принципы их отверждения
- •5.9. Охрана окружающей среды при производстве олигоэфиров
- •5.10. Феноло- и аминоальдегидные пленкообразователи
- •5.10.1 Фенолформальдегидные пленкообразователи
- •Поликонденсация фенола с формальдегидом при кислотном катализе (новолаки)
- •Новолачные олигомеры
- •Поликонденсация фенола с формальдегидом при основном катализе. Резолы
- •Резольные олигомеры
- •5.10.2. Модифицированные фенолоформальдегидные олигомеры
- •5.10.3. Полимеры на основе формальдегида и гомологов фенола
- •5.10.4. Полимеры на основе фенолов и других альдегидов
- •Фенолофурфурольные олигомеры
- •5.10.5. Совмещенные полимеры
- •5.10.6. Резорциноформальдегидные полимеры
- •5.10.7. Технология производства новолачных и резольных олигомеров
- •1 Объемный мерник; 2 автоматические порционные весы; 3, 4 весовые мерники; 5, 13 жидкостные счетчики; 6, 7, 14 конденсаторы; 8 – реактор;
- •5.10.8. Аминоальдегидные пленкообразователи
- •Исходное сырье
- •Основные закономерности синтеза карбамидоформальдегидных олигомеров
- •Модифицированные карбамидоформальдегиды
- •Структура и свойства карбамидоформальдегидных олигомеров
- •Основные закономерности процесса синтеза меламиноформальдегидных олигомеров
- •5.10.9. Свойства и применение аминоформальдегидов
- •5.10.10. Технология получения аминоформальдегидных олигомеров
- •5.11. Циклогексаноновые и циклогексанонформальдегидные пленкообразователи
- •5.12. Пленкообразователи эпоксидного типа
- •Отверждение
- •Отверждение аминами
- •Отверждение дикарбоновыми кислотами и их ангидридами
- •Каталитическое отверждение
- •5.12.1. Свойства и применение эпоксидных олигомеров
- •5.12.2. Циклоалифатические эпоксидные олигомеры
- •5.12.3. Алифатические эпоксидные олигомеры
- •5.12.4. Эпоксидированные новолачные олигомеры
- •5.12.5. Технология производства эпоксидных олигомеров
- •1 Конденсатор; 2 автоматические порционные весы; 3 объемный мерник;
- •4 Весовой мерник; 5 вакуум-приемник; 6 реактор с электроиндукционным обогревом; 7 обогреваемый приемник расплава олигомера; 8 барабан-кристаллизатор; 9 приемный бункер
- •Техника безопасности при производстве эпоксидных полимеров и защита окружающей среды
- •5.12.6. Лакокрасочные материалы на основе эпоксидных олигомеров
- •5.13. Пленкообразователи полиуретанового типа
- •5.13.1. Блокированные изоцианаты
- •5.13.2. Полиэфируретаны
- •5.13.3. Лакокрасочные материалы на основе полиуретановых пленкообразователей
- •5.14. Элементоорганические пленкообразующие полимеры
- •Реакции образования и строение
- •24 Горизонтальный смеситель
- •5.14.1. Модифицированные кремнийорганические пленкообразователи. Реакции отверждения. Лакокрасочные материалы на основе модифицированных кремнийорганических пленкообразователей
- •5.15. Полиамиды
- •1, 2 Жидкостные счетчики; 3, 7 весовые мерники, 4 – объемный мерник;
- •5, 6, 8 Конденсаторы; 9 реактор с пароводяной рубашкой; 10, 13, 16 – вакуум-приемники; 11, 14 реакторы с электроиндукционным обогревом,
- •5.16. Поликарбонаты
- •5.17. Пентапласт
- •5.18. Полиимиды
- •Глава 6 полимеризационные пленкообразователи
- •6.1. Полиуглеводороды
- •6.2. Поливинилацетат и его производные
- •1, 2 Жидкостные счетчики; 3, 59, 17, 19 конденсаторы; 4 автоматические порционные весы; 10, 11 аппараты для растворения поливинилового спирта;
- •6.3. Пленкообразующие на основе акриловых полимеров
- •6.4. Пленкообразующие на основе диеновых полимеров и сополимеров, их особенности
- •6.5. Эфироцеллюлозные пленкообразователи
- •6.6. Пленкообразователи на основе растительных масел
- •Химические основы переработки масел
- •6.7. Сополимеризация масел с виниловыми мономерами
- •6.7.1. Малеинизированные и стиролизованные масла
- •6.7.2. Эпоксидированные масла
- •6.7.3. Дегидратация масел
- •6.7.4. Технологические схемы получения препарированных масел и олиф
- •31, 32 Аппараты для отделения жирных кислот
- •6.7.5. Механизм химического отверждения масляных пленкообразователей
- •6.8. Сиккативы
- •6.10. Природные пленкообразующие смолы
- •6.10. Мономеры и олигомеры для получения покрытий на подложке
- •Способы инициирования полимеризации на подложке
- •Глава 7. Старение полимеров под воздействием тепла и излучений
- •7.1. Понятие о «старении» полимеров
- •7.2. Термодеструкция и термическая стойкость полимеров
- •7.3. Деструкция полимеров под действием физических и механических факторов
- •Глава 8. Деструкция полимеров под воздействием кислорода и химических реагентов
- •8.1. Действие кислорода на полимеры. Окисление и окислительная деструкция
- •8.2. Деструкция полимеров под действием химических агентов
- •8.3. Принципы стабилизации полимеров в целях защиты их от старения
- •Оглавление
- •Химия и технология пленкообразующих веществ
- •220050. Минск, Свердлова, 13а.
Основные закономерности процесса синтеза меламиноформальдегидных олигомеров
Поликонденсация меламина с формальдегидом состоит из серии последовательно-параллельных реакций: гидроксиметилирования меламина и последующей конденсации его метилольных производных.
Гидроксиметилирование меламина происходит по аминогруппам.
М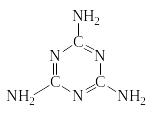 еламин
амид циануровой
кислоты (1,3,5-триамино-2,4,6-триазин);
еламин
амид циануровой
кислоты (1,3,5-триамино-2,4,6-триазин);
Тпл=351С
Присутствие трех реакционных центров в молекуле меламина обеспечивает присоединение к нему до шести молекул формальдегида с образованием гексаметилолмеламина:
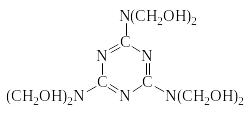
Схема последовательно-параллельных реакций гидроксиметилирования меламина включает образование продуктов с различной степенью замещения. Все реакции в схеме равновесные и протекают с небольшим экзотермическим эффектом (Н=13кДжмоль формальдегида):
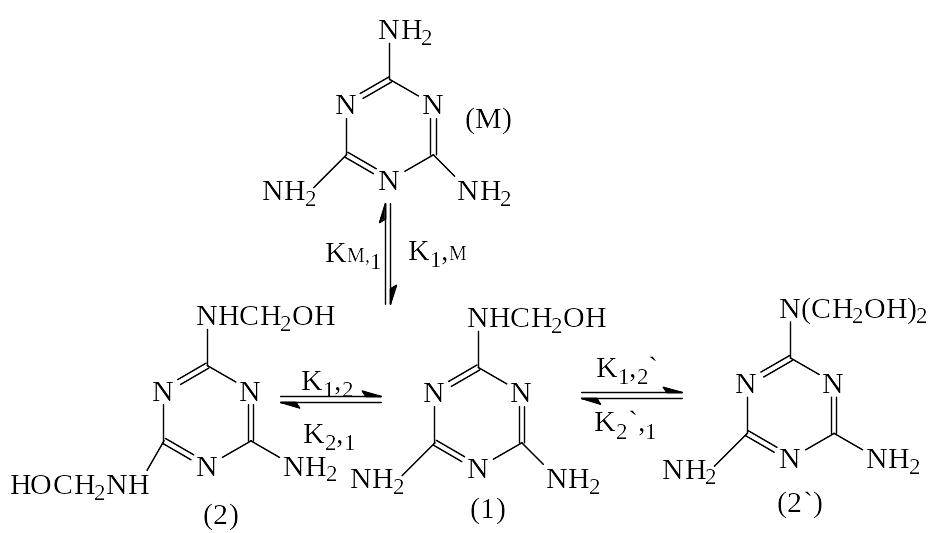
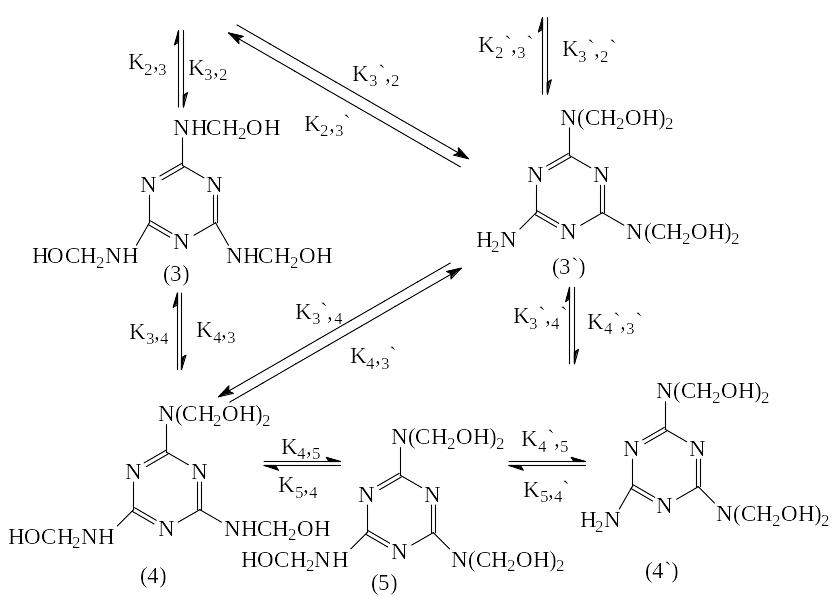
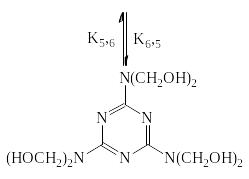
Константы равновесия реакций гидроксиметилирования меламина (t=48С; рН=9):
Км,1=26,5 К2,3=4,4 К3,4=2,9 К4,5=1,3
К1,2=12,0 К2,3=1,8 К3,4=0,47 К4,5=21,0
К1,2=0,85 К2,3=24,5 К3,4=7,2 К5,6=0,6
Уменьшение констант равновесия в ряду Км,1; К1,2; К2,3; К4,5; К5,6 (соответственно 26,5; 12,0; 4,4; 2,9; 1,3 и 0,6) свидетельствует о затруднении гидроксиметилирования с увеличением степени замещения.
В результате гидроксиметилирования обычно образуется смесь продуктов с различным числом метилольных групп в молекуле. Состав смеси в значительной степени зависит от исходного соотношения формальдегида и меламина в реакционной системе.
При соотношении формальдегидмеламин равном 1 в реакционной массе остается значительное количество непрореагировавшего меламина (60%). При соотношении, равном 3, основные продукты – моно- и диметилольные производные меламина. При увеличении указанного соотношения исходных веществ до 57 в составе продуктов наряду с моно- и диметилольными производными появляется значительное количество три- и тетраметилольных производных. Гексаметилолмеламин обнаруживается в составе продуктов лишь при соотношении формальдегидмеламин10, но доля его остается невысокой; даже при увеличении этого соотношения до 30 гексаметилолмеламина образуется лишь около 12%.
Причиной значительного содержания в составе продуктов производных с невысокой степенью метилолирования являются низкие значения констант равновесия реакций гидроксиметилирования. Поэтому, чтобы получить продукты с достаточно большим числом метилольных групп в молекуле, необходим значительный избыток формальдегида. За счет значительного избытка формальдегида удается получать продукты реакции, не содержащие непрореагировавший меламин. Меламин полностью вступает в реакцию лишь при соотношении формальдегидмеламин7.
Гидроксиметилирование меламина с заметной скоростью протекает даже в отсутствие катализатора, при температурах 3550С. Реакция подвержена катализу кислотами и основаниями.
О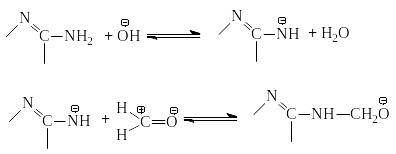 сновной
катализ сводится к повышению нуклеофильности
меламина за счет отрыва протона от одной
из NH2-групп:
сновной
катализ сводится к повышению нуклеофильности
меламина за счет отрыва протона от одной
из NH2-групп:
Трудность отрыва протона от такого сильного основания, каким является меламин, обуславливает эффективность основного катализа лишь при высоких значениях рН (9).
Специфика меламина, как сильного одноосновного основания, особенно сильно проявляется при кислотном катализе. В присутствии кислоты меламин практически полностью превращается в одноосновную сопряженную кислоту:
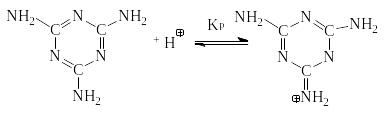
К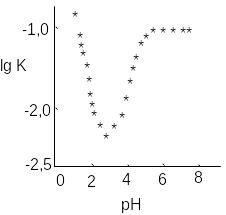 онстанта
равновесия этой реакции Кр105.
Поэтому добавление кислоты в количестве
до 1 моль на 1 моль меламина (рН в области
2) не только не
приводит к увеличению скорости реакции,
а, наоборот, замедляет ее из-за низкой
активности протонированной формы
меламина (рис. 49).
онстанта
равновесия этой реакции Кр105.
Поэтому добавление кислоты в количестве
до 1 моль на 1 моль меламина (рН в области
2) не только не
приводит к увеличению скорости реакции,
а, наоборот, замедляет ее из-за низкой
активности протонированной формы
меламина (рис. 49).
(![]() )
)
Рис. 49. Зависимость логарифма константы скорости реакции гидроксиметилирования (lg k) меламина от рН при катализе НСl. Концентрация формальдегида и меламина равна 0,094 мольл (при рН = 2,2 соотношение концентраций катализатора НСl и меламина составляет 1)
Поэтому кислотный катализ эффективен лишь при условии, что соотношение кислотамеламин 1 (рН2). В этом случае возможно активирование формальдегида по механизму кислотного катализа с последующим взаимодействием с меламином:
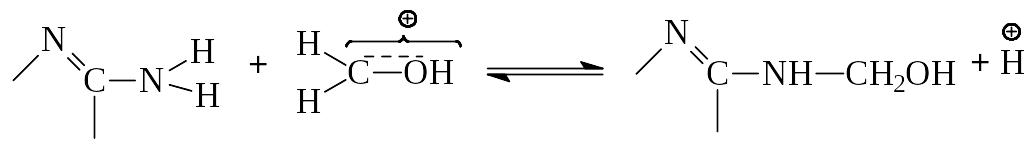
Поэтому скорость реакции гидроксиметилирования при рН2 резко возрастает.
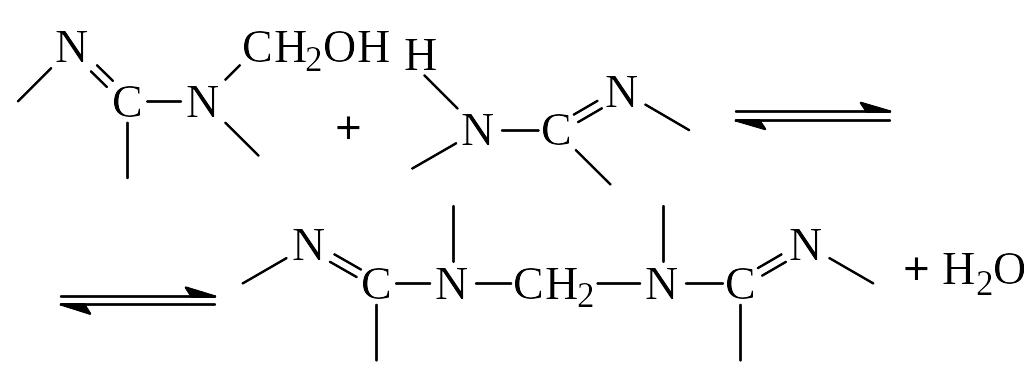 При конденсации метилольных производных
меламина происходит образование
олигомерных продуктов за счет следующих
реакций:
При конденсации метилольных производных
меламина происходит образование
олигомерных продуктов за счет следующих
реакций:
(1)
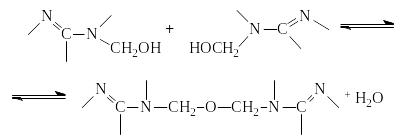
(2)
Реакция (1) преобладает в тех случаях, когда в составе продуктов гидроксиметилирования присутствуют в основном метилольные производные с небольшой степенью замещения. Реакция (2) оказывается преобладающей при условии наличия метилольных производных с более высокой степенью замещения (три-, тетра- и пентаметилолмеламина).
Хотя процесс конденсации метилольных производных меламина, так же как и метилольных производных карбамида, подвержен кислотному катализу, он имеет свои особенности. Так, при уменьшении рН с 7 до 2 скорость конденсации проходит через максимум при рН=44,5. Этот максимум соответствует отношению кислоты-катализатора к метилольному производному меламина, равному 0,5.
Данная особенность обусловлена высокой основностью метилольных производных меламина (рКа диметилольного производного равно 4,5, триметилольного – 3,9). Такая высокая основность приводит к образованию сопряженных кислот, структура которых для ди- и триметилольных производных может быть представлена следующим образом:
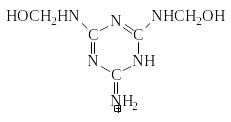
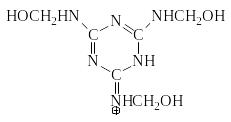
и
Поэтому конденсация метилольных производных в кислой среде может идти за счет взаимодействия нейтральных молекул, сопряженных кислот, а также сопряженных кислот с нейтральными молекулами с образованием метиленовых связей.
