
- •3.Біологічні макромолекули та їх роль в клітині
- •4.Формування просторової структури білків,біологічне значення цього процесу
- •6.Захиснафункціябілків
- •7. Пояснити біологічну зумовленість різноманітності та специфічності білкових структур.
- •8. Унікальні властивості днк
- •10. Молекулярна організація Хромосом
- •12.Організація тРнк та функціональне значення її ділянок
- •14.Сутність та біологічне значення функціональних зв'язків між білками та нуклеїновими кислотами
- •15.Особливості мітохондріальних геномів
- •15.Особливості мітохондріальних геномів
- •18. Функціональна різноманітність ферментного комплексу реплікації.
- •19. Механізм реплікативного та репараційного синтезу днк.
- •20. Функціональні зв’язки в системі днк-білки. (ст.. 89)
- •22. Біологічний сенс і-рнк, її роль в реалізації генетичної інформації.
- •23. (Ст. 133)Структура рнк-полімерази, роль у процесах реалізації генетичної інформації.
- •24. Механізми транскрипції.
- •25. Молекулярні основи експресії генів.
- •31. Особливості взаємодії геному та апарату трансляції в бактеріальних клітинах.
- •32. Генетичний код, його властивості.
- •33. Трансляція в прокаріотичних клітинах та мітохондріях.
- •34. Дозрівання білкових молекул.
- •35. Шаперони і фолдази, їх роль у фолдингу.
- •45. Синтез р-рнк та її роль у клітині
- •48. Рекомбінація молекули днк та її біологічне значення
- •49. Гіпотеза походження двомембранних органел
- •50. Взаємодія ядерного та мітохондріального геномів.
- •51.Функціональна роль компартментації цитоплазми.
- •52.Молекулярні основи поділу та розмноження клітин.
- •53.Роль циклонів та циклін-залежних кіназ у поділі клітини.
- •54.Теломери та роль теломерази у підтриманні мітотичної активності клітин.
1.Склад ТА ФУНКЦІЇ ЛІПІДІВ Залежно від хімічної структури компонентів, що вивільняються за умов повног гідролізу, ліпіди поділяються на такі класи:
1. Прості ліпіди.
1.1. Ацилгліцероли.
1.2. Стериди.
1.3. Цериди (воски).
2. Складні ліпіди.
2.1. Фосфоліпіди.
2.1.1. Гліцерофосфоліпіди.
2.1.2. Сфінгофосфоліпіди.
1. Прості ліпіди — ліпіди, що при гідролізі утворюють спирт тажирні кислоти.
1.1. Ацилгліцероли (ацилгліцериди) — ліпіди, що є складними ефірами гліцеролу (гліцерину) та жирних кислот. Ацилгліцероли (зокрема триацилгліцероли, або тригліцериди) мають емпіричну назву — нейтральні жири. Тригліцериди є основною складовою частиною адипоцитів жирової тканини людини і тварин, являючи собою молекулярну форму зберігання вищих жирних кислот — найбільш енергоємкого метаболічного палива. Природні тригліцериди є змішаними ліпідами, тобто до їх складу входять залишки різнихжирнихкислот.
1.2. Стериди — ліпіди, що є складними ефірами циклічних спиртів стеролів (стеринів) та жирних кислот. Стероли є 3-гідроксипохідними вуглеводню стерану(циклопентанпергідрофенантрену). Найбільш розповсюдженим стеролом тваринного організму є холестерол (холестерин), що входить як структурний ліпід до складу плазматичних мембран та є попередником в синтезі інших стеринів та їх похідних(стероїдів).До біологічно важливих стеринів належать стероїдні гормони кори надниркових залоз, чоловічі та жіночі статеві гормони, вітаміни групи Д та їх похідні, жовчні кислоти.
1.3. Цериди (воски) — прості ліпіди, які є складними ефірами вищих жирних кислот та високомолекулярних спиртів, зокрема цетилового До восків тваринного походження належать бджолиний віск, спермацет, ланолін, що використовуються у фармації для виготовлення мазей, кремів, у виробництві косметичних засобів.
2. Складні ліпіди — ліпіди, що при гідролізі вивільняють спирт (гліцерол, сфінгозин,інозит), а також фосфат, аміносполуки, вуглеводи. Складні ліпіди є полярними, амфіфільними сполуками і більшість із них виконує структурні функції, входячи до складу біологічних мембран. Триацилгліцерол (тригліцерид) Холестерол (холестерин) Стеран (циклопентан-пергідрофенантрен)
2.1. Фосфоліпіди.Численну групу складних ліпідів складають фосфоліпіди, які, залежно від спирту,що входить до їх складу, поділяються на гліцерофосфоліпідита сфінгофосфоліпіди.До фосфоліпідів належать: Гліцерофосфоліпіди (фосфогліцериди) —складні ефіри гліцеролутавищих жирних кислот, що є похідними фосфатидної кислоти, етерифіко-ваної аміноспиртами холіном, етаноламіном (коламіном) і оксіамінокислотою серином.Фосфодіефірний зв’язок у складі гліцерофосфоліпідів утворений гідроксильними группами холіну (фосфатидилхоліни, або лецитини), етаноламіну (фосфатидилетаноламіни, або кефаліни) або серину (фос-фатидилсерини).Природні гліцерофосфоліпіди містять у центральному (2-му, положенні залишки ненасичених, а в крайньому (1-му, -) — насичених жир-них кислот.Сфінгофосфоліпіди —складні ефіри багатоатомного аміноспирту сфінгозину та вищих жирних кислот, що можуть такожмістити залишки холіну, фосфорної кислоти. N-ацильні похідні сфінгозину та жирних кислот мають назву церамідів:Сфінгофосфоліпіди є фосфорними ефірами церамідів та аміноспиртів — холіну,етаноламіну, серину. В нервовій тканині людини та вищих тварин присутні сфінгомієліни(N-ацил-сфінгеніл-фосфохоліни): Фосфатидна кислота Холін Етаноламін Серин Фосфатидилхолін Фосфатидилетаноламін Фосфатидилсерин Сфінгозин N-Ацилсфінгозин (церамід)
2.2. Гліколіпіди — сполуки, в яких ліпідна частина ковалентно зв’язана з вуглеводною. Гліколіпіди є складними ефірами вищих жирних кислот тагліцеролу або сфінгозину і містять у своєму складі вуглеводний компонент (зокрема, глюкозу, галактозу та їхпохідні або олігосахаридну групу). Глікозилгліцероли (глікозилгліцериди) — гліколіпіди, що є ефірами гліцеролу. Глікосфінголіпіди — гліколіпіди, що є ефірами N-ацилсфінгозинів (церамідів). Цей клас гліколіпідів (або сфінголіпідів) має важливе біологічне значення у зв’язку з розповсюдженням глікосфінголіпідів у складі біомембран, зокрема в нервовійтканині; дотого ж, існує ряд спадкових захворювань, пов’язаних з порушеннямметаболізму цього класу ліпідів. Залежно від будови вуглеводної частини молекули, глікосфінголіпіди розділяють на декілька класів: цереброзиди, гангліозиди, сульфатидита глобозиди:
а) цереброзиди —моногексозидицерамідів; найбільш поширеними представниками є галактоцереброзиди та глюкоцереброзиди: Природними цереброзидами мембран нейронів головного мозку є галакто-цереброзиди; аномальненакопичення в мозку глюкоцереброзидів спостерігається при хворобі Гоше (Gaucher), що супроводжується затримкою розумового розвитку та важкими неврологічними порушеннями.
б) сульфатиди — сульфатовані похідні цереброзидів, найбільш поширеним представником яких є галактоцереброзидсульфат (3'-сульфогалактоцереброзид).Генетичний дефект, який призводить до підвищеного вмісту в нервовій тканині галактоцереброзидсульфату, має місце при спадковій хворобі — мета хроматичній лейкодистрофії, що проявляється важкими психічними розладами.
в)глобозиди — олігосахаридні похідні (олігогексозиди) церамідів.Олігосахаридний залишок глобозидів найчастіше містить у своєму складі галактозу, глюкозу або N-ацетилгалактозамін. Прикладами глобозидів є дигексозид лактозилцерамід еритроцитарних мембран, тригексозид галактозиллактозилоцерамід.
г) гангліозиди — глікосфінголіпіди, що містять в олігосахаридному ланцюзі,крім галактози, глюкози та N-гексозамінів, один або більше залишків дев’ятивуглецевого моносахариду нейрамінової або N-ацетилнейрамінової (сіалової) кислоти.
Ліпіди мембран Ліпідні компоненти біологічнихмембран представлені переважно різними класами полярних ліпідів: фосфоліпідами (фосфатидилхоліном, фосфатидилетаноламіном, фосфатидилсерином, сфінгомієліном) — до 80-90% загального вмісту мембранних ліпідів; гліколіпідами (переважно глікосфінголіпідами). Зовнішня плазматична мембрана характеризується значним вмістом вільного холестеролу та його ефірів і наявністю гліколіпідів, які відсутні в інших мембранних структурах
2. Роль води в живих системах Властивості води H2O багато в чому унікальні й обумовлені її будовою. В утворенні хімічних зв'язків у молекулі води беруть участь р-електрони атома Оксигену й s-електрони атомів Гідрогену. В окремій молекулі води атоми Гідрогену й Оксигену розташовані так, що утворюють рівнобедрений трикутник. У вершині його атом Оксигену, у кутах при основі — атоми Гідрогену. Зв'язки H-О-H розташовані під кутом 104,5º. Атом Оксигену має більшу електронегативність, тому зв'язок О-H є полярним. Атоми Гідрогену несуть частковий позитивний заряд, а атом Оксигену — частковий негативний заряд. У різних частинах молекули зосереджені протилежні заряди. Таким чином, молекула води є полярною, має кутову форму і є електричним диполем. Кожна молекула води, як магніт, притягує до себе інші молекули або йони. Тому, на відміну від більшості інших рідин, вода є ідеальним розчинником для багатьох речовин.
Вода як розчинник. Вода – чудовий розчинник для полярних речовин. До них відносяться іонні з'єднання, такі як солі, у яких заряджені частинки (іони) дисоціюють у воді, коли речовина розчиняється, а також деякі неіонні з'єднання, наприклад цукру і прості спирти, в молекулі яких присутні заряджені (полярні) групи (-OH). Результати численних досліджень будови розчинів електролітів свідчать, що при гідратації іонів у водних розчинах основну роль грає ближня гідратація – взаємодія іонів з найближчими до них молекулами води. Великий інтерес представляє з'ясування індивідуальних характеристик ближньої гідратації різних іонів, як ступеня скріплення молекул води в гідратних оболонках, так і ступеня спотворення в цих оболонках тетраедричної льодоподібної структури чистої води – зв'язки в молекулі змінюються на неповний кут. Величина кута залежить від іона. Коли речовина розчиняється, його молекули або іони дістають можливість рухатися вільніше і, відповідно, його реакційна здатність зростає. З цієї причини в клітці велика частина хімічних реакцій протікає у водних розчинах. Неполярні речовини, наприклад ліпіди, не змішуються з водою і тому можуть розділяти водні розчини на окремі компартаменти, подібно тому, як їх розділяють мембрани. Неполярні частини молекул відштовхуються водою і в її присутності притягуються один до одного, як це буває, наприклад, коли крапельки масла зливаються в більш крупні краплі; інакше кажучи, неполярні молекули гідрофобні. Подібні гідрофобні взаємодії грають важливу роль в забезпеченні стабільності мембран, а також багатьох білкових молекул, нуклеїнових кислот і інших субклітинних структур.
3.Біологічні макромолекули та їх роль в клітині
Біомолекули — біоорганічні сполуки, що входять до складу живих організмів та спеціалізовані для утворення клітинних структур і участі в біохімічних реакціях, які становлять сутність обміну речовин та фізіологічних функцій живих клітин.
Функції біомолекул у живих організмах:
а) участь у біохімічних реакціях обміну речовин в ролі субстратів та проміжних продуктів (метаболітів). Прикладами є моносахариди та їх фосфорні ефіри, жирні кислоти та продукти їх окислення, амінокислоти, кетокислоти, дикарбонові кислоти, пуринові та піримідинові основи тощо;
б) участь в утворенні інших, більш складних молекул — білків, нуклеїнових
кислот, полісахаридів, ліпідів (наприклад, амінокислоти, нуклеотиди, вищі жирні кислоти тощо), або біологічних структур (мембран, рибосом, ядерного хроматину тощо);
в) участь у регуляції біохімічних процесів та фізіологічних функцій окремих
клітин та цілісного організму. Біомолекулами-регуляторами є вітаміни, гормони та гормоноподібні сполуки, внутрішньоклітинні регулятори — циклічні нуклеотиди цАМФ, цГМФ тощо.
біополімери — білки, полісахариди і нуклеїнові кислоти (ДНК, РНК).
Ліпіди (жири) — не є макромолекулами, оскільки вони не створюють великих ковалентно зв'язаних молекул.
4.Формування просторової структури білків,біологічне значення цього процесу
У 1959 р датський біохімік К.Ліндерстрем-Ланг запропонував розрізняти 4 рівня структурної організації білків:первинна,вторинна,третинна і четвертинна структури,які визначають відповідно амінокислотну послідовність , упорядковану структуру основного ланцюга поліпептида,трьохмірну структуру білка і структури білкових агрегатів. Ця класифікація панувала до 80 років ХХ ст, коли Шульц і Шимер з урахуванням структурних особливостей білків запропонували доповнити її ще двома рівнями організації : зверхвторичними структурами і доменами. Внаслідок цього склалалось уява про 6 рівнів структурної організації білків з певною організацією, вираженою Шульцем і Шимером в вигляді схеми,за основу в якій покладено визначена генетично детермінована амінокислотна послідовність поліпептидного ланцюга(первинна структура) яка визначає всі наступні більш високі рівні організації
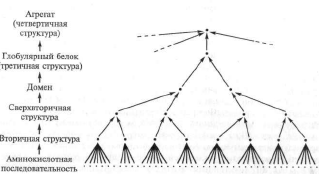
Біологічне значення: В залежності від форми і будови амінокислотних ланцюгів виникають різні рівні організації і різні конформації(що залежить від зміни перерозподілу амінокислотних груп) Розглядаючит молекулярні механізми формування вищих рівнів структурної організації білків, необхідно зауважити,що всі високовпорядковані форми просторової конформації білкових молекул детерміновані первинною структурою поліпептидного ланцюга, тобто амінокислотною послідовністю, яка визначається генетичним кодом клітини, в якій синтезується даний білок. Вторинна, третинна, четвертинна та доменна організації білків є результатом довільного, спонтанного формування просторових угруповань, що спрямовані на досягнення складним біофізичним утворенням, яке являє собою макромолекулу білка, термодинамічно стабільного стану
5.Cутність доменної організації білкових молекул(домен – це проміжна ланка переходу від вторинної до тритинної структури)Аналіз електронної платності білка показує наявність в білках чітко виражених областей – структурних доменів.Молекулярна маса елементарних структурних доменів становить 20кДа.
Домени — структурні ділянки білкових молекул, що являють собою глобулярні утворення всередині білків із третинною структурою. Діаметр глобулярного домену дорівнює в середньому 2,5 нм; до його складу входить 100-150 амінокислотних залишків.Окремі домени є функціонально відносно автономними утвореннями в складі білкових молекул, і доменні білки в цьому відношенні подібні до олігомерних білків. Але, на відміну від білків із четвертинною структурою (олігомерів), окремі доменні глобули утворюються тим самим поліпептидним ланцюгом і,відповідно, зв’язані між собою пептидними фрагментами (“шарнірними” ділянками). Зв’язки між доменами можна розщепити тільки за допомогою протеолітичних ферментів. Прикладами доменних білків є ферменти гліколітичного шляху окислення глюкози — гліцеральдегідфосфатдегідрогеназа та фосфогліцераткіназа у складі яких окремі домени реалізують різні етапи складного каталітичного акту. всі високо впорядковані форми просторової конформації білкових молекул детерміновані первинною структурою поліпептидного ланцюга, тобто амінокислотною послідовністю, яка визначається генетичним кодом клітини, в якій синтезується даний білок.Вторинна, третинна, четвертинна та доменна організації білків є результатом довільного, спонтанного формування просторових угруповань, що спрямовані на досягнення складним біофізичним утворенням, яке являє собою макромолекулу білка, термодинамічно стабільного стану
