
- •31. Коллигативные св-ва разб.Р-ров неэлектролитов.
- •Закон Рауля:
- •Следствия из 1 закона Рауля:
- •Закон Вант-Гоффа:
- •Закон разбавления Оствальда
- •33. Сильные электролиты
- •34. Особенности коллигативных свойств растворов электролитов
- •Роль осмоса в биологических системах
- •Основные положения протолит.Теории кислот и оснований (Лоури-Брёнстеда)
- •Механизм буферного действия
- •37 Реакции гидролиза
- •РН водных растворов солей различных типов
- •Роль гидролиза в био системах
- •Условие образования и растворения осадка
34. Особенности коллигативных свойств растворов электролитов
Растворы электролитов (соли, кислоты, основания) обладают способностью проводить электрический ток. В 1887 г. Вант-Гофф установил, что определенное экспериментально осмотическое давление в растворах электролитов превышает вычисленное по уравнению
Росм = СМ·R·T
Подобное отклонение измеренных величин от вычисленных наблюдается также для ∆tкип и ∆tзам растворов электролитов.
Вант-Гофф ввел поправочный множитель i, названный изотоническим коэффициентом. Растворы с одинаковым осмотическим давлением называют изотоническими.
Вводя i в уравнения, получаем соотношения, пригодные для описания свойств разбавленных растворов всех веществ:
Росм = i·СМ·R·T ∆Ткип = i·Е·Сm ∆Р = i·Р0·N1 ∆Тзам = i·К·Сm
Изотонический коэффициент i зависит от природы раствора и его концентрации, но для одного и того же раствора значение i одинаково во всех 4-х приведенных уравнениях.
Осмос играет важнейшую роль в процессах жизнедеятельности животных и растений, поскольку клеточная плазматическая мембрана является полупроницаемой. Осмос обусловливает поднятие воды по стеблю растений, рост клетки и многие другие явления.
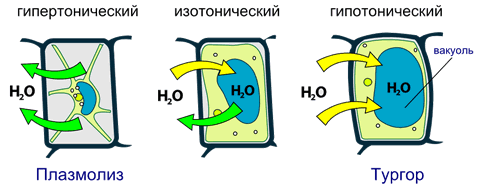
Рассмотрим роль осмоса в водном режиме растительной клетки. Осмотическое давление жидкости, контактирующей с клеткой, может быть больше, меньше либо равно осмотическому давлению внутриклеточной жидкости. Соответственно выделяют гипертонические, гипотонические и изотонические растворы.
Если клетка находится в контакте с гипертоническим раствором, вода выходит из неё путём осмоса через плазматическую мембрану. Протопласт (живое содержимое клетки) при этом уменьшается в объёме, сморщивается и в конце концов отстаёт от клеточной стенки. Этот процесс называют плазмолизом. Процесс плазмолиза обычно обратим.
Если клетку поместить в чистую воду или гипотонический раствор, вода путём осмоса поступает в клетку; протопласт при этом увеличивается в объёме и оказывает давление на сравнительно жёсткую клеточную стенку. Этот процесс называется тургором. Тургорное давление препятствует дальнейшему поступлению воды в клетку. Именно тургорное давление поддерживает стебли растений в вертикальном положении, придаёт растениям прочность и устойчивость.
Изотонические растворы не оказывают влияния на водный режим клетки.
У животных клеток нет клеточной стенки, поэтому они более чувствительны к осмотическому давлению жидкости, в которой находятся.
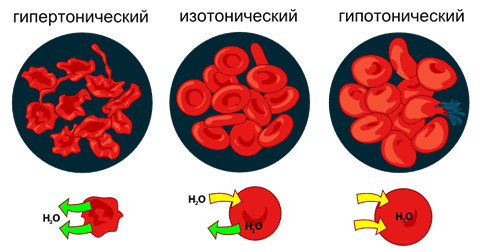
Изоосмия, изотония (от изо... и греч. osmós — толчок, tónos — напряжение), относительное постоянство осмотического давления в жидких средах и тканях организма, обусловленное поддержанием на данном уровне концентраций содержащихся в них веществ: электролитов, белков и т. д. Изоосмия — одна из важнейших физиологических констант организма, обеспечиваемых механизмами саморегуляции (см. Гомеостаз). Отклонение осмотического давления от нормального физиологического уровня » 0,76—0,81 Мн/м2 (7,6—8,1 ат) влечёт за собой нарушение обменных процессов между кровью и тканевой жидкостью.
