
- •004Федеральное агентство по образованию
- •Химия гетероциклических соединений
- •Номенклатура.
- •Способы синтеза пиридинов.
- •Физические свойства пиридина и его ближайших гомологов
- •Строение молекулы пиридина. Ароматичность.
- •Химические свойства пиридина
- •Образование π-комплексов.
- •Реакции с участием атома азота.
- •Реакции с участием атома углерода. Реакции электрофильного замещения атома водорода
- •Глава 2. Хинолин
- •2.1. Номенклатура.
- •2.4. Физические свойства хинолина и его ближайших гомологов.
- •2.5. Строение молекулы хинолина. Ароматичность.
- •2.6. Кислотно-основные свойства хинолина.
- •2.7. Химические свойства хинолинов.
- •2.7.1. Реакции хинолинов по атому азота.
- •2.7.1.1. Алкилирование.
- •2.7.2.2.Ацилирование.
- •2.7.2. Реакции электрофильного замещения атома водорода.
- •2.7.2.1. Нитрование.
- •2.7.2.2. Сульфирование.
- •2.7.2.3 Галогенирование.
- •2.7.2.4. Меркурирование.
- •2.7.3. Реакции нуклеофильного замещения атома водорода.
- •2.7.3.1. Аминирование.
- •2.7.3.2. Гидроксилирование.
- •2.7.3.3. Алкилирование и арилирование.
- •2.7.4. Реакции нуклеофильного замещения атома галогена.
- •2.7.5. Реакции радикального замещения в ряду хинолина.
- •2.7.6. Реакции окисления и восстановления в ряду хинолина.
- •2.8. Химические свойства алкилхинолинов.
- •2.9. Химические свойства хинолин-n-оксида.
- •2.10. Практическое использование производных хинолина.
- •Глава 3. Изохинолин
- •2.1. Номенклатура.
- •3.2. Нахождение в природе.
- •3.3. Методы получения изохинолинов.
- •3.3.1. Однокомпонентный синтез.
- •3.3.1.1. Синтез типа n(1)c(8a).
- •3.3.2. Двухкомпонентные синтезы.
- •3.4. Физические свойства изохинолина и его ближайших гомологов.
- •3.5. Строение молекулы изохинолина. Ароматичность.
- •3.6. Кислотно-основные свойства изохинолина.
- •3.7.2.1. Нитрование.
- •3.7.2.2. Сульфирование.
- •3.7.2.3 Галогенирование.
- •3.7.3.4. Нитрование.
- •3.7.4. Реакции нуклеофильного замещения атома галогена.
- •3.7.5. Реакции радикального замещения в ряду изохинолина.
- •3.7.6. Реакции окисления и восстановления в ряду изохинолина.
- •3.8. Химические свойства алкилизохинолинов.
- •3.9. Химические свойства изохинолин-n-оксида.
- •3.10. Практическое использование производных изохинолина.
004Федеральное агентство по образованию
ГОУ ВПО «Пермский государственный университет»
С.Н.Шуров
Химия гетероциклических соединений
ШЕСТИЧЛЕННЫЕ ГЕТРОЦИКЛЫ
С ОДНИМ ГЕТЕРОАТОМОМ:
ПИРИДИН, ХИНОЛИН, ИЗОХИНОЛИН
Учебное пособие для студентов химического факультета,
изучающих спецкурс
«Химия гетероциклических соединений»
Пермь 2008
УДК 547
ББК
Ш362
Шуров С.Н.
Ш362 АЗИНЫ: ШЕСТИЧЛЕННЫЕ ГЕТРОЦИКЛЫ С ОДНИМ ГЕТЕРО-АТОМОМ: ПИРИДИН, ХИНОЛИН, ИЗОХИНОЛИН: Учебное пособие для студентов химического факультета / Перм.ун-т.- Пермь, 2008. – 100 с.
ISBN
Пособие предназначено для студентов Пермского университета, изучающих спецкурс «Химия гетероциклических соединений». В пособии рассмотрены основные способы синтеза азинов: пиридина, хинолина и изохинолина, а также их строение, свойства и области применения.
Рецензенты
ISBN
Введение
Азинами называются шестичленные гетероциклические соединения, у которых в кольце находится хотя бы один атом азота. Шестичленные гетероциклы с двумя и большим количеством атомов азота называют диазинами, триазинами и т.д. Простейшим моноазином является пиридин. Азиновые циклы могут быть конденсированы с другими циклами, например с бензольным. Существует два бензопиридина – хинолин и изохинолин. В настоящем пособии рассматриваются простейшие моноазины – пиридин, хинолин и изохинолин.

пиридин хинолин изохинолин
Формальная замена группы СН в молекулах бензола или нафталина при переходе к азинам существенно меняет реакционную их способность по сравнению с карбоциклическими аналогами. Моноазины менее склонны к реакциям электрофильного замещения, но более восприимчивы к атакам нуклеофильных реагентов. Пиридин и бензопиридины присоединяют некоторые ре-агенты, причем продукты присоединения часто бывают настолько устойчивыми, что могут быть выделены.
П И Р И Д И Н
Сообщение о получении соединения, содержащего, как было позже показано, пиридиновый цикл, датируется 1846 г. Именно в этом году шотландский химик Т.Андерсон на заседании королевского химического общества в Эдинбурге сообщил о выделении из каменноугольной смолы нового химического вещества пиколина, изомерного анилину. Как показали его же дальней-шие исследования, полученный пиколин не был индивидуальным соединением, а представлял смесь пиридина и метилпиридинов, названных в последствии пиколинами. В 1851 г. Т.Андерсон выделил из костяного масла – продук-та сухой перегонки оленьего рога - достаточно чистый пиридин. Синтетически пиридин был получен в 1877 г. У.Рамсеем из ацетилена и синильной кислоты при 800-950°С.
На структурное родство пиридина и бензола обратили внимание В.Кер-нер (1869 г.) и независимо Дж. Дьюар (1871 г.). Структурную формулу пиридина (как азабензола) предложил в 1888 г. А.Ладенбург.
Номенклатура.
Нумерация атомов в молекуле пиридина (азина по системе Ганча-Вид-мана) начинается с атома азота.

Атомы углерода С2 и С6 называются также α-углеродными атомами, С3 и С5 – β-углеродными атомами, а атом С4 – γ-углеродным атомом. Метилпиридины называются пиколинами:
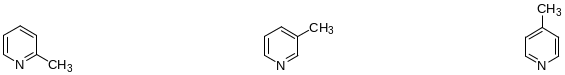
α –пиколин β-пиколин γ –пиколин
Диметилпиридины называют лутидинами, а триметилпиридины – коллидинами:

2,4-лутидин 2,4,6-коллидин
Тривиальные названия имеют и некоторые карбоновые кислоты пиридинового ряда:

пиколиновая никотиновая изоникотиновая
кислота кислота кислота
Пиридин-2,3-дикарбоновая кислота называется хинолиновой, а пиридин-3,4-дикарбоновая кислота – изохинолиновой кислотой.
Полностью гидрированный пиридин называется пиперидином, пиколины – пипеколинами.
Нахождение в природе.
Пиридин и его ближайшие гомологи находятся в продуктах переработки каменного угля, откуда их и выделяют. Несмотря на то, что количество «пиридиновых» оснований по массе составляет 0.1% от массы переработанной угля, этого количества долгое время оказывалось достаточно для удовлетворения нужд промышленности и науки. Некоторые более сложные производные пиридина, например, никотин и анабазин, обнаружены в растениях Nicotiana tabacum и Anabasis aphylla L., соответственно.

никотин анабазин
