
Лекции по молекулярной физике / Лекция 18
.doc6.12 Капиллярные явления
Пусть жидкость находится в каком-либо сосуде. Если расстояния между поверхностями, ограничивающими жидкость сравнимы с радиусом кривизны поверхности жидкости, то такие сосуды называются капиллярами. Явления, происходящие в капиллярах, называются капиллярными явлениями. К капиллярным явлениям относят капиллярный подъём жидкости и капиллярное сцепление между смачиваемыми поверхностями.
 Наиболее
простыми и часто используемыми капиллярами
являются цилиндрические капилляры
(рис.6.20). Поверхность жидкости в таких
капиллярах является сферической. Пусть
r
- радиус кривизны поверхности жидкости,
R
– радиус капилляра, θ – краевой угол.
В случае частичного смачивания жидкость
будет подниматься по капилляру под
действием давления Лапласа, до тех пор,
пока его не скомпенсирует гидравлическое
давление жидкости:
Наиболее
простыми и часто используемыми капиллярами
являются цилиндрические капилляры
(рис.6.20). Поверхность жидкости в таких
капиллярах является сферической. Пусть
r
- радиус кривизны поверхности жидкости,
R
– радиус капилляра, θ – краевой угол.
В случае частичного смачивания жидкость
будет подниматься по капилляру под
действием давления Лапласа, до тех пор,
пока его не скомпенсирует гидравлическое
давление жидкости:
![]() ,
(6.46)
,
(6.46)
 где
ρ – плотность жидкости, g
– ускорение силы тяжести, h
– высота капиллярного подъёма. Радиус
кривизны поверхности жидкости удобно
выразить через радиус капилляра, который
можно легко измерить:
где
ρ – плотность жидкости, g
– ускорение силы тяжести, h
– высота капиллярного подъёма. Радиус
кривизны поверхности жидкости удобно
выразить через радиус капилляра, который
можно легко измерить:
![]() .
Давление Лапласа для сферической
поверхности определяют по формуле
(6.42). Подставляя его выражение в формулу
(6.46), получим:
.
Давление Лапласа для сферической
поверхности определяют по формуле
(6.42). Подставляя его выражение в формулу
(6.46), получим:
![]() (6.47)
(6.47)
В случае полного смачивания θ =0о, cos θ =1, r = R и формула высоты капиллярного подъёма имеет вид:
![]()
 (6.48)
(6.48)
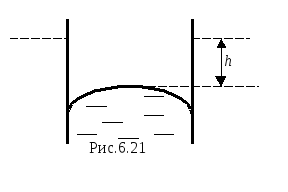
При полном несмачивании θ=180о, cos θ = - 1, и высота капиллярного подъёма будет отрицательной, то есть поверхность жидкости опустится на величину h (рис. 6.21).
Интересно отметить, что в сообщающихся капиллярах высота уровня жидкости не одинакова. Наибольший капиллярный подъём наблюдается в самом узком капилляре, а наименьший – в самом широком капилляре (рис.6.22).
 В
случае капиллярного подъёма между двумя
плоскопараллельными поверхностями,
находящимися на расстоянии d
(рис.6.23), поверхность жидкости будет
иметь цилиндрическую форму. Радиус
кривизны поверхности выразим через
расстояние между поверхностями:
В
случае капиллярного подъёма между двумя
плоскопараллельными поверхностями,
находящимися на расстоянии d
(рис.6.23), поверхность жидкости будет
иметь цилиндрическую форму. Радиус
кривизны поверхности выразим через
расстояние между поверхностями:![]() .
Высота подъёма жидкости по-прежнему
будет определена условием (6.46). Высота
капиллярного подъёма в этом случае
равна:
.
Высота подъёма жидкости по-прежнему
будет определена условием (6.46). Высота
капиллярного подъёма в этом случае
равна:
![]() (6.49)
(6.49)
Для полного смачивания
![]() .
Капиллярные явления наблюдаются при
подъёме воды к поверхности почвы, при
использовании промокательной бумаги,
тряпки, при подъёме керосина в фитилях
и т.п.
.
Капиллярные явления наблюдаются при
подъёме воды к поверхности почвы, при
использовании промокательной бумаги,
тряпки, при подъёме керосина в фитилях
и т.п.
 Капиллярное
сцепление.
Известно, что две пластины, смоченные
жидкостью, очень трудно разъединить,
прикладывая силу в направлении,
перпендикулярном пластинам. Причина
такого сильного взаимодействия пластин
– наличие отрицательного давления
Лапласа. Любой элемент свободной
поверхности жидкости представляет
собой вогнутый цилиндр (рис.6.24). Давление,
возникающее из-за кривизны поверхности,
будет отрицательным. Следовательно,
давление в жидкости будет меньше
нормального на величину давления
Лапласа, которое для цилиндрической
поверхности в случае полного смачивания
будет равно
Капиллярное
сцепление.
Известно, что две пластины, смоченные
жидкостью, очень трудно разъединить,
прикладывая силу в направлении,
перпендикулярном пластинам. Причина
такого сильного взаимодействия пластин
– наличие отрицательного давления
Лапласа. Любой элемент свободной
поверхности жидкости представляет
собой вогнутый цилиндр (рис.6.24). Давление,
возникающее из-за кривизны поверхности,
будет отрицательным. Следовательно,
давление в жидкости будет меньше
нормального на величину давления
Лапласа, которое для цилиндрической
поверхности в случае полного смачивания
будет равно
![]() ,
где d
– расстояние между пластинами.
,
где d
– расстояние между пластинами.
Пластины
будут сдавлены давлением Лапласа. Сила
сцепления пластин может быть определена
по формуле![]() ,
где S
– площадь пластины, смоченной жидкостью
(площадь основания вогнутого цилиндра).
При малом зазоре d
между пластинами, давление Лапласа
велико и сила сцепления имеет большое
значение. Сила сцепления также возрастает
при увеличении площади поверхности
пластины, смоченной жидкостью.
,
где S
– площадь пластины, смоченной жидкостью
(площадь основания вогнутого цилиндра).
При малом зазоре d
между пластинами, давление Лапласа
велико и сила сцепления имеет большое
значение. Сила сцепления также возрастает
при увеличении площади поверхности
пластины, смоченной жидкостью.
6.13 Зависимость коэффициента поверхностного натяжения от температуры и свойств вещества
С повышением температуры коэффициент поверхностного натяжения жидкостей уменьшается, а при критической температуре равен нулю. Коэффициент поверхностного натяжения жидкостей зависит также от плотности и молярной массы жидкости. Причём зависимость коэффициента поверхностного натяжения от температуры выражена тем сильнее, чем больше плотность жидкости и меньше её молярная масса. Для определения коэффициента поверхностного натяжения можно использовать полуэмпирическую формулу [1,2]:
![]() (6.50)
(6.50)
Здесь В – постоянный коэффициент, практически одинаковый для всех жидкостей, Тк – критическая температура, ρ- плотность жидкости, μ – её молярная масса, τ- небольшая величина размерности температуры. Формула (6.50) неприменима вблизи критической температуры. Коэффициент поверхностного натяжения водных растворов зависит от рода растворённого вещества. Одни вещества, например, такие как спирт, мыло, стиральные порошки, растворённые в воде, имеющие меньшую, чем у воды плотность, приводят к уменьшению коэффициента поверхностного натяжения и называются поверхностно активными веществами. Поверхностно активные вещества применяют в качестве смачивателей, флотационных реагентов, пенообразователей, диспергаторов- понизителей твёрдости, пластифицирующих добавок, модификаторов кристаллизации и т.п. Увеличение концентрации таких веществ приводит к уменьшению коэффициента поверхностного натяжения. Другие вещества, растворённые в воде, например, сахар, соль, приводят к увеличению плотности раствора и увеличивают коэффициент поверхностного натяжения. Увеличение концентрации таких веществ приводит к увеличению коэффициента поверхностного натяжения. Для экспериментального определения коэффициентов поверхностного натяжения используют несколько методов измерения: метод Ребиндера, метод капиллярных волн, метод капли и пузырька и др.
