
Глава 4 патоморфология, патогенез и патофизиология
Вдыхание сигаретного дыма и других вредных частиц приводит к воспалению в легочной ткани; этот нормальный ответ на повреждение чрезмерно усилен у лиц, склонных к развитию ХОБЛ. Такой патологический воспалительный ответ может вызвать разрушение паренхимы (приводящее к эмфиземе) и нарушение работы нормальных защитных и восстановительных механизмов (приводящее к фиброзу мелких бронхов). Следствием этих патологических изменений является образование «воздушных ловушек» и прогрессирующего ограничения скорости воздушного потока. Ниже представлен краткий обзор патоморфологических изменений при ХОБЛ.
ПАТОМОРФОЛОГИЯ
Характерные для хронической обструктивной болезни легких патоморфологические изменения обнаруживают в проксимальных дыхательных путях, периферических дыхательных путях, паренхиме легких и легочных сосудах (табл. 4-1). Эти патологические изменения включают признаки хронического воспаления с увеличением количества специфических типов воспалительных клеток в разных отделах легких, а также структурные изменения, обусловленные чередованием процессов повреждения и восстановления. В целом воспалительные и структурные изменения увеличиваются со степенью тяжести заболевания и сохраняются даже после прекращения курения.

Таблица 4-1. Патоморфологические изменения при ХОБЛ
Проксимальные дыхательные пути (трахея, бронхи с внутренним диаметром >2 мм)
Воспалительные клетки: повышенное количество макрофагов, T-лимфоцитов CD8+ (цитотоксические), небольшое количество нейтрофилов или эозинофилов.
Структурные изменения: повышенное количество бокаловидных клеток, увеличенные подслизистые железы (обе особенности ведут к гиперсекреции слизи), плоскоклеточная метаплазия эпителия.
Периферические дыхательные пути (бронхиолы с внутренним диаметром <2 мм)
Воспалительные клетки: повышенное количество макрофагов, T-лимфоцитов (CD8+ > CD4+) и B-лимфоцитов, лимфоидные фолликулы, повышенное количество фибробластов, небольшое количество нейтрофилов или эозинофилов.
Структурные изменения: утолщение стенки бронхиол, перибронхиальный фиброз, воспалительный экссудат в просвете бронха, сужение бронхиол (обструктивный бронхиолит); усиление воспалительного ответа и увеличение экссудата коррелируют со степенью тяжести заболевания.
Паренхима легких (респираторные бронхиолы и альвеолы)
Воспалительные клетки: повышенное количество макрофагов и T-лимфоцитов CD8+.
Структурные изменения: разрушение альвеолярной стенки, апоптоз эпителиальных и эндотелиальных клеток.
• Центрилобулярная эмфизема: дилатация и разрушение респираторных бронхиол, чаще всего выявляемые у курильщиков.
• Панацинарная эмфизема: разрушение альвеолярных мешочков, а также респираторных бронхиол; чаще всего обнаруживаются при дефиците α1-антитрипсина.
Легочные сосуды
Воспалительные клетки: повышенное количество макрофагов и T-лимфоцитов.
Структурные изменения: утолщение интимы, дисфункция эндотелиальных клеток, гипертрофия гладкомышечных клеток→легочная гипертензия.
ПАТОГЕНЕЗ
Воспаление в дыхательных путях у пациентов с ХОБЛ выглядит как патологически усиленный нормальный воспалительный ответ дыхательных путей на хронические ирританты, например сигаретный дым. Механизмы такого усиления пока не вполне понятны, но могут быть генетически обусловлены. В ряде случаев ХОБЛ может развиться у некурящих лиц, однако природа воспалительного ответа у таких пациентов неизвестна. В результате окислительного стресса и избытка протеиназ в легочной ткани происходит дальнейшее усиление воспалительного процесса в легких. Вкупе все эти механизмы приводят к характерным для ХОБЛ патоморфологическим изменениям
Воспалительные клетки
Для ХОБЛ характерна специфическая картина, включающая нейтрофилы, макрофаги и лимфоциты (табл. 4-2). Эти клетки выделяют воспалительные медиаторы и взаимодействуют со структурными клетками дыхательных путей и паренхимы легких.

Таблица 4-2. Воспалительные клетки при ХОБЛ
Нейтрофилы. Повышенное количество в мокроте курильщиков без ХОБЛ. В дальнейшем повышается при ХОБЛ и зависит от тяжести заболевания. В тканях обнаруживается небольшое количество нейтрофилов. Они могут играть важную роль в гиперсекреции слизи и высвобождении протеиназ.
Макрофаги. Значительно повышенное количество в просвете дыхательных путей, паренхиме легких и жидкости бронхоальвеолярного лаважа. Образуются из моноцитов крови, которые дифференцируются в макрофаги в ткани легких. У пациентов с ХОБЛ вырабатывают увеличенные количества воспалительных медиаторов и протеиназ в ответ на сигаретный дым и способны к защитному фагоцитозу.
T-лимфоциты. В стенке дыхательных путей и легочной паренхиме отмечается повышение количества клеток CD4+ и CD8+, причем увеличивается отношение CD8+/CD4+. Повышенное количество T_клеток CD8+ (Tc1) и клеток Th1, которые выделяют интерферон_γ и экспрессируют хемокиновый рецептор CXCR3. Клетки CD8+ могут оказывать цитотоксическое действие на альвеолярные клетки, что способствует их разрушению.
B-лимфоциты. Повышенное количество в периферических дыхательных путях и в лимфоидных фолликулах, возможно, в ответ на хроническую колонизацию и инфекцию дыхательных путей.
Эозинофилы. Увеличение количества эозинофильных белков в мокроте и эозинофилов в стенке дыхательных путей при обострениях.
Эпителиальные клетки. Могут активироваться под действием сигаретного дыма и вырабатывать воспалительные медиаторы.
Воспалительные медиаторы
Показано, что у пациентов с ХОБЛ повышаются концентрации многих воспалительных медиаторов, которые привлекают воспалительные клетки из кровотока (факторы хемотаксиса), усиливают воспалительный процесс (провоспалительные цитокины) и вызывают структурные изменения (факторы роста). В табл. 4-3 представлены примеры всех типов медиаторов.

Таблица 4-3. Воспалительные медиаторы, участвующие в патогенезе ХОБЛ
Факторы хемотаксиса:
• Липидные медиаторы: например, лейкотриен B4 (LTB4) привлекает нейтрофилы и T-лимфоциты
• Хемокины: например, интерлейкин-8 (IL-8) привлекает нейтрофилы и моноциты.
Провоспалительные цитокины: например, фактор некроза опухолей α (TNF-α), IL-1 и IL-6 усиливают воспалительный процесс и могут способствовать развитию некоторых системных эффектов ХОБЛ.
Факторы роста: например, трансформирующий фактор роста β (TGF-β) может вызывать развитие фиброза в мелких бронхах.
Дисбаланс в системе протеиназы–антипротеиназы
Существуют убедительные данные о том, что в легких больных ХОБЛ нарушен баланс между протеиназами, расщепляющими компоненты соединительной ткани, и антипротеиназами, защищающими от действия протеиназ. При ХОБЛ повышается уровень нескольких видов протеиназ, образующихся в воспалительных и эпителиальных клетках. Всё большее количество данных указывает на возможность взаимодействия между ферментами рассматриваемой системы. Опосредованное протеиназами разрушение эластина, главного соединительнотканного компонента паренхимы легких, служит важной характерной особенностью эмфиземы и, вероятно, является необратимым.
Особенности воспаления при ХОБЛ и БА
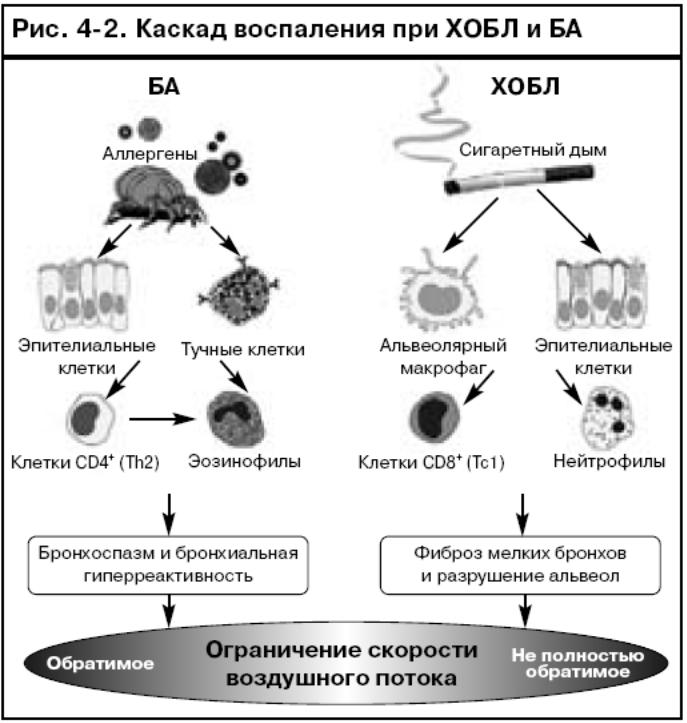
Несмотря на то что и для ХОБЛ, и для БА характерно хроническое воспаление респираторного тракта, в развитии этих двух заболеваний участвуют разные воспалительные клетки и медиаторы, что, в свою очередь, обусловливает различия в физиологических эффектах, симптомах и ответе на терапию (рис. 4-2). Однако при тяжелой БА и ХОБЛ воспаление в легких имеет гораздо больше схожих черт, чем различий. У некоторых пациентов с ХОБЛ имеются признаки БА и возможен смешанный характер воспаления с повышением уровня эозинофилов. И наконец, у курящих больных БА развиваются патоморфологические изменения, типичные для ХОБЛ.
ПАТОФИЗИОЛОГИЯ
В настоящее время достаточно хорошо изучено, как лежащие в основе ХОБЛ процессы приводят к формированию типичных физиологических нарушений и симптомов. Так, например, снижение ОФВ1, в первую очередь, обусловлено воспалением и сужением периферических дыхательных путей, а снижение диффузионной способности легких является результатом разрушения паренхимы при эмфиземе.
Ограничение скорости воздушного потока и воздушные ловушки
Выраженность воспаления, фиброза и экссудации в просвет мелких бронхов коррелирует со степенью снижения ОФВ1 и отношения ОФВ1/ФЖЕЛ, а также, вероятно, с характерным для ХОБЛ ускоренным уменьшением ОФВ1. Такая обструкция периферических дыхательных путей всё сильнее препятствует выходу воздуха из легких в фазу выдоха (так называемые воздушные ловушки), и в результате развивается гиперинфляция. Хотя эмфизема в большей степени связана с нарушениями газообмена, чем со снижением ОФВ1, она также способствует образованию воздушных ловушек при выдохе, особенно при разрушении контактов альвеолярных стенок с мелкими бронхами у пациентов с далеко зашедшим заболеванием. Гиперинфляция приводит к снижению инспираторной емкости, особенно при физической нагрузке (в таком случае говорят о динамической гиперинфляции), в результате появляются одышка и ограничение переносимости физической нагрузки. В настоящее время считают, что гиперинфляция развивается уже на ранних стадиях заболевания и служит основным механизмом появления одышки при нагрузке. Бронхолитики, действующие на периферические бронхи, уменьшают выраженность воздушных ловушек, тем самым уменьшая легочные объемы, улучшая симптомы и переносимость физической нагрузки.
Нарушения газообмена
Нарушения газообмена приводят к гипоксемии и гиперкапнии и при ХОБЛ бывают обусловлены несколькими механизмами. В целом газообмен ухудшается по мере прогрессирования заболевания. Степень тяжести эмфиземы коррелирует со снижением PaO2 в артериальной крови и другими признаками нарушенного вентиляционно-перфузионного отношения (VA/Q). Обструкция периферических бронхов также приводит к нарушению отношения VA/Q; при тяжелом заболевании обструкция сочетается с нарушением функции дыхательных мышц, что способствует снижению вентиляции с последующей задержкой в крови углекислого газа. Нарушение альвеолярной вентиляции и уменьшение легочного кровотока обусловливают дальнейшее прогрессирование дисбаланса VA/Q.
Гиперсекреция слизи
Гиперсекреция слизи, приводящая к хроническому продуктивному кашлю, является характерной особенностью хронического бронхита и не обязательно сочетается с ограничением скорости воздушного потока. Напротив, симптомы гиперсекреции слизи обнаруживаются не у всех пациентов с ХОБЛ. Если гиперсекреция имеется, она обусловлена метаплазией слизистой с увеличением количества бокаловидных клеток и размеров подслизистых желез в ответ на хроническое раздражающее действие на дыхательные пути сигаретного дыма и других вредных агентов. Гиперсекрецию слизи стимулируют различные медиаторы и протеиназы; многие из них действуют путем активации рецептора эпидермального фактора роста (EGFR).
Легочная гипертензия
Легкая или среднетяжелая легочная гипертензия может развиваться уже на поздних стадиях ХОБЛ вследствие обусловленного гипоксией спазма мелких артерий легких, который в конечном счете приводит к структурным изменениям: гиперплазии интимы и позднее гипертрофии/гиперплазии гладкомышечного слоя. В сосудах отмечается воспалительная реакция, сходная с реакцией в дыхательных путях, и дисфункция эндотелия. Обеднение легочного капиллярного кровотока при эмфиземе также может способствовать повышению давления в легочном круге. Прогрессирующая легочная гипертензия может приводить к гипертрофии правого желудочка и в итоге к правожелудочковой недостаточности (легочному сердцу).
Системные проявления
Становится всё более очевидным, что ХОБЛ присущ ряд системных проявлений, особенно при тяжелом заболевании, и что эти проявления оказывают выраженное влияние на выживаемость пациентов и развитие сопутствующих заболеваний (табл. 4-6).

Таблица 4-6. Системные проявления ХОБЛ
• Кахексия
• Потеря скелетной мускулатуры: апоптоз, атрофия от бездействия
• Остеопороз
• Депрессия
• Нормохромная нормоцитарная анемия
• Повышенный риск сердечно-сосудистых заболеваний: связан с повышением уровня CРБ
ОБОСТРЕНИЯ
Обострения представляют собой дальнейшее усиление воспалительной реакции в дыхательных путях пациентов с ХОБЛ; причиной развития обострений могут являться бактериальные или вирусные инфекции или поллютанты окружающей среды. Механизмы воспалительного процесса, участвующие в развитии обострений ХОБЛ, недостаточно изучены. При легких и среднетяжелых обострениях отмечается увеличение в мокроте и бронхиальной стенке количества нейтрофилов, а по данным некоторых исследований и эозинофилов. Это увеличение сопровождается повышением концентраций определенных медиаторов, в том числе TNF-α, LTB4 и IL-8, а также ростом уровня маркеров окислительного стресса. Во время обострения отмечается усиление выраженности гиперинфляции и воздушных ловушек в сочетании со сниженным экспираторным потоком, что приводит к усилению одышки . Кроме того, выявляется усугубление дисбаланса VA/Q, что приводит к тяжелой гипоксемии.
