- •Закон мозлі
- •9 Квантово-механічна модель атома корпускулярно-хвильовий дуалізм
- •Принцип невизначеності
- •Хвильове рівняння шредінгера
- •Хвильові функції та електронні орбіталі
- •Характеристика стану електрона за квантовими числами
- •Атомні ядра склад і будова атомних ядер
- •Властивості взаємодіючих атомів
- •Валентність
- •Метод валентних зв'язків умови утворення ковалентного зв'язку
- •Водневий зв'язок природа й енергія водневого зв'язку
- •Міжчастинкові взаємодії доказ існування міжчастинкових сил
- •Вандерваальсова взаємодія молекул
- •Іонно-молекулярна взаємодія
- •Будова твердого тіла загальна характеристика твердого стану речовини
- •Будова ідеальних кристалів 7.2.1. Основні положення
- •Кристалічна гратка
- •Типи кристалічних ґраток
- •Будова іонних кристалів основні типи кристалічних ґраток іонних сполук
- •Металічний стан і його особливості кристалічна структура металів
- •Хімічний зв'язок у металах
Метод валентних зв'язків умови утворення ковалентного зв'язку
Ковалентний зв'язок зумовлений силами взаємодії атомів з однаковими або близькими значеннями електронегативності, що виникають унаслідок обміну валентними електронами. Зв'язок здійснюється в результаті утворення спільних електронних пар у полі ядер обох атомів.
Хімічний зв'язок утворюється тоді, коли зближення атомів супроводжується зменшенням повної енергії системи. З певним наближенням приймають, що енергія молекули складається з кінетичної і потенціальної енергії електронів і ядер, що взаємодіють між собою. Кінетичну енергію руху ядер при цьому не враховують, бо через велику різницю в масах електрони в молекулах рухаються значно швидше1, ніж ядра. Тому вважають ядра нерухомими, а їх енергію — залежною не від координат, а лише від фіксованої відстані між ними (наближення Борна—Оппенгеймера).
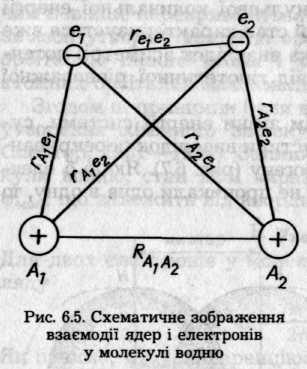
На прикладі молекули водню розглянемо сили, що діють у молекулах і зумовлюють зв'язування атомів. Молекула водню — це система з двох ядер і двох електронів (рис. 6.5). У цій системі виникають такі види взаємодії: відштовхування між ядрами та електронами різних атомів і притягання кожного електрона до обох ядер.
Для характеристики енергії системи застосовують криві потенціальної енергії. Зміна внутрішньої енергії в системі з двох атомів водню залежить від напрямленості спінів взаємодіючих електронів (рис. 6.6). Гайтлер і Лондон показали (1927), що під час зближення двох атомів водню, спіни електронів яких напрямлені паралельно, енергія системи безперервно зростає (верхня крива). У ядерно-електронній взаємодії переважають сили відштовхування, і молекула утворитися не може. При зближенні атомів з антипаралельними спінами між ними спочатку переважають сили притягання, внаслідок чого енергія системи знижується, поки не досягне мінімального значення Еmin, що відповідає між'ядерній відстані (рівноважний стан) г0. Після цього переважають сили відштовхування, що зумовлює різке збільшення енергії, яка при r→0 прямує до нескінченності. Дія двох протилежних сил сумарно виражена нижньою кривою.
У схему утворення хімічного зв'язку необхідно внести поправку: вважати ядра нерухомими в стані з мінімумом енергії не можна — це суперечить принципу невизначеності. Вони здійснюють коливання відносно рівноважних положень, тому енергія молекули фактично більша, ніж у точці мінімуму кривої, на значення нульової коливальної енергії Ео. Звідси Езв = ЯМін- Ео Цей реальний стан характеризується вже середньою між'ядерною відстанню, яка внаслідок асиметрії потенціальної кривої дещо відрізняється від гіпотетичної рівноважної відстані.
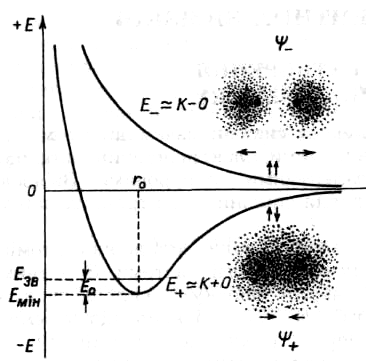
Рис. 6.6. Зміна потенціальної енергії та розподіл електронної густини при утворенні молекули водню
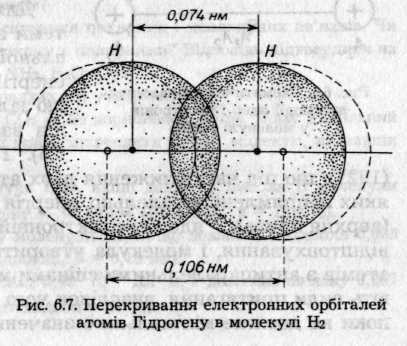
Утворення хімічного зв'язку, окрім зміни енергії системи, супроводжується зміною електронної густини внаслідок перекривання електронних орбіталей атомів Гідрогену (рис. 6.7). Якщо б електронні орбіталі двох атомів Гідрогену не проникали одна в одну, то довжина зв язку мала б дорівнювати 0,053*2 = 0,106 нм. Насправді ж довжина зв'язку в молекулі водню становить 0,074 нм.
Щоб визначити, як саме розподілена електронна густина в молекулі, слід розв'язати рівняння Шредінгера. Однак точний розв'язок рівняння відомий лише для молекулярного іона водню, тобто для системи з двох ядер і одного електрона. Для систем з двома й більшим числом електронів застосовують наближені методи. Найпоширенішими є два квантово-механічні методи обчислення енергії систем з ядер і електронів — метод валентних зв'язків (ВЗ) і метод молекулярних орбіталей (МО). В обох методах багатоелек-тронні хвильові функції для молекули будуються за специфічними правилами з одноелектронних атомних функцій.