
- •Закон мозлі
- •9 Квантово-механічна модель атома корпускулярно-хвильовий дуалізм
- •Принцип невизначеності
- •Хвильове рівняння шредінгера
- •Хвильові функції та електронні орбіталі
- •Характеристика стану електрона за квантовими числами
- •Атомні ядра склад і будова атомних ядер
- •Властивості взаємодіючих атомів
- •Валентність
- •Метод валентних зв'язків умови утворення ковалентного зв'язку
- •Водневий зв'язок природа й енергія водневого зв'язку
- •Міжчастинкові взаємодії доказ існування міжчастинкових сил
- •Вандерваальсова взаємодія молекул
- •Іонно-молекулярна взаємодія
- •Будова твердого тіла загальна характеристика твердого стану речовини
- •Будова ідеальних кристалів 7.2.1. Основні положення
- •Кристалічна гратка
- •Типи кристалічних ґраток
- •Будова іонних кристалів основні типи кристалічних ґраток іонних сполук
- •Металічний стан і його особливості кристалічна структура металів
- •Хімічний зв'язок у металах
Властивості взаємодіючих атомів
Дослідження свідчать, що розподіл електронної густини в об'ємі ізольованого атома відрізняється від розподілу електронної густини того ж атома, який взаємодіє з іншими атомами в хімічній сполуці. Незмінним у сполуці залишається ядро атома та найближчі до нього внутрішні орбіталі — атомний кістяк. Тому найпростішими структурними складовими хімічних сполук є не атоми, а ядра атомів і електрони. Отже, молекула — це фізично стійка система з певного числа ядер і електронів, що закономірно розміщені в просторі та зв'язані хімічним зв'язком за допомогою валентних електронів. Взаємодія між ядрами та електронами всередині молекул значно сильніша, ніж між окремими молекулами. Для утворення хімічного зв'язку мають значення лише електростатичні сили ядерно-електронної взаємодії. Усі інші взаємодії між ядрами та електронами (магнітні, гравітаційні) дуже малі порівняно з ядерно-електронним притяганням і відштовхуванням.
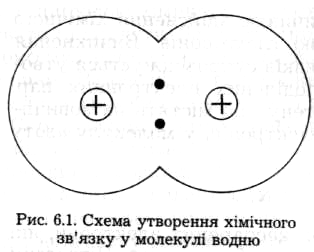
У процесі утворення хімічного зв'язку загальна енергія системи електронів і ядер, що взаємодіють, зменшується. Наприклад, при сполученні двох атомів Гідрогену у молекулу водню виділяється 432,1 кДж/моль енергії. Зменшення енергії зумовлено тим, що електрони одночасно притягаються до двох ядер. У результаті перекривання електронних орбіталей при зближенні атомів у просторі зв'язування густина від'ємного електричного заряду в зоні перекривання підвищується. Позитивно заряджені ядра притягаються в напрямку перекривання орбіталей, що й забезпечує стійкість молекули (рис. 6.1). Причина утворення зв'язку полягає у взаємодії електронів, що володіють протилежними спінами, і ядер атомів, яка й приводить до зменшення енергії системи.
Отже, хімічний зв'язок — це наслідок ядерно-електронної взаємодії, що зумовлює існування хімічних сполук — молекул, іонів, радикалів, кристалів. Характерними рисами хімічного зв'язку є:
зниження повної енергії багатоатомної системи порівняно з енергією ізольованих атомів, з яких вона утворена;
істотний перерозподіл електронної густини у просторі зв'язування порівняно з простим накладанням електронних густин незв'язаних атомів, що перебувають на відстані зв'язку.
Оскільки молекулу розглядають як систему, утворену при взаємодії атомів, ядра яких складають цю систему, то звичайно говорять про хімічний зв'язок не між ядрами атомів, а між атомами, хоч це і менш точно відображає суть хімічного зв'язку.
Мірою здатності елемента до утворення хімічного зв'язку є валентність. Описати хімічний зв'язок — це насамперед з'ясувати, як перерозподіляється електронна густина в молекулі. За характером розподілу електронної густини в речовині розрізняють три основних типи хімічного зв'язку: ковалентний (гомеополярний, атомний), іонний (гетерополярний, електровалентний) і металічний. Крім перелічених типів сильного хімічного зв'язку існує ще слабкий хімічний зв'язок (водневий, вандерваальсовий). Для більшості речовин характерне поєднання різних типів зв'язку.
Основні характеристики хімічного зв'язку визначаються будовою та властивостями взаємодіючих атомів: валентними орбіталя-ми, ефективними радіусами й зарядами, електронегативністю, валентністю та ступенем окиснення, координаційним числом, здатністю поляризувати і поляризуватися.
Хімічний зв'язок здійснюється здебільшого валентними електронами. У s- і р-елементів валентними є електрони зовнішнього рівня, а у d-елементів — це s-електрони зовнішнього і d-електрони передзовнішнього рівнів.
З поняттям валентних електронів тісно пов'язане інше важливе поняття — валентні орбіталі. Валентними орбіталями називають атомні орбіталі, які беруть участь в утворенні хімічного зв'язку.
Електронні оболонки атомів не мають чітко окреслених зовнішніх меж, тому визначити абсолютні розміри ізольованих атомів неможливо. Доводиться мати справу з радіусами атомів, сполучених між собою тим чи іншим хімічним зв'язком. Такі радіуси розглядають як ефективні, бо вони проявляють себе в дії.
Ефективні (відносні) атомні радіуси обчислюють за експериментальними даними про між'ядерні відстані в молекулах чи кристалах (Брегг, 1920; Слейтер, 1964). Половина між'ядерної відстані й відповідає атомному радіусу елемента. Розрізняють ковалентні та металічні ефективні атомні радіуси. Ковалентні радіуси дорівнюють половині між'ядерної відстані в молекулах чи кристалах простих речовин. Металічні радіуси становлять половину відстані між центрами атомів у кристалічній гратці металів. Наприклад, між'ядерна відстань С—С в алмазі дорівнює 0,154 нм, звідки ковалентний ефективний атомний радіус Карбону гс = 0,077 нм.
Для характеристики розмірів катіонів і аніонів у кристалічних сполуках застосовують поняття іонних радіусів. Іонні радіуси — це ефективні радіуси атомів у кристалічних сполуках з переважно іонним зв'язком. Значення іонних радіусів обчислюють, зважаючи на ядерні відстані в іонних кристалах, припускаючи, що останні дорівнюють сумі радіусів катіона та аніона.
Систему іонних радіусів запропонував норвезький геохімік Гольдшмідт (1926). її удосконалювали та доповнювали Полінг (1927), Бєлов, Бокій (1953) та ін. Нині застосовують більш достовірну фізичну систему Шеннона й Пруітта (1970), яка базується на експериментальних рентгенографічних даних про розподіл електронної густини між катіоном і аніоном у структурах кристалів. За радіус катіона (аніона) приймають відрізок на прямій, що з'єднує катіон і аніон, від центра катіона (аніона) до мінімальної електронної густини. У цій системі радіуси аніонів Флюору та Оксигену дорівнюють 0,119 і 0,129 нм відповідно. Іонні радіуси залежать не тільки від електронної конфігурації, але й від координаційного числа іона, при збільшенні якого вони зростають.
Іонні радіуси відрізняються від атомних радіусів. Радіус катіона завжди менший, а радіус аніона — більший, ніж радіус відповідного нейтрального атома. Зокрема, атомний радіус Калію г(К) = = 0,236 нм, а г(К+) = 0,152 нм; г(С1) = 0,060 нм, а г(Сl-) = 0,167 нм.
Вандерваальсові радіуси визначають найкоротші віддалі між незв'язаними атомами. їх знаходять за відстанями між однаковими атомами, що дотикаються в сусідніх молекулах речовини, застосовуючи принцип адитивності.
Розмір оболонки атома можна характеризувати положенням максимуму електронної густини зовнішнього електронного шару. Теоретично обчислену відстань від ядра до головного максимуму електронної густини зовнішньої орбіталі приймають за справжній (орбітальний) радіус атома. Для кожного атома може існувати одне значення орбітального радіуса в нормальному стані й декілька значень у збуджених станах. Оскільки електронну густину обчислюють наближеними методами, то орбітальні радіуси не слід абсолютизувати. З усіх відомих найповнішими є обчислення, виконані Вебером і Кромером (1965).
Якщо атоми утворюють хімічний зв'язок, то їхня електронна густина змінюється. Кількісною характеристикою цієї зміни є ефективний заряд, або зарядове число, атомів δ— реальний заряд (в одиницях заряду електрона) на атомі в сполуці. Його виражають різницею між числом електронів, що оточують даний атом у сполуці, та числом електронів вільного атома (Брегг, 1926). Ефективний заряд є сумою заряду ядра і електронів зв'язаного атома. Він виражає асиметрію електронних орбіталей і носить умовний характер, бо електронна густина делокалізована, її неможливо розділити між ядрами.
Ефективні заряди атомів у сполуках невеликі: позитивний заряд не перевищує 2+, а негативний — 2- . При утворенні молекул електрони ніколи не переходять повністю від одних атомів до інших. Зарядове число слід відрізняти від заряду іона, який має цілочислове значення.
Для характеристики здатності атомів певної сполуки відтягувати на себе електронну густину інших атомів користуються поняттям електронегативностг.. Наприклад, у молекулі хлороводню електронегативність атома Хлору більша, ніж атома Гідрогену, тому Хлор відтягує на себе електронну пару і отримує частковий негативний заряд: СІ02. Електронегативність не має однозначного визначення й чіткого фізичного змісту. Проте електронегативність може характеризувати здатність атомів до поляризації ковалентних зв'язків.
