
- •Глава 13
- •13.1.3. Нахождение в природе, изотопный состав
- •13.1.4. Краткие исторические сведения
- •13.2. Простые вещества
- •13.2.2. Металлический алюминий
- •13.2.3. Металлические галлий, индий и таллий
- •13.3. Сложные соединения элементов 13-й группы
- •13.3.1. Кислородные соединения
- •13.3.1.1. Борный ангидрид
- •13.3.1.2. Оксид алюминия (III)
- •13.3.1.3. Оксиды э2о3 элементов подгруппы галлия
- •13.3.1.4. Борные кислоты, бораты и эфиры
- •13.3.1.5. Гидроксид алюминия, алюминаты и соли алюминия (III)
- •13.3.1.6. Гидроксиды э(он)3 и соли элементов подгруппы галлия
- •13.3.1.7. Соединения элементов в низших степенях окисления
- •13.3.2. Галогениды
- •13.3.2.1. Галогениды бора
- •13.3.2.2. Галогениды алюминия
- •13.3.2.3. Тригалогениды элементов подгруппы галлия
- •13.3.2.2. Моногалогениды элементов подгруппы галлия
- •13.3.2.5. Дигалогениды элементов подгруппы галлия
- •13.3.3. Другие бинарные соединения
- •13.3.3.1. Водородные соединения
- •13.3.3.2. Азотные соединения
- •13.3.3.3. Бориды, карбиды, фосфиды
- •13.3.3.4. Халькогениды
- •13.4. Комплексные и металлоорганические соединения элементов 13-й группы
- •13.4.1. Комплексы бора
- •13.4.2. Комплексы алюминия и элементов подгруппы галлия
- •13.4.3. Металлоорганические соединения
- •13.5. Промышленное получение бора и металлических алюминия, галлия, индия, таллия
- •13.6. Биологическая роль элементов 13-й группы
Ю.Д. Третьяков, Л.И. Мартыненко, А.Н. Григорьев, А.Ю. Цивадзе
Неорганическая химия. Химия элементов
Учебник для вузов: В 2 книгах. Книга II/. – М.: Химия, 2001.
Глава 13
13-Я ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ –
БОР, АЛЮМИНИЙ, ПОДГРУППА ГАЛЛИЯ
13.1.Общая характеристика
13.1.1. Положение в Периодической системе
13-я группа ПС включает бор 5В, алюминий 13Аl и элементы подгруппы галлия - галлий 31Ga, индий 49In, таллий 81Tl. Все они принадлежат к числу так называемых p-элементов - их нейтральные атомы содержат первый (среди элементов данного периода) р-электрон. В табл.13.1 представлены важнейшие характеристики элементов 13-й группы
13.1.2. Строение электронной оболочки, валентность, основные типы химических соединений
Все элементы 13-й группы содержат валентные электроны на двух подуровнях одного электронного уровня (табл.13.1),причем подуровень пs полностью завершен (пs2), а подуровень пр только начинает заполняться (пр1).
Важной особенностью 13-й группы ПС по сравнению с группами 1 - 12, включающими только элементы-металлы, является наличие в ней одного элемента-неметалла (бора)
Химические и физические свойства бора (простого вещества и сложных соединений, в состав которых он входит) сближают его не с алюминием - его более тяжелым аналогом, а с кремнием, расположенным в ПС по диагонали к бору. Здесь действует «правило диагонали»: наблюдается близкая аналогия в свойствах простых и сложных соединений бора, имеющего меньшие размеры атома, но и меньшую степень окисления (+3), и кремния, имеющего большие размеры, но и большую степень окисления (+4).
Другая особенность бора состоит в том, что он находится в левой вершине «треугольника неметаллов» ПС; его соседи слева (бериллий) и снизу (алюминий) обладают металлическими свойствами, и только сосед справа (углерод) является неметаллом. Наконец, бор представляет собой электронодифицитный элемент, и с этим связанны многие необычные свойства боросодержащих соединений: их валентная ненасыщенность, склонность к реакциям присоединения, образованию полимерных соединений с мостиковыми связями.
Неметаллические свойства гомо- и гетероатомных соединений бора обусловлены большой прочностью связи валентных электронов в атоме бора. Например, ПИ1 бора на 2 эВ превышает ПИ1 его электронных аналогов - элементов подгруппы галлия, проявляющих свойства элементов-металлов (см. табл. 13.1). Высокое значение ПИ бора объясняется тем, что на его наружной электронной оболочке (п = 2) находятся 3 электрона (2s22p1), т.е. по сравнению с элементами-металлами Li и Be, предшествующими бору во втором периоде, происходит накопление валентных электронов, оболочка с главным квантовым числом п = 2 приближается к наполовину заполненной, что повышает ее прочность. К тому же ковалентный радиус бора очень мал (0,97 Å), что типично для элементов-неметаллов. Малые размеры атома бора способствуют повышению прочности связи валентных электронов с ядром атома, что делает кристаллический бор полупроводником (большая ширина запрещенной зоны), а в гетероатомных соединениях по той же причине осуществляется ковалентная связь бора с атомами-партнерами. Действительно, отрыв валентных электронов с превращением бора в катион В3+ потребовал бы слишком больших энергетических затрат. Поэтому в соединениях бора, где он проявляет степень окисления +3, реальный положительный заряд на атоме бора значительно меньше, а прочность химических связей обусловлена главным образом ковалентными, а не ионными силами. То же относится к соединениям, в которых бор проявляет степень окисления -3: размер ионов В3- (~2 Å) слишком велик, чтобы содержащие их соединения были устойчивыми.
Таблица 13.1. Важнейшие характеристики элементов 13-й группы
Элемент |
Ar |
Электронная конфигурация изолированного атома* |
Радиус, Å |
Потенциал ионизации, эВ |
ЭО |
Степень окисления** |
||||||
Э0 |
Э+ |
Э3+ |
ПИ1 |
ПИ2 |
ПИ3 |
ПИ4 |
||||||
(КЧ = 6) |
(КЧ = 6) |
|||||||||||
5В |
10,811 |
1s22s22p1 |
0,97а |
|
0,11 |
0,27 |
8,297 |
25,15 |
37,93 |
259,37 |
2,01 |
-3, 0, +3 |
13Al |
26,9816 |
2s22p63s23p1 |
1,43б |
|
0,39 |
0,53 |
5,986 |
18,83 |
28,45 |
119,99 |
1,47 |
0, (+1), +3 |
31Ga |
69,723 |
3s23p63d104s24p1 |
1,39б 1,31в |
1,20 |
0,58 |
0,62 |
5,999 |
20,51 |
30,71 |
64,3 |
1,82 |
0, (+1), +3 |
49In |
114,818 |
4s24p64d105s25p1 |
1,66б 1,48в |
1,40 |
0,76 |
0,80 |
5,786 |
18,87 |
28,03 |
53,9 |
1,49 |
0, (+1), +3 |
81Tl |
204,3833 |
4d104f145s25p65d106s26p1 |
1,71б 1,54а |
1,50 |
1,03 |
0,88 |
6,108 |
20,43 |
29,83 |
|
1,44 |
0, +1, +3 |
* См. примечание к табл. 11.1.
** В скобках приведены менее характерные степени окисления
а Ковалентный радиус
б Атомный радиус
в Ковалентный тетраэдрический радиус
Имея на внешнем электронном уровне 3 валентных электрона, бор может образовывать ковалентные соединения, где он, согласно методу валентных связей, sp2-гибридизован (соединение имеет геометрию плоского треугольника) или sp3-гибридизован (тетраэдр). В обоих случаях происходит «распаривание» 2s2-электронной пары атома бора (рис. 13.1).
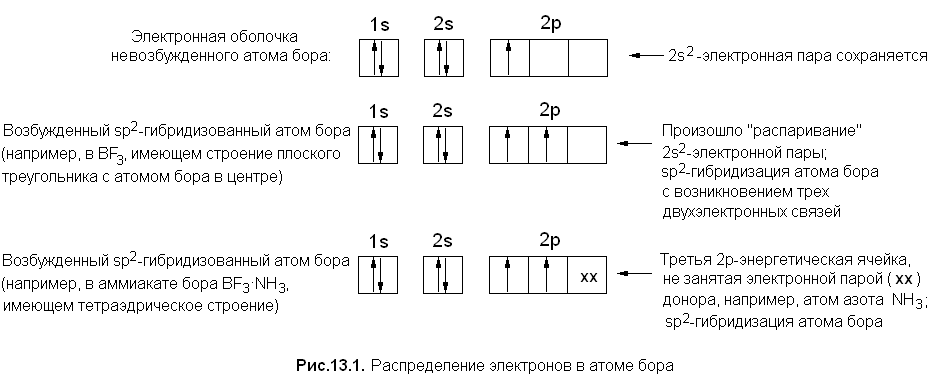
Алюминий также относится к числу р-элементов, так как «собственный» электрон алюминия начинает электронный 3р-подуровень (см. табл. 13.1). Потеряв наружные 3s23p1-электроны, алюминий становится трехзарядным ионом с электронной оболочкой благородного газа (2s22р6), что и определяет валентные отношения алюминия. Ион Аl3+ изоэлектронен ионам соседних по периоду элементов 2-й и 1-й групп ПС Mg2+ и Na+. Однако, благодаря большему заряду ядра атома и большему заряду иона, размеры Аl3+(0,53 Å) значительно меньше размеров ионов Mg2+ (0,72 Å) и Na+ (l,02 Å). Это делает ион Аl3+ сильным поляризатором, и соответственно химическая связь Аl3+ с атомами или ионами, способными поляризоваться, носит в значительной степени ковалентный характер. Однако малополяризующиеся анионы (такие, как F−, О2−) при контакте с Аl3+ не деформируются или только в малой степени подвергаются деформации. Поэтому связь Аl—F, Аl—О обычно носит преимущественно ионный характер. Естественно, что ион Аl3+ - сильный комплексообразователь, причем тип связи в образованных им КС зависит от поляризуемости лиганда. «Жестким» лигандам соответствуют комплексы с ионной связью, «мягким» - с преимущественно ковалентной связью.
Соединения, где алюминий проявляет степень окисления +1, получены, но значительно менее характерны, чем для самого тяжелого элемента 13-й группы - таллия.
Важной особенностью 13-й группы является присутствие в ней постпереходных элементов подгруппы галлия - Ga, In, Tl. Эти три элемента следуют в периодах ПС непосредственно за декадами переходных 3d-, 4d- и 5d- элементов (отсюда и название «постпереходные», или «запереходные», элементы). Как видно из табл. 13.1, элементы подгруппы галлия имеют под валентной (ns2np1) восемнадцатиэлектронную оболочку [(n - 1)s2(n - 1)р6(n - 1)d10] (а Тl еще и 32-электронную), что придает элементам, содержащим такую «подкладку», особые поляризационные свойства, в частности, легкую деформируемость и склонность к проявлению эффекта дополнительной поляризации. Именно этот эффект обусловливает легкую восстанавливаемость тяжелых элементов этой группы, особенно таллия, для которого, в отличие от легких аналогов, в равной степени характерны степени окисления +3 и +1.
Бор и алюминий в соответствии с классической терминологией, предложенной Д.И.Менделеевым, являются «типическими» элементами по отношению к элементам подгруппы скандия и подгруппы галлия, если речь идет о короткой форме ПС.
Спорным является отнесение элементов подгруппы галлия или подгруппы скандия в короткопериодном варианте ПС к побочной или главной подгруппе. Требуемая принципом Менделеева монотонность в изменении кислотно-основных свойств образованных элементами группы оксидов, гидроксидов, солей достигается в том случае, если за бором и алюминием следуют Sc, Y, La. Если же в качестве аналогов бора и алюминия рассматриваются Ga, In, Tl, то после усиления основных свойств соединений от В к Аl наблюдается их ослабление при переходе к Ga - гидроксид Ga(OH)3 более амфотерен, чем Аl(ОН)3. Таким образом, нарушается принцип монотонности изменения свойств при переходе от типических элементов к элементам главной подгруппы, если за таковую принимать подгруппу галлия. Напротив, последовательность В - Аl – Sc – Y - La вполне отвечает требованиям монотонного изменения свойств (усиление основности) в главной подгруппе.
Переход к длиннопериодной форме ПС снимает вопрос об отнесении подгрупп Sc (переходные элементы) и Ga (постпереходные элементы) к главной или побочной, поскольку за основу классификации элементов однозначно принимается электронное строение их изолированных атомов. С этой точки зрения за типическими р-элементами В и Аl в 13-й группе должны следовать р-элементы Ga, In, Тl. Но как в таком случае быть с немонотонным изменением кислотно-основных свойств?
Объективный анализ показывает, что в последующих группах ПС мы встречаемся с таким же нарушением принципа монотонности изменения свойств соединений при переходе от типических элементов к элементам подгрупп германия, мышьяка, селена, брома, криптона, так как элементы соответствующих групп, начиная с подгруппы галлия, принадлежат к числу постпереходных. Их валентным электронам предшествует полностью сформированная 18-электронная легко деформируемая оболочка. Этим постпереходные элементы отличаются от типических, у которых валентным электронам предшествует жесткая, мало деформируемая электронная оболочка типа благородного газа.
Значит, немонотонное изменение химических свойств элементов в 13 - 18 группах, содержащих постпереходные элементы, неизбежно. Эта немонотонность традиционно рассматривается под названием «вторичная периодичность» в группах галогенов и серы, но на самом деле она присуща всем группам, начиная с 13-й, где впервые появляются постпереходные элементы.
Таким образом, длиннопериодный вариант не только не нарушает химических принципов построения ПС, но делает их более общими и обоснованными.
В связи с нахождением валентных электронов на подуровнях ns2np1 все элементы 13-й группы проявляют в своих соединениях степени окисления +3 и +1. Устойчивость соединений со степенью окисления +3 в подгруппе галлия уменьшается от Ga к Тl (а устойчивость соединений со степенью окисления +1 растет), что связано с ростом поляризующего действия ЭIII по мере увеличения их радиуса и появлением у Тl сильно выраженного эффекта дополнительной поляризации. Так, если для Ga наиболее характерна степень окисления +3, то для Тl типична +1. В этом отношении постпереходные элементы противоположны d-переходным, которым свойственно повышение устойчивости соединений с высшей степенью окисления с ростом атомного номера элемента в группе.
Известны также соединения элементов подгруппы галлия, в которых они имеют степень окисления +2, но фактически в них либо существует связь Э—Э, как, например, в монохалькогенидах (см. разд. 13.3.3.4), либо они представляют собой КС, в состав которых входят одновременно атомы в степенях окисления +1 и +3, как, например в «дигалогенидах» ЭI[ЭIIICl4], где Э = Ga, In, Tl.
Для элементов подгруппы галлия характерно КЧ = 4 (sp3-гибридизация) и 6 (sp3d2-гибридизация). Однако в связи с тем, что с ростом порядкового номера элемента возрастает участие d- и f-орбиталей в образовании химических связей, а также благодаря увеличению размера атома и ионов, у Тl встречаются соединения и с более высоким КЧ (например, 7 и 8).
В табл. 13.2 представлены типичные соединения элементов 13-й группы.
Таблица 13.2. Типичные гомо- и гетероатомные соединения элементов 13-й группы
Класс соединений |
Формула |
Элемент, образующий соединение |
Характерные свойства |
Простые вещества |
Э0 |
В |
Неметалл |
Al, Ga, In, Tl |
Металлы |
||
Оксиды |
Э2О3 |
В |
Кислотные свойства (ангидрид борной кислоты) |
Al - Tl |
Амфотерные оксиды, Тl2О3 - окислитель. |
||
Э2О |
Ga |
Летучий оксид. |
|
Гидроксиды |
Э(ОН)3 |
В |
Кислотные свойства (ортоборная кислота) |
Al - Tl |
Амфотерные свойства с преобладанием основных |
||
Соли, полученные твердофаз-ным методом |
(ЩЭ)2Э4О7 (полибораты) |
В |
Проявление кислотных свойств - образование оксоанионов |
(ЩЭ)ЭО2 (алюминаты, галлаты, индаты, таллаты) |
Al - Tl |
Смешанные оксиды |
|
Соли, полученные в водных растворах |
Na[Э(OH)4], Na2Э4O710Н2О |
В |
Гидролиз буры дает щелочную среду |
Э(NO3)3, Э2(SO4)3, ЭХ3 |
Al - Tl |
Растворимые соли, при гидролизе дают кислую среду |
|
Комплексные гидроксосое-динения |
[Э(ОН)6]3−, [Э(ОН)4]− |
Al - In |
Проявляют способность к комплексообразованию из-за амфотерности |
В - In |
|||
КС с моно-дентатными лигандами |
BF3NH3 [Э(ОН2)6]3+ |
В Al - Tl |
Комплексообразование за счет донорно-акцепторных связей |
КС с полидентат-ными лигандами |
Эфиры борной кислоты и глицерина. |
В |
Летучие соединения |
Комплексонаты, β-дикетонаты |
Al - Tl |
Устойчивые хелатные соединения |
