
- •I Физические свойства горных пород-коллекторов нефти и газа
- •II физико-механические и тепловые свойства горных пород
- •§ 1. Напряженное состояние пород в условиях залегания в массиве
- •§ 2. Напряженное состояние пород в районе горных выработок
- •§ 3. Деформационные и прочностные свойства горных пород
- •4. Упругие изменения свойств коллекторов в процессе разработки и эксплуатации нефтяных и газовых месторождении
- •§ 5. Влияние давления на коллекторские свойства пород
- •§ 6. Упругие колебания в породах и их акустические свойства
- •§ 7. Тепловые свойства горных пород
- •Глава III состав и физические свойства природных газов и нефтей
- •§1. Физическое состояние нефти газа при различных условиях в залежи
- •§ 2. Состав и классификация нефтей
- •§ 3. Состав и классификация природных газов
- •§ 4. Газовые смеси Плотность газа
- •Состав газовой смеси
- •Содержание тяжелых углеводородов в газе
- •Парциальное давление и парциальный объем компонента в смеси идеальных газов
- •§5. Жидкие смеси Состав и характеристика жидкой смеси
- •Объем паров после испарения жидкости
- •§ 6. Коэффициент сверхсжимаемости природных газов
- •§ 7. Плотности природного газа, стабильного и насыщенного углеводородного конденсата
- •§ 8. Вязкость газов и углеводородных конденсатов
- •§ 9. Определение изобарной молярной теплоемкости природных газов
- •Пругость насыщенных паров
- •§ 11. Растворимость газов в нефти и в воде
- •§ 12. Давление насыщения нефти газом
- •§ 13. Сжимаемость нефти. Объемный коэффициент
- •§ 14. Плотность пластовой нефти
- •§ 15. Вязкость пластовой нефти
- •§ 16. Структурно-механические свойства аномально-вязких нефтей
- •§ 17. Приборы для исследования свойств пластовых нефтей
- •Установка асм-зоом для исследования пластовых нефтей
- •§ 18. Фотоколориметрия нефти
- •Глава IV фазовые состояния углеводородных систем
- •§ 1. Схемы фазовых превращений углеводородов
- •Поведение бинарных и многокомпонентных систем в критической области
- •§ 2. Критическая температура и критическое давление многокомпонентных углеводородных смесей
- •§ 3. Влагосодержание природных газов и газоконденсатных систем, влияние воды на фазовые превращения углеводородов
- •§ 4. Фазовое состояние системы нефть-газ при различных давлениях и температурах
- •§ 5. Краткая характеристика газогидратных залежей
- •§ 6. Газоконденсатная характеристика залежи. Приборы для лабораторного изучения свойств газоконденсатных смесей
- •Методика исследования на установке уфр-2
- •Исследование проб сырого конденсата и отсепарированного газа
- •§ 7. Расчет фазовых равновесий углеводородных смесей
- •Константы фазовых равновесий
- •Уравнения фазовых концентраций
- •Определение констант фазового равновесия по давлению схождения
- •Аналитический расчет фазовых превращений газоконденсатных смесей при изменении давления и температуры
- •Глава V пластовые воды и их физические свойства
- •§ 1. Состояние остаточной (связанной) воды в нефтяных и газовых коллекторах
- •§ 2. Методы определения количества остаточной (связанной) воды в пластах
- •§ 3. Состояние переходных зон нефть-вода, нефть-газ и вода-газ
- •§ 4. Физические свойства пластовых вод
- •§ 5. Выпадение неорганических кристаллических осадков цз попутно добываемой воды
- •Глава VI молекулярно-поверхностные свойства системы нефть—газ—вода—порода
- •§ 1. Роль поверхностных явлений при движении нефти, воды и газа в пористой среде
- •§ 2. Зависимость поверхностного натяжения пластовых жидкостей от давления и температуры
- •§ 3. Смачивание и краевой угол. Работа адгезии. Теплота смачивания
- •§ 4. Кинетический гистерезис смачивания
- •§ 5. Свойства поверхностных слоев пластовых жидкостей
- •§ 6. Измерение углов смачивания
- •Глава VII физические основы вытеснения нефти водой и газом из пористых сред
- •§ 1. Источники пластовой энергии. Силы, действующие в залежи
- •§ 2. Поверхностные явления при фильтрации пластовых жидкостей. Причины нарушения закона дарси
- •§ 3. Электрокинетические явления в пористых средах
- •§ 4. Дроссельный эффект при движении жидкостей и газов в пористой среде
- •§ 5. Общая схема вытеснения из пласта нефти водой и газом
- •§ 6. Нефтеотдача пластов при различных условиях дренирования залежи
- •§ 7. Роль капиллярных процессов при вытеснении нефти водой из пористых сред
- •§ 8. Использование теории капиллярных явлений для установления зависимости нефтеотдачи от различных факторов
- •§ 9. Зависимость нефтеотдачи от скорости вЫтеснения нефти водой
- •§ 10. Компонентоотдача газовых и газоконденсатных месторождений
- •Глава VIII повышение нефте- и газоотдачи пластов
- •§ 2. Моющие и нефтевытесняющие свойства вод
- •§ 3. Обработка воды поверхностно-активными веществами
- •§ 4. Применение углекислого газа для увеличения нефтеотдачи пластов
- •§ 5. Вытеснение нефти из пласта растворами полимеров
- •§ 6. Щелочное и термощелочное заводнение
- •§ 7. Мицеллярные растворы
- •§ 8. Термические способы увеличения нефтеотдачи
- •§ 9. Условия взаиморастворимости углеводородов оторочки с нефтью и газом
- •§ 10. Извлечение нефти газом высокого давления
- •Список литературы
§ 4. Газовые смеси Плотность газа
Под плотностью или объемной массой тела понимают отношение массы тела в состоянии покоя к его объему.
Плотность газа в нормальных физических условиях может быть определена по его молекулярной массе
![]() ,
кг/м3 (1)
,
кг/м3 (1)
Если плотность газа задана при нормальном давлении, то пересчет ее на другое давление р (при той же температуре) для идеального газа проводится по формуле
![]() (Ш.2)
.
(Ш.2)
.
Часто для характеристики газа применяют относительную плотность его по воздуху при нормальных условиях 0=0:1,293. |
Коммерческие расчеты в газовой промышленности производятся при стандартных физических условиях: давлении 0,1013 МПа и температуре 20 °С.
Состав газовой смеси
Газовые смеси (как и смеси жидкостей и паров) характеризуются массовыми или молярными концентрациями компонентов. Объемный состав газовой смеси примерно совпадает с молярным, так как объем 1 кмоля идеального газа при одинаковых физических условиях, по закону Авогадро, имеет одно и то же численное значение, в частности при О °С и 760 мм рт. ст. равен 22,41 м3.
Для характеристики газовой смеси надо знать ее среднюю молекулярную массу, среднюю плотность в кг/м3 или относительную плотность по воздуху.
Если известен молярный состав смеси в процентах, то средняя молекулярная масса
![]() .
(3)
.
(3)
где у1, у2,…, уn — молярные (объемные) доли компонентов, %;
M1, М2, ..., Мn — молекулярные массы компонентов.
Если задан массовый состав смеси в процентах, то ее средняя молекулярная масса вычисляется по формуле
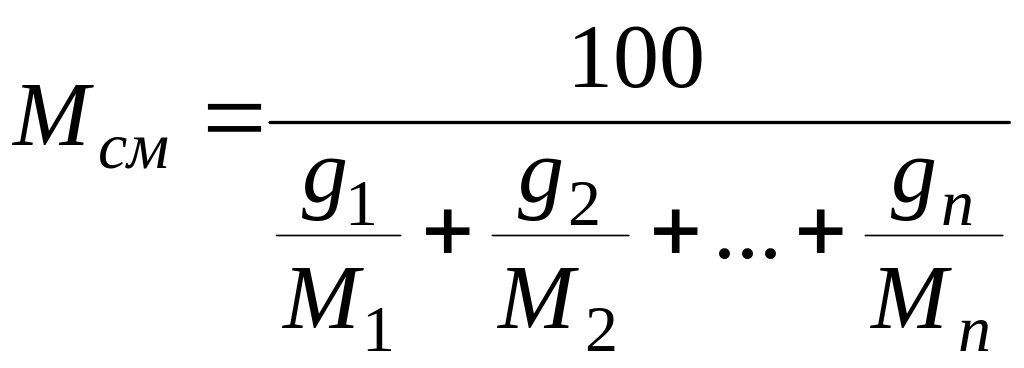 (4)
(4)
где g1, g2, ..., gn — массовые доли компонентов, %.
Плотность смеси см определяют по вычисленному значению средней молекулярной массы Мсм по формуле, аналогичной (1):
![]() .
(5)
.
(5)
Относительную плотность определяют по формуле
![]() (6)
(6)
где рcм и рв — плотность смеси и воздуха при температуре О °С и нормальном давлении.
Содержание тяжелых углеводородов в газе
Для полной характеристики природного газа необходимо также знать содержание в нем тяжелых углеводородов. Принято считать, что в газе три фракции: пропановая, бутановая и газовый бензин, причем последний, для подсчета ресурсов, принимается состоящим из 1/3 бутана и 2/3 пентана (по массе).
Если дан массовый или молярный состав газа, то содержание тяжелых углеводородов определяется по формуле
Gi = 10giсм = 10уii, (7)
где gi — массовая доля данного тяжелого углеводорода в газе, %; cм — средняя плотность природного газа, кг/м3; yi — молярная доля данного тяжелого углеводорода в газе, %; i--плотность данного тяжелого углеводорода, кг/м3.
После определения содержания в газе каждого отдельного углеводорода (пропана, бутана, пентана и высших) делают пересчет на содержание пропана, бутана, газового бензина. Для этого прибавляют к пентану требуемое количество бутана, чтобы получить газовый бензин
Пример. По данному массовому составу газа требуется определить содержание в нем пропана, бутана и газового бензина (в г/м3). Массовый состав газа (в %): метан—19,50; этан—11,80; пропан — 37,95; изобутан — 3,25; н-бутан—12,05; пентан и высшие — 8,15; азот —7,30.
Решение. Для определения средней плотности газа найдем среднюю молекулярную массу газа по формуле (4)
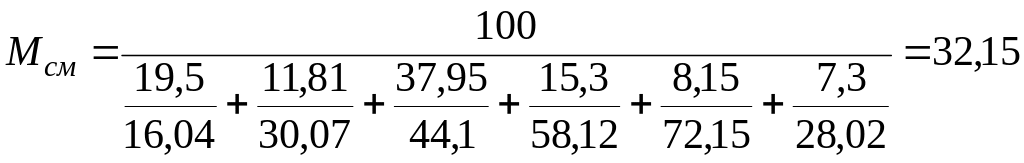
Средняя плотность газа по формуле (5)
![]() кг/м3
кг/м3
Состав газа определим по формуле (7)
пропана 1037,951,43 = 542 г/м3
изобутана 103,251,43 = 46,5 г/м3
н-бутана 1012,051,43=172 г/м3
пентана и высших 108,151,43 = 117 г/м3
Итого: 877,5 г/м3
Газового бензина (пентана две части и н-бутана одна часть) будет 117 +117/2 = 175,5 г/м3
н-бутана 172 —58,5= 113,5 г/м3
изобутана 46,5 г/м3
пропана 542,0 г/м3
Всего тяжелых углеводородов 877,5 г/м3
