
- •Лекция 1 Химия р-элементов.
- •Элементы главной подгруппы VII группы
- •Химические свойства
- •Лекция 2 Элементы VI группы главной подгруппы
- •Кислород и его соединения
- •Распространение в природе
- •Получение
- •Физические свойства серы
- •Химические свойства
- •Соединения серы
- •Сульфид-ион характеризуется сильными восстановительными свойствам
- •Лекция 3 Элементы V группы главной подгруппы
- •Получение аммиака
- •Соединения азота в степени окисления -I
- •Кроме того, они склонны к реакциям диспропорционирования:
- •Лекция 4 фосфор
- •Соединения фосфора Степень окисления -3
- •Лекция 5
- •Элементы уii группы побочной подгруппы
- •Лекция 7 элементы у1 группы побочной подгруппы
- •Лекция 8
- •Гидроксид цинка амфотерен и растворяется как в кислотах. Так и в щелочах
- •Элементы I группы
- •350072, Краснодар, Московская 2а,
- •350058, Краснодар, Старокубанская 88/4, Типография КубГту
│ Министерство образования и науки РФ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Кубанский государственный технологический университет
Кафедра неорганической химии
БОКОВИКОВА Т.Н., МРЧЕНКО Л. А.
ХИМИЯ ЭЛЕМЕНТОВ
(конспект лекций)
Утверждено Редакционно-издательским советом университета в качестве учебного пособия
Краснодар
2011
УДК 541 (075)
Химия элементов/ Конспект лекций : Т.Н. Боковикова, Марченко Л.А.; Кубан. гос. технол. ун-т .- Краснодар: Изд. Куб.ГТУ, 2011.- 58 с.
Содержит конспект лекций по химии элементов. Учебное пособие состав-лено на основе государственного образовательного стандарта направления 206100.
Блиогр. назв. 8
Печатается по разрешению Редакционно-издательского совета Кубанского государственного технологического университета
Рецензенты: д-р хим. наук, проф. Доценко С.П.
канд. хим. наук, доц. Найденов Ю.В.
Содержание
-
Предисловие …………………………………………………………
-
Введение………………………………………………………………
-
Лекция 1. Элементы У11 группы главной подгруппы……………
-
Лекция 2. Элементы У1 группы главной подгруппы …………….
-
Лекция 3. Элементы У группы главной подгруппы. Азот………
-
Лекция 4. Элементы У группы главной подгруппы. Фосфор,
подгруппа мышьяка ………………………………………………..
7. Лекция 5 . Элементы У111 группы побочной подгруппы.
Семейство железа…………………………………………………….
-
Лекция 6 . Элементы У11 группы побочной подгруппы …………
-
Лекция 7 . Элементы У1 группы побочной подгруппы ………….
-
Лекция 8 . Элементы 11 группы побочной подгруппы ………….
-
Лекция 9 . Элементы 1 группы побочной подгруппы ………….
Лекция 1 Химия р-элементов.
Общие закономерности.
Р- элементы -это элементы главных подгрупп III - VIII групп. У р-элеме-нтов валентными являются электроны и орбитали внешнего энергетического уровня. Число внешних электронов равно номеру группы. В периодах с ростом атом-ного номера элемента эффективные атомные радиусы уменьшаются, энергия ионизации, сродства к электрону, электроотрицательность увеличива-ются. В группах с с ростом атомного номера элемента эффективные атомные радиусы увеличиваются, энергия ионизации, сродства к электрону, электро-отрицательность уменьшаются. Однако, не всегда свойства элементов изме-няются монотонно, в характере изменения свойств по периоду проявляется внутренняя периодичность, а в группе - вторичная периодичность. Так, энергия ионизации бериллия больше, чем у бора, азота больше, чем кислорода, что можно объяснить с помощью представлений об экранировании ядра. Эффект экранирования ядра обусловлен электронами внутренних слоев, которые заслоняя ядро, ослабляют притяжение к нему внешнего электрона. Явление вторичной периодичности можно объяснить исходя из представлений о проникновению электронов к ядру, так как в соответствии с квантово-волновой теорией любой электрон некоторое время может находится в области близкой к ядру. Эффект проникновения увеличивает связь внешних электронов с ядром, поэтому при переходе от Si к Ge, от Pb Sn энергия ионизации не уменьшается, а увеличивается.
У р-элементов валентными являются электроны внешнего энергетического уровня. При участии в образовании связи всех валентных электронов элемент проявляет высшую степень окисления, которая равна номеру группы. Энергетически более стабильны соединения, в которых элементы нечетных групп проявляют нечетные степени окисления, а четных групп – четные степени окисления. При переходе от III к VIII группе высшая степень окисления элемента становится все менее устойчивой, что объясняется увеличением энергетического различия между s- и p- орбиталями внешнего слоя атома, а, следовательно, и уменьшением возможности участия в образовании химической связи ns2 –электронов. При этом энергетическое различие между ns и nр- уровнями для элементов 4-го периода выше, чем для
3-го и 5-го. Особенно велико различие между энергиями 6 s и 6р, поэтому для р-элементов 6 периода высшая степень окисления неустойчива.
Элементы главной подгруппы VII группы
В данную подгруппу входят : фтор, хлор, бром, йод и астат.
В ряду : F CI Br I At
Эффективный атомный радиус увеличивается

Энергия сродства к электрону, энергия ионозации, электроотрицательность уменьшаются
 Неметаллические
свойства и окислительная способность
уменьшаются
Неметаллические
свойства и окислительная способность
уменьшаются


Элементы VII группы в невозбужденном состоянии имеют электронную конфигурацию ns2nр5 :
Э0…ns2nр5;
![]()
При возбуждении (кроме фтора ) элементы подгруппы проявляют ковалентность, равную III, V и VII :
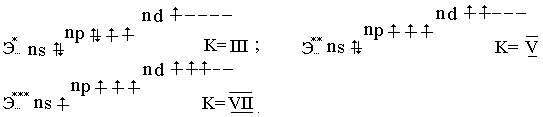
Фтор проявляет степени окисления -1 и 0 , для остальных элементов подгруппы возможны степени окисления : -I , 0, +1, +3,+4, +5 и +7.
Распространение в природе. Наиболее распространенные соединения фтора – флюорит CaF2 , криолит Na3AlF6, фторапатит 3Ca(PO4)2 2CaF2. Хлор содержится в океанской воде, в виде каменной соли NaCl, сильвинита NaCl·KCl и карналлита KMgCl3·6H2O. Бром и иод самостоятельных месторождений не образуют, их добывают из буровых и подземных вод, кроме этого иод добывают из золы морских водорослей. Распространенность галогенов в природе уменьшается от фтора к иоду.
Получение. В лаборатории хлор, бром и йод получают по реакциям :
MnO2 + 4HCI = MnCI2 + CI2 + 2H2O ;
Cl2 + 2КBr = Br2 + 2КCl
Cl2 + 2К J = J2 + 2КCl.
Фтор в промышленности получают исключительно электролизом расплава KF·2HF ( в водном растворе это невозможно , так как фтор реагирует с водой с выделением кислорода). 2F2 + 2H2O = 2HF+O2 .
Хлор
получают электролизом растворов или
расплавов солей: 2NaCl
+2H2O
→ 2NaOH
+2H2
+ Cl2
2NaCl
![]() 2Na
+ Cl2.
2Na
+ Cl2.
Бром и йод получают окисляя в водных растворах ионы Br- и J, хлором, напри-мер: 2NaJ + Cl2 = J20↓ + 2NaCl.
