
- •2.3.1 Фракционный состав
- •2.3.2. Групповой состав
- •2.3.3. Гетероатомные соединения нефти и природного газа
- •2.3.4. Техническая характеристика нефтей
- •2.3.5. Классификация нефтей
- •3. Химизм и механизмы основных процессов технологии природных энергоносителей и углеродных материалов
- •3.1. Термические процессы
- •3.1.1. Термический крекинг и пиролиз углеводородов
- •3.1.2. Сажеобразование
- •3.1.3. Полукоксование и коксование тги
- •3.2. Каталитический крекинг и алкилирование углеводородов
- •3.2.1. Каталитический крекинг
- •3.2.2. Алкилирование парафинов олефинами
- •3.2.3. Алкилирование по ароматическому атому углерода
- •3.3. Процессы, связанные с переносом водорода
- •3.3.1. Гидрирование
- •3.3.2. Риформинг
- •3.3.3. Гидрокрекинг нефтяных остатков
- •3.3.4. Деструктивно-гидрогенизационная переработка тги
- •3.4. Окисление углеродсодержащих веществ
- •3.4.1. Выветривание и самовозгорание углей
- •3.4.2. Окисление и стабилизация топлив и масел
- •3.5. Газификация горючих ископаемых
- •3.6. Синтезы на основе оксида углерода и водорода
3.2. Каталитический крекинг и алкилирование углеводородов
3.2.1. Каталитический крекинг
Каталитический крекинг нефтепродуктов более широко применяется по сравнению с термическим для производства легких моторных топлив. Это вызвано несколькими причинами: получением бензина с более высокими октановыми числами, чем при термическом крекинге, большей удельной производительностью установок каталитического крекинга, более мягкими температурными условиями процесса. Основное отличие каталитического процесса от термического состоит в том, что в присутствии ионных катализаторов наблюдается не гомолитический, а гетеролитический разрыв связей С-С. Происходит изменение механизма с радикально-цепного на ионный, также остающийся цепным. В качестве катализаторов крекинга используют вещества с кислотной функцией типа алюмосиликатов, оксиды алюминия и др. Активные промежуточные частицыљ- ионы карбонияљ- образуются при взаимодействии катализатора с олефинами, которые, хоть и небольшом количестве, могут образовываться вследствие термодеструкции исходного углеводородного сырья:
CnH2n + MOH CnH2n+1+ + MO-.
Ионы карбония CnH2n+1+ неустойчивы и способны распадаться на молекулы олефина и новый ион карбония, с более короткой углеродной цепью. Такой ион достаточно легко отрывает водород в виде гидрид-иона от исходных нейтральных молекул. В результате этой реакции образуется углеводород с короткой цепью, и регенерируется ион карбония. Таким образом развивается цепной процесс расщепления парафинов. Как и в случае радикалов, стабилизация карбокатионов осуществляется за счет сопряжения и сверхсопряжения связей. И те, и другие частицы электронодефицитны, поэтому стабилизирующие их факторы одинаковы. В частности, ряд стабильности катионов такой:
СН3+<R
CH2+<R
CH+![]() R'<
R
C+
R',
R'<
R
C+
R',
![]()
R''
поэтому газ каталитического крекинга отличается по своему составу от газов термического крекинга. Вследствие малой устойчивости частиц СН3+ и С2Н5+ в газах каталитического крекинга преобладают углеводороды С3-С4. Карбокатион менее стабилен, чем радикал равной молекулярной массы и той же структуры, поэтому для него облегчаются реакции изомеризации. Они связаны с перестройкой углеродного скелета молекулы и гидридным переносом. Изомеризация возможна и для радикалов, но в этом случае она происходит более медленно, чем другие реакции с их участием, а поэтому доля изомерных углеводородов среди продуктов некаталитической деструкции мала. В результате изомеризации карбокатиона образуются более разветвленные и, соответственно, более стабильные частицы, например:
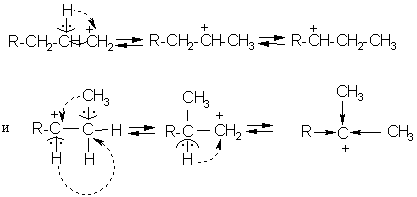
В результате подобных превращений состав продуктов каталитического крекинга обогащен изомерными углеводородами, за счет чего октановое число бензина каталитического крекинга повышено по сравнению с бензином термического крекинга. Этот эффект усиливается вследствие каталитического перераспределения водорода между олефинами и нафтенами, присутствующими в реакционной массе:
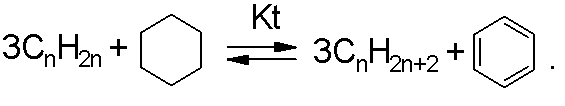
Арены, как и разветвленные парафины, повышают детонационную стойкость моторных топлив, поэтому бензин каталитического крекинга оказывается более высококачественным, чем продукт термического крекинга с тем же интервалом температур кипения. Обрыв цепи происходит при взаимодействии карбокатиона с оснувным центром катализатора, при этом карбокатион теряет протон и превращается в олефин. Каталитический крекинг проводят при температуре 450-480љњС в течение ~1љс, как правило, при атмосферном давлении и разбавлении водяным паром. Это способствует смещению равновесия идущей с увеличением объема реакции в сторону продуктов, а также снижает коксообразование. Осаждение твердых продуктов реакции на активных центрах катализатора отравляет его, и для очистки поверхности кокс выжигают горячим воздухом. Как и в случае термодеструкции, при каталитическом крекинге повышение температуры приводит к увеличению выхода газообразных и снижению выхода жидких углеводородов. При этом средняя молекулярная масса веществ газовой и жидкой фаз снижается, а также увеличивается коксообразование. Ингибиторыљ- соединения с осно'вной функцией, которые могут связывать активные частицы, и уменьшают скорость процесса. Увеличить его скорость можно за счет дополнительного инициирования, используя небольшие добавки олефинов в реакционную массу.
