
- •Обмен и функции углеводов. Переваривание.
- •Гликолиз
- •Цикл Кори
- •Пентозофосфатный путь превращения глюкозы
- •Обмен гликогена
- •Глюконеогенез
- •Регуляция гликолиза и глюконеогенеза в печени
- •Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Переваривание и всасывание жиров
- •Липолиз триглицеридов в жировой ткани
- •Окисление жирных кислот
- •1. Активация жк.
- •2. Транспорт жк внутрь митохондрий.
- •3. Внутримитохондриальное окисление жирных кислот.
- •Окисление жк с нечетным числом углеродных атомов
- •Окисление ненасыщенных жирных кислот
- •Нарушения окисления жирных кислот
- •Обмен ацетил-КоА
- •1.4. Липогенез
- •Регуляция синтеза и распада жирных кислот
- •Метаболизм фосфолипидов
- •Незаменимые жирные кислоты. Эйкозаноиды
- •Обмен холестерина
- •Распространение и функции холестерина
- •Биосинтез холестерина
- •Обмен эфиров холестерина
- •Синтез желчных кислот
- •Регуляция липидного обмена
- •Нарушения липидного обмена
1.4. Липогенез
Липогенез - биосинтез de novo жирных кислот.
1. Карбоксилирование ацетил-КоА и образование малонил-КоА. Фермент - ацетил-КоА-карбоксилаза, содержит биотин.
СО2 + АТФ + биотин-фермент ® карбоксибиотин-фермент + АДФ + ФН
карбоксибиотин-фермент + СН3-СО-SКоА ®
® НООС-СН2-СО-S-КоА + биотин-фермент
малонил-КоА
Мультиферментный комплекс, называемый синтетазой (синтазой) жирных кислот, состоит из 6 ферментов, связанных с ацилпереносящим белком (АПБ). Он имеет две свободные HS-группы.
2. Соединение ацетил-КоА и малонил-КоА с АПБ.
3. Конденсация двух ацетильных остатков.
4. Восстановление карбонильной группы.
5. Дегидратация.
6. Гидрирование. В результате образуется бутирил-АПБ.
Источники НАДФН для синтеза жирных кислот: примерно половину поставляет пентозофосфатный путь окисления глюкозы. Другая половина образуется за счет действия НАДФ-зависимой малатдегидрогеназы.
Пальмитиновая кислота служит предшественником других жирных кислот организма. Удлинение углеродной цепи происходит при участии фермента элонгазы. Ненасыщенные жирные кислоты образуются из насыщенных при участии ферментов десатураз.
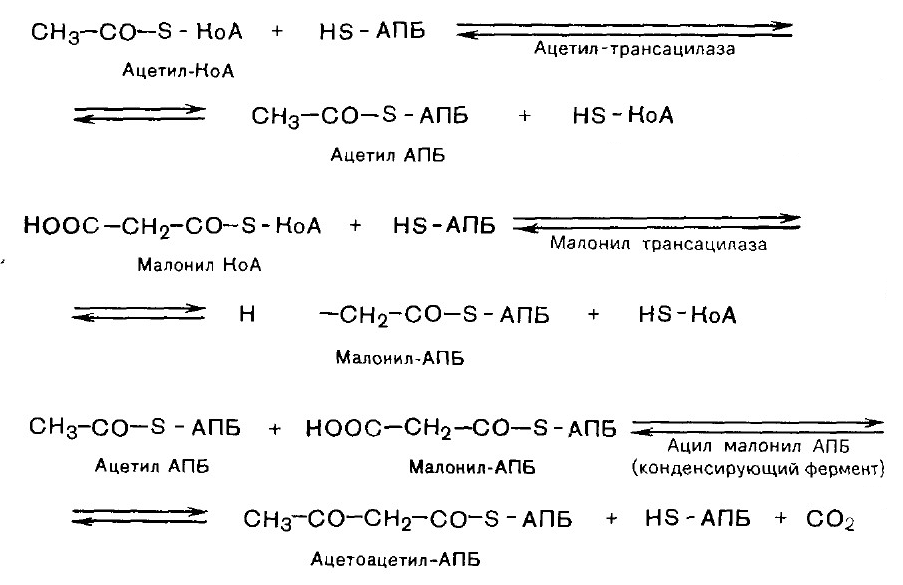
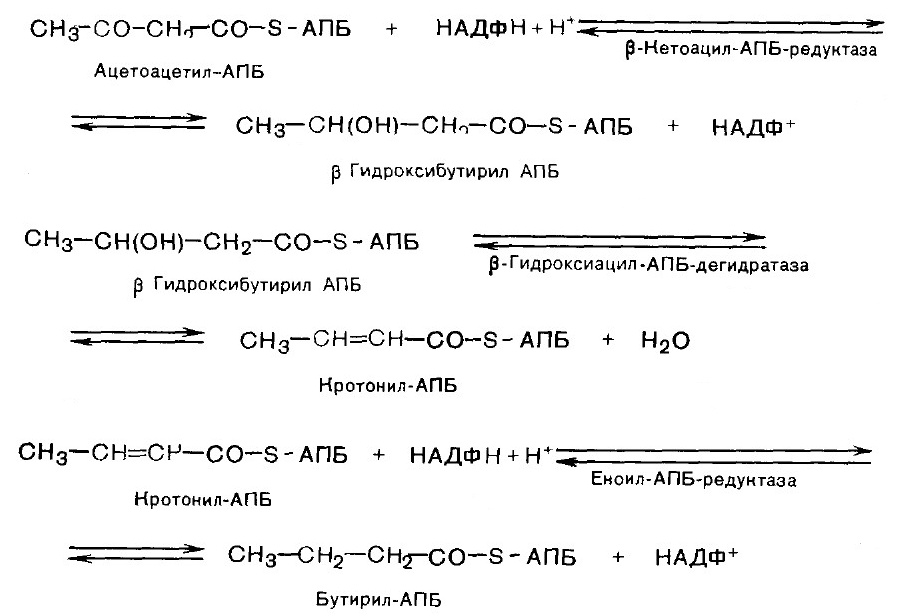
Далее цикл реакций повторяется. На последней стадии происходит гидролиз и освобождение АПБ.
![]()
Регуляция синтеза и распада жирных кислот
Переключение процессов синтеза жирных кислот на их окисление происходит при смене периода пищеварения на постабсорбтивное состояние и осуществляется с помощью регуляторных механизмов.
Важнейшее звено регуляции синтеза жирных кислот - ацетил-КоА-карбоксилаза. В период пищеварения в цитозоле увеличивается концентрация цитрата, который является переносчиком ацетильных остатков из митохондрий. Цитрат - аллостерический активатор ацетил-КоА-карбоксилазы. Ускоряется синтез малонил-КоА и, следовательно, синтез жирных кислот. Конечный продукт – пальмитил-КоА – ингибитор ацетил-КоА-карбоксилазы.
Активность ацетил-КоА-карбоксилазы регулируется глюкагоном и адреналином посредством аденилатциклазной системы. Фосфорилированная форма фермента неактивна, дефосфорилированная – активна. Эти гормоны также путем фосфорилирования переводят липазу в жировой ткани в активное состояние. Следовательно, синтез жирных кислот прекращается, а начинается мобилизация ТАГ, окисление жирных кислот и синтез кетоновых тел.
Регуляторный фермент β-окисления – ацилкарнитинтрансфераза. Его аллостерический ингибитор – малонил-КоА. В постабсорбтивный период, когда поступление ацетильных остатков из митохондрий в цитозоль прекращается, синтез малонил-КоА тоже прекращается, и активируется β-окисление. β-окисление активируется также при активном расходовании АТФ.
Скорость биосинтеза жирных кислот во многом определяется скоростью образования триглицеридов и фосфолипидов.
Метаболизм фосфолипидов
Фосфолипиды не являются существенным энергетическим материалом. Они играют важную роль в организации клеточных мембран, в формировании липопротеиновых комплексов, свертывании крови, иммунологических реакциях, в переносе электронов в дыхательной цепи.
Фосфолипиды распадаются на высшие жирные кислоты, фосфорную кислоту, азотистые основания и глицерин гидролитическим путем. Фосфолипазы относятся к подклассу эстераз (класс гидролаз).
Фосфолипаза А1 атакует эфирную связь фосфолипидов в положении 1. Фосфолипаза А2 катализирует гидролиз эфирной связи в положении 2, образуются свободная жирная кислота и лизофосфолипид. Фосфолипаза A1 локализована в ЭПС, а А2 - в митохондриях. Фосфолипаза С атакует эфирную связь в положении 3, образуется 1,2-диглицерид и фосфорильное основание. Фосфолипаза D катализирует отщепление от фосфолипида азотистого основания.

Наиболее детально изучены фосфолипазы А2. Они содержатся в яде некоторых змей. Действие фосфолипаз на мембраны приводит к существенным изменениям в их функциональной активности.
Дальнейший обмен ВЖК и глицерина рассмотрен ранее. Рассмотрим превращения холина. Одной из важнейших является реакция его ацетилирования:
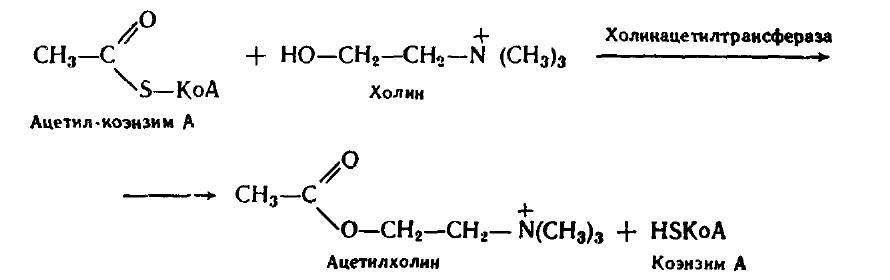
Ацетилхолин участвует в передаче нервных импульсов.
Биосинтез фосфолипидов интенсивно происходит в печени, стенке кишечника, семенниках, яичниках, молочной железе, главным образом в ЭПС клетки.
При синтезе холин- и этаноламинсодержащих фосфолипидов при участии ЦТФ образуются ЦДФ-холин или ЦДФ-этаноламин - реакционноспособные азотистые основания. Затем они реагируют с 1,2-диглицеридами. Фосфатидилхолин (лецитин) может образоваться также из фосфатидилэтаноламина. Донор метильных групп - S-аденозилметионин.
При синтезе инозитсодержащих фосфолипидов при участии ЦТФ образуется ЦДФ-диглицерид - реакционноспособная форма диглицерида, которая затем реагирует с азотистым основанием.
