
- •Обмен и функции углеводов. Переваривание.
- •Гликолиз
- •Цикл Кори
- •Пентозофосфатный путь превращения глюкозы
- •Обмен гликогена
- •Глюконеогенез
- •Регуляция гликолиза и глюконеогенеза в печени
- •Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Переваривание и всасывание жиров
- •Липолиз триглицеридов в жировой ткани
- •Окисление жирных кислот
- •1. Активация жк.
- •2. Транспорт жк внутрь митохондрий.
- •3. Внутримитохондриальное окисление жирных кислот.
- •Окисление жк с нечетным числом углеродных атомов
- •Окисление ненасыщенных жирных кислот
- •Нарушения окисления жирных кислот
- •Обмен ацетил-КоА
- •1.4. Липогенез
- •Регуляция синтеза и распада жирных кислот
- •Метаболизм фосфолипидов
- •Незаменимые жирные кислоты. Эйкозаноиды
- •Обмен холестерина
- •Распространение и функции холестерина
- •Биосинтез холестерина
- •Обмен эфиров холестерина
- •Синтез желчных кислот
- •Регуляция липидного обмена
- •Нарушения липидного обмена
Биосинтез холестерина
Все атомы углерода холестерина происходят из ацетата. Ферментативный синтез холестерина насчитывает более 35 энзиматических реакций. Подавляющая часть холестерина — около 80% -синтезируется в печени (в микросомах), в клетках тонкого кишечника - около 10%, 5% - в клетках кожи. Всего в организме человека за сутки образуется 1,3 г холестерина.
I - превращение активного ацетата в мевалоновую кислоту.
В результате конденсации 2 молекул ацетил-КоА образуется ацетоацетил-КоА, который при взаимодействии с третьей молекулой ацетил-КоА образует β-гидрокси-β-метилглутарил-КоА. Затем в ГМГ-КоА-редуктазной реакции при участии фермента ГМГ-КоА-редуктазы он восстанавливается до мевалоновой кислоты. Эта необратимая реакция лимитирует скорость биосинтеза холестерина.

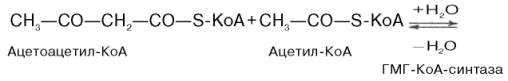

II - образование сквалена из мевалоновой кислоты.
Мевалоновая кислота фосфорилируется при помощи АТФ и участвует в ряде реакций, в результате чего образуется фарнезилпирофосфат (С15). Затем 2 молекулы фарнезилпирофосфата конденсируются и восстанавливаются при участии НАДФН + Н+, образуя сквален (С30).
![]()

III - циклизация сквалена в холестерин под влиянием сквален-оксидоциклазы. Первоначально образуется ланостерин, который затем превращается в холестерин.
Регуляция синтеза холестерина
Основным пунктом регуляции является реакция образования мевалоновой кислоты.
1. Аллостерическая регуляция. Холестерин, а в печени - и желчные кислоты ингибируют ГМГ-КоА-редуктазу.
2. Репрессия синтеза ГМГ-КоА-редуктазы холестерином.
3. Регуляция путем фосфорилирования-дефосфорилирования ГМГ-КоА-редуктазы; активна нефосфорилированная форма. Глюкагон вызывает дезактивацию, а инсулин – активацию путем сложного каскада реакций. Таким образом, скорость синтеза холестерина изменяется при смене абсорбтивного и постабсорбтивного состояний.
4. Скорость синтеза ГМГ-КоА-редуктазы в печени подвержена четким суточным колебаниям: максимальна в полночь, а минимальна - в утренние часы.
Обмен эфиров холестерина
В клетках этерификация холестерина происходит при действии ацил-КоА-холестерин-ацилтрансферазы (АХАТ):
Ацил-КоА + Холестерин НS-КоА + Ацилхолестерин
В клетках образуется в основном линолеилхолестерин. Эфиры находятся главным образом в цитозоле в составе липидных капель. Образование эфиров можно рассматривать, с одной стороны, как механизм удаления из мембран избыточного холестерина, а с другой стороны - как механизм запасания холестерина в клетке. Мобилизация запасов происходит при участии ферментов эстераз, гидролизующих эфиры холестерина:
Ацилхолестерин + Н2О Жирная кислота + Холестерин
Синтез и гидролиз эфиров происходят особенно активно в клетках коры надпочечников.
В липопротеинах крови образование эфиров происходит при участии лецитин-холестерин-ацилтрансферазы (ЛХАТ), катализирующей перенос ацильного остатка с лецитина на холестерин. ЛХАТ образуется в печени, секретируется в кровь и присоединяется к липопротеинам. Наиболее активна ЛХАТ в ЛВП, где она локализована в поверхностном слое. Образующиеся здесь эфиры холестерина гидрофобны и погружаются в липидное ядро. В фосфолипидном монослое освобождается место для холестерина, которое может быть заполнено холестерином из клеточных мембран или из других липопротеинов. Таким образом, ЛВП в результате действия ЛХАТ оказываются ловушкой холестерина.
