
- •М.П. Завгородній, м.М. Корнет, о.А. Бражко, л.О. Омельянчик біоорганічна хімія.
- •Частина 2
- •Тема 8. Гетерофукціональні сполуки (гідроси- та оксокислоти)
- •8.1 Гідроксокислоти
- •Лабораторна робота
- •8.2 Оксокислоти
- •Тема 9. Α-Амінокислоти, пептиди і білки
- •Лабораторна робота
- •Тема 10. Ліпіди
- •Лабораторна робота
- •Тема 11. Вуглеводи
- •11.1 Моноцукриди
- •Лабораторна робота
- •11.2 Дицукриди
- •Лабораторна робота
- •11.3 Поліцукриди
- •Лабораторна робота
- •Тема 12. Нуклеотиди та нуклеїнові кислоти
- •Тема 13. Біологічно важливі гетероциклічні сполуки
- •Лабораторна робота
- •Тема 14. Низькомолекулярні біорегулятори. Терпени
- •Лабораторна робота
- •Тема 15. Низькомолекулярні біорегулятори. Стероїди та алкалоїди
- •15.1 Стероїди
- •15.2. Алкалоїди
- •Лабораторна робота
- •Тема 16. Низькомолекулярні біорегулятори. Антибіотики і вітаміни
- •16.1 Антибіотики
- •Навчальне видання
- •Боорганічна хімія.
Тема 8. Гетерофукціональні сполуки (гідроси- та оксокислоти)
- загальна характеристика гідроксокислот;
- методи синтезу та якісні реакції;
- солеутворення;
- загальна характеристика оксикислот;
- кето-енольна таутомерія.
Основні поняття: методи синтезу гідрокси- та оксосполук, реакція Уфельдмана, реакція розкладання, кето-енольна таутомерія
8.1 Гідроксокислоти
Гідроксикислоти, або оксикислоти, – похідні карбонових кислот, у радикалі яких один або кілька атомів гідрогену заміщені на гідроксильні (спиртові) групи. Іноді їх називають спиртокислотами.
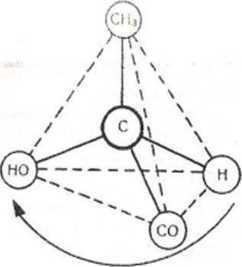
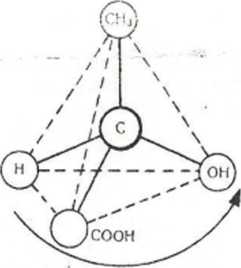
Рис.1 Моделі асиметричних молекул лактатної кислоти
Кількість карбоксильних груп, що містяться в молекулі кислоти, визначає її основність. За кількістю гідроксилів, включаючи гідроксили карбоксильних груп, визначають атомність гідроксикислот. Залежно від кількості карбоксильних груп, що містяться в молекулах таких сполук, розрізняють одно-, двох- і трьохосновні гідроксикислоти. За кількістю гідроксильних груп, що містяться в молекулах цих сполук, розрізняють двох-, трьох- і багатоатомні гідроксикислоти. За місцем розміщення групи –ОН у радикалі розрізняють α-, β-, γ-, σ-гідроксикислоти.
Для гідроксикислот характерна оптична ізомерія. В основу пояснення цього явища покладено уявлення про просторове розміщення атомів і атомних груп у молекулах гідроксикислоти. В молекулі оптичного ізомера є симетричний атом (або кілька атомів) карбону. Це такий атом карбону, кожна валентність якого сполучена з одним із різних атомів або груп атомів. Прикладом такого асиметричного атома може бути атом карбону в центрі молекули 2-оксипропанової («молочної) кислоти (рис. 1). Для 2-оксипропанової кислоти, що має розгорнуту формулу СН3СНОНСООН, існує два оптичних ізомери (правий і лівий – D- і L-) та їх рівнозначна, оптично неактивна суміш – рацемат. Такий вид ізомерії іноді називають дзеркальною, оскільки правий і лівий ізомери однієї й тієї самої гідроксикислоти являють собою дзеркальне відображення один одного. Дзеркальні ізомери оптично активні: один з них обертає площину поляризації світла вправо другий – вліво. їх називають стереоізомерами. Вони є оптичними антиподами.
Гідроксикислоти дуже поширені в природі. Наприклад, 2-оксипропанова (лактатна) кислота – складова частина кислого молока, квашених овочів і фруктів, силосу; 2,3-діоксибутандіова (тартратна) кислота - складова частина багатьох вин, де вона міститься у вигляді калієвих і натрієвих солей, тощо. Окремим гідроксикислотам – 2-оксипропановій (лактатній), 2-оксибутандіоновій (яблучній), 2-оксипропан- 1,2,3-триовій (цитратній), ізоцитратній – належить важлива роль в обміні речовин у циклі трикарбонових кислот Кребса – ЦТК у клітинах живих організмів тощо.
Гідроксикислоти – хімічно активні речовини. Наявність у складі їхніх молекул двох видів функціональних груп (-СООН і -ОН) дає їм змогу легко вступати в різні хімічні реакції,характерні для карбонових кислот, спиртів і типові для самих гідро кислот.
