- •I. Физколлоидная химия
- •1. Физическая химия
- •1.1. Вода
- •1.1.1. Вода как уникальная молекула жизни
- •1.1.3. Буферные растворы
- •1.2. Биоэнергетика клетки
- •1.3. Термохимия
- •1.4. Химическая кинетика и катализ
- •2. Коллоидная химия
- •2.1. Классификация дисперсных систем
- •2.2. Классификация дисперсных систем по агрегатному состоянию дисперсной фазы
- •2.2. Поверхностные явления
- •2.3. Адсорбция
- •2.4. Коллоидные растворы (золи)
- •2.4.1. Характеристика коллоидных растворов
- •2.4.2. Растворы высокомолекулярных соединений
- •II. Биологическая химия
- •3. Белки
- •3.1. Общая характеристика белков
- •3.3. Методы выделения, фракционирования и очистки белков
- •3.3.1. Методы выделения белков
- •3.4. Физико-химические свойства белков
- •3.5. Аминокислоты
- •3.6. Структура белковой молекулы
- •I'm 1.8. Денатурация и ренатурация рибонукле- азы (по Анфинсену):
- •3.7. Классификация белков
- •3.7.1. Простые белки
- •3.7.2. Сложные белки
- •4. Нуклеиновые кислоты
- •4.1. Общая характеристика нуклеиновых кислот
- •4.2. Нуклеотиды и нуклеозиды
- •4.3. Дезоксирибонуклеиновая кислота
- •4.4. Рибонуклеиновые кислоты
- •5. Углеводы 5.1. Общая характеристика углеводов
- •5.2. Моносахариды
- •5.3. Олигосахариды
- •5.4. Полисахариды (глюканы)
- •6. Липиды
- •6.1. Общая характеристика липидов
- •6.2. Простые липиды
- •6.3. Сложные липиды
- •6.4. Двойной липидный слой клеточных мембран
- •Контрольные вопросы и задания
- •7. Витамины
- •7.1. Общая характеристика витаминов
- •7.2. Классификация и номенклатура витаминов
- •7.2.1. Жирорастворимые витамины
- •7.2.2. Водорастворимые витамины
- •8. Ферменты 8.1. Общая характеристика ферментов
- •8.3. Общие свойства ферментов
- •8.4. Активирование и ингибирование ферментов
- •8.2. Участие ионов металлов в активировании ферментов
- •8.5. Классификация и номенклатура ферментов
- •III класс. Гидролазы. Они разрывают внутримолекулярные связи путем присоединения
- •8.6. Применение ферментов
- •9. Гормоны
- •9.1. Уровни регуляции гормонов
- •9.2. Гормоны, выделяемые железами внутренней секреции
- •9.3. Гормоны местного действия
- •11. Обмен углеводов
- •11.1. Переваривание углеводов в пищеварительном тракте
- •11.2. Катаболизм глюкозы
- •11.3. Цикл трикарбоновых кислот
- •11.4. Пентозофосфатный путь окисления глюкозо-6-фосфата
- •11.5. Биосинтез углеводов
- •11.6. Регуляция обмена углеводов
- •12. Обмен липидов
- •12.1. Переваривание липидов в пищеварительном тракте
- •12.2. Промежуточный обмен липидов
- •2. Если синтезируется много сн3—со—КоА, а энергии для синтеза жира недостаточно, то образуется активированная ацетоуксусная кислота:
- •12.3. Биосинтез липидов
- •12.4. Метаболизм стеринов и стеридов
- •13. Обмен белков
- •13.2. Биологическая ценность белков
- •13.3. Особенности переваривания белков у моногастричных животных
- •13.4. Особенности переваривания белков у жвачных
- •13.5. Метаболизм белков в тканях
- •13.6. Особенности обмена отдельных аминокислот
- •13.7. Биосинтез белка
- •14. Обмен нуклеиновых кислот
- •14.1. Переваривание нуклеиновых кислот в пищеварительном тракте
- •14.2. Промежуточный обмен нуклеиновых кислот (распад нуклеиновых кислот в тканях)
- •14.3. Биосинтез нуклеиновых кислот
- •14.4. Рекомбинантные молекулы и проблемы генной
- •15. Обмен воды и солей
- •15.1. Содержание и роль воды в организме
- •15.2. Электролиты тканей
- •15.3. Потребность организма в минеральных веществах, их поступление и выделение
- •16. Взаимосвязь обмена белков, жиров и углеводов
- •17. Биохимия крови
- •18. Биохимия нервной ткани
- •18.1. Химический состав нервной ткани
- •18.2. Обмен веществ в нервной ткани
- •18.3. Химизм передачи нервного импульса
- •19. Биохимия мышечной ткани
- •19.1. Морфология и биохимический состав мышечной ткани
- •19.2. Механизм сокращения мышцы
- •19.3. Окоченение мышц
- •20. Биохимия молока и молокообразования
- •21. Биохимия почек и мочи
- •22. Биохимия кожи и шерсти
- •23. Биохимия яйца
- •Приложение
14. Обмен нуклеиновых кислот
14.1. Переваривание нуклеиновых кислот в пищеварительном тракте
Нуклеиновые кислоты в кормах находятся в виде нуклеопротеидов. В ротовой полости корма подвергаются измельчению, смачиваются слюной. В желудке белки нуклеопротеидов подвергаются действию пепсина, а в кишечнике — трипсина и других протеаз; белки нуклеопротеидов гидролизуются до аминокислот и аминокислоты всасываются.
Процесс расщепления нуклеопротеидов показан на рисунке 14.1.
Нуклеиновые кислоты расщепляются под действием нуклеаз — рибонуклеазы (РНКазы) и дезоксирибонуклеазы (ДНКазы), содержащихся в соке поджелудочной железы. ДНКазы поджелудочной железы — эндонуклеазы — расщепляют ДНК на двухспираль- ные куски, а затем до олигонуклеотидов (содержащих около четы-

рех нуклеотидных остатков) со свободной -ОН группой в 3'- и фосфатной группой в 5'-положениях в остатке дезоксирибозы. Далее гидролиз происходит до образования мононуклеотидов. Нук- леотиды, нуклеозиды и неорганический фосфат всасываются в кровь и поступают в печень.
РНКазы гидролизуют РНК также до образования нуклеотидов нуклеозидов и фосфорной кислоты. Продукты гидролиза нуклеиновых кислот поступают в клетки организма, где используются для синтеза нуклеотидов, нуклеиновых кислот или для удовлетворения энергетических потребностей организма.
14.2. Промежуточный обмен нуклеиновых кислот (распад нуклеиновых кислот в тканях)
В клетках тканей нуклеиновые кислоты распадаются под влиянием нуклеаз. Различают эндонуклеазы и экзонуклеазы Эндонуклеазы гидролизуют фосфодиэфирные связи одновременно во многих участках молекулы нуклеиновых кислот По специфичности действия различают ДНКазы и РНКазы. В результате их действия образуются олигонуклеотиды и лишь небольшое количество мононуклеотидов. Экзонуклеазы отщепляют нуклеотиды с 3'- или 5'-конца, в результате образуются свободные рибонуклеозид или дезоксирибонуклеозид — 3'- или 5'- фосфаты, например:

Рибо- и дезоксирибонуклеозидфосфаты расщепляются до нуклеозидов и фосфорной кислоты (под действием фосфатаз).
Нуклеозиды могут расщепляться и гидролитическим путем с участием фермента нуклеозидазы:

Другие мононуклеотиды подвергаются расщеплению таким же образом.
Пентозы окисляются до СО2 и Н2О; фосфорная кислота используется для фосфорилирования органических соединений или выводится из организма. Азотистые основания превращаются в конечные продукты обмена и выделяются с мочой.
Пурины вначале дезаминируются до гипоксантина и ксантина, затем окисляются до конечных продуктов обмена — мочевой кислоты у человека, обезьян, свиней, птиц и аллантоина у коров, лошадей, собак и кроликов. Мочевая кислота может образовываться из свободных пуринов — аденина и гуанина, а также из соответствующих нуклеозидов и нуклеотидов. Мочевая кислота в печени окисляется до аллантоина:

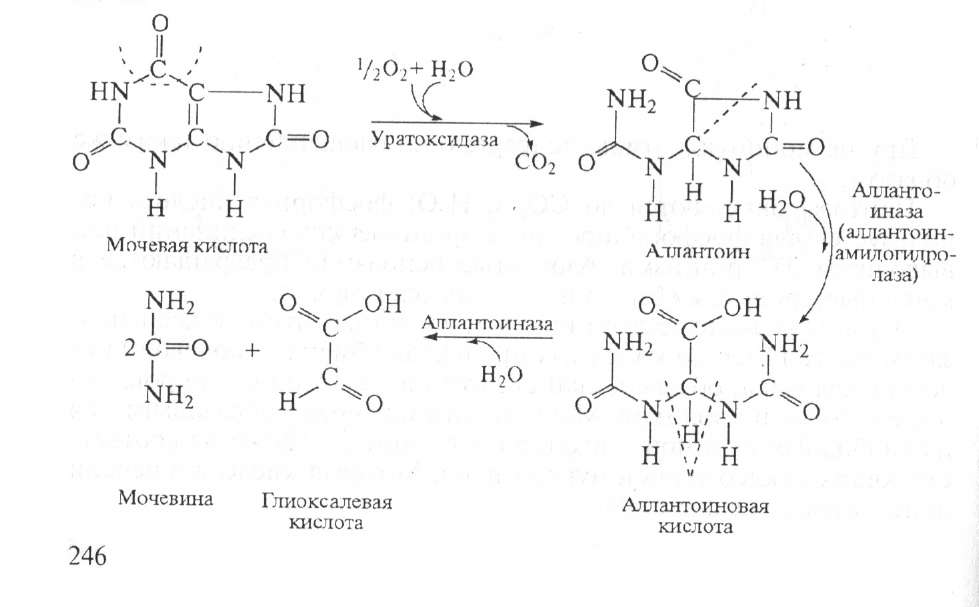
1 уанин под действием фермента гуаназы превращается в ксантин. Мочевая кислота плохо растворяется в воде (1:15 000), и при нарушении обмена нуклеиновых кислот, особенно при избыточном поступлении в организм пуринов, мочевая кислота и ее соли откладываются в виде кристаллов в суставах пальцев, хрящах, в коже и мышцах, образуя узелки. Вокруг узелков развивается очень болезненный воспалительный очаг. Это заболевание известно под названием подагра. У многих животных, кроме млекопитающих (у некоторых рыб, амфибий, морских беспозвоночных) аллантоин может подвергаться дальнейшему расщеплению с образованием аллантоиновой кислоты, а из нее — мочевины и глиоксалевой кислоты:
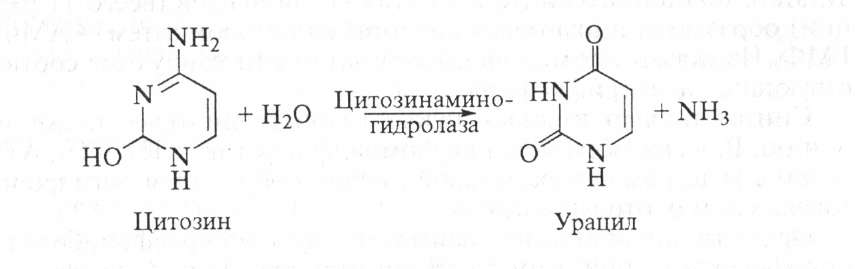
Цитозин дезаминируется под действием фермента дезаминазы с образованием урацила и аммиака, который включается в орнитиновый цикл образования мочевины. Урацил и тимин восстанавливаются в дигидроурацил и дигидротимин, которые далее распадаются с образованием p-уреидпроизводных с выделением аммиака, С02, р-аланина и его метилированного производного:
Распад урацила происходит по схеме, представленной на рисунке 14.2. Распад тимина происходит по такой же схеме.