
- •I. Физколлоидная химия
- •1. Физическая химия
- •1.1. Вода
- •1.1.1. Вода как уникальная молекула жизни
- •1.1.3. Буферные растворы
- •1.2. Биоэнергетика клетки
- •1.3. Термохимия
- •1.4. Химическая кинетика и катализ
- •2. Коллоидная химия
- •2.1. Классификация дисперсных систем
- •2.2. Классификация дисперсных систем по агрегатному состоянию дисперсной фазы
- •2.2. Поверхностные явления
- •2.3. Адсорбция
- •2.4. Коллоидные растворы (золи)
- •2.4.1. Характеристика коллоидных растворов
- •2.4.2. Растворы высокомолекулярных соединений
- •II. Биологическая химия
- •3. Белки
- •3.1. Общая характеристика белков
- •3.3. Методы выделения, фракционирования и очистки белков
- •3.3.1. Методы выделения белков
- •3.4. Физико-химические свойства белков
- •3.5. Аминокислоты
- •3.6. Структура белковой молекулы
- •I'm 1.8. Денатурация и ренатурация рибонукле- азы (по Анфинсену):
- •3.7. Классификация белков
- •3.7.1. Простые белки
- •3.7.2. Сложные белки
- •4. Нуклеиновые кислоты
- •4.1. Общая характеристика нуклеиновых кислот
- •4.2. Нуклеотиды и нуклеозиды
- •4.3. Дезоксирибонуклеиновая кислота
- •4.4. Рибонуклеиновые кислоты
- •5. Углеводы 5.1. Общая характеристика углеводов
- •5.2. Моносахариды
- •5.3. Олигосахариды
- •5.4. Полисахариды (глюканы)
- •6. Липиды
- •6.1. Общая характеристика липидов
- •6.2. Простые липиды
- •6.3. Сложные липиды
- •6.4. Двойной липидный слой клеточных мембран
- •Контрольные вопросы и задания
- •7. Витамины
- •7.1. Общая характеристика витаминов
- •7.2. Классификация и номенклатура витаминов
- •7.2.1. Жирорастворимые витамины
- •7.2.2. Водорастворимые витамины
- •8. Ферменты 8.1. Общая характеристика ферментов
- •8.3. Общие свойства ферментов
- •8.4. Активирование и ингибирование ферментов
- •8.2. Участие ионов металлов в активировании ферментов
- •8.5. Классификация и номенклатура ферментов
- •III класс. Гидролазы. Они разрывают внутримолекулярные связи путем присоединения
- •8.6. Применение ферментов
- •9. Гормоны
- •9.1. Уровни регуляции гормонов
- •9.2. Гормоны, выделяемые железами внутренней секреции
- •9.3. Гормоны местного действия
- •11. Обмен углеводов
- •11.1. Переваривание углеводов в пищеварительном тракте
- •11.2. Катаболизм глюкозы
- •11.3. Цикл трикарбоновых кислот
- •11.4. Пентозофосфатный путь окисления глюкозо-6-фосфата
- •11.5. Биосинтез углеводов
- •11.6. Регуляция обмена углеводов
- •12. Обмен липидов
- •12.1. Переваривание липидов в пищеварительном тракте
- •12.2. Промежуточный обмен липидов
- •2. Если синтезируется много сн3—со—КоА, а энергии для синтеза жира недостаточно, то образуется активированная ацетоуксусная кислота:
- •12.3. Биосинтез липидов
- •12.4. Метаболизм стеринов и стеридов
- •13. Обмен белков
- •13.2. Биологическая ценность белков
- •13.3. Особенности переваривания белков у моногастричных животных
- •13.4. Особенности переваривания белков у жвачных
- •13.5. Метаболизм белков в тканях
- •13.6. Особенности обмена отдельных аминокислот
- •13.7. Биосинтез белка
- •14. Обмен нуклеиновых кислот
- •14.1. Переваривание нуклеиновых кислот в пищеварительном тракте
- •14.2. Промежуточный обмен нуклеиновых кислот (распад нуклеиновых кислот в тканях)
- •14.3. Биосинтез нуклеиновых кислот
- •14.4. Рекомбинантные молекулы и проблемы генной
- •15. Обмен воды и солей
- •15.1. Содержание и роль воды в организме
- •15.2. Электролиты тканей
- •15.3. Потребность организма в минеральных веществах, их поступление и выделение
- •16. Взаимосвязь обмена белков, жиров и углеводов
- •17. Биохимия крови
- •18. Биохимия нервной ткани
- •18.1. Химический состав нервной ткани
- •18.2. Обмен веществ в нервной ткани
- •18.3. Химизм передачи нервного импульса
- •19. Биохимия мышечной ткани
- •19.1. Морфология и биохимический состав мышечной ткани
- •19.2. Механизм сокращения мышцы
- •19.3. Окоченение мышц
- •20. Биохимия молока и молокообразования
- •21. Биохимия почек и мочи
- •22. Биохимия кожи и шерсти
- •23. Биохимия яйца
- •Приложение
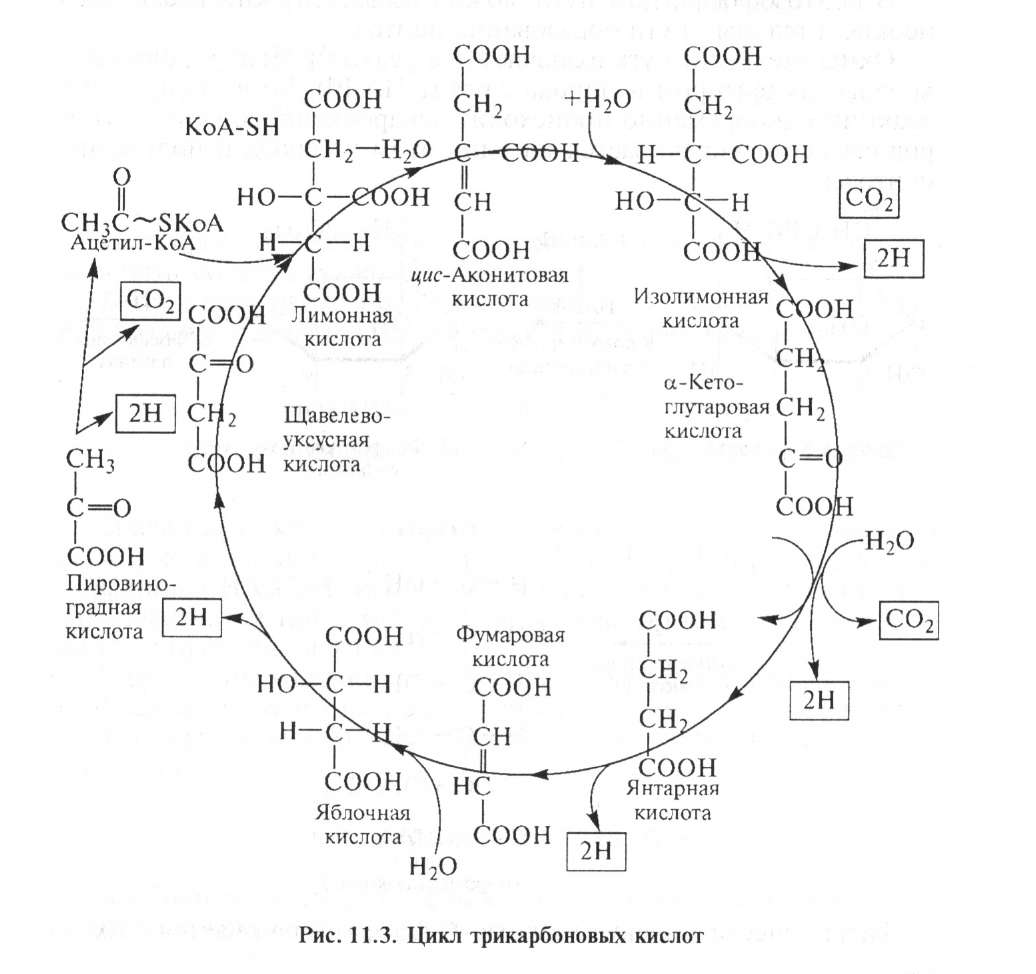
11.3. Цикл трикарбоновых кислот
Цикл трикарбоновых кислот, или цикл Кребса, — это завершающий этап распада энергетических материалов в клетке. При этом активированная уксусная кислота (ацетил-SKoA) — промежуточный метаболит углеводов, белков и липидов — окисляется до конечных продуктов — диоксида углерода, воды и энергии. Реакции цикла трикарбоновых кислот происходят во внутренних отсеках митохондрий.
Митохондрии обычно имеют форму цилиндра с закругленными концами, длиной 1...4 мкм и шириной 0,3...0,7 мкм (рис. 11.2). Число митохондрий в разных клетках различно, например в клетках печени их может быть до 2000.
Система ферментов тканевого окисления (дыхания) расположена на внутренней мембране, где происходит окисление СН3— СО~КоА до конечных продуктов — С02, Н20, с выделением энергии. В цикле трикарбоновых кислот происходит дегидрирование ди- и трикарбоновых кислот, тканевое дыхание и окислительное фосфорилирование, в этих реакциях участвуют ферменты дыхательной цепи и окислительного фосфорилирования.
Реакции цикла трикарбоновых кислот происходят в несколько этапов.


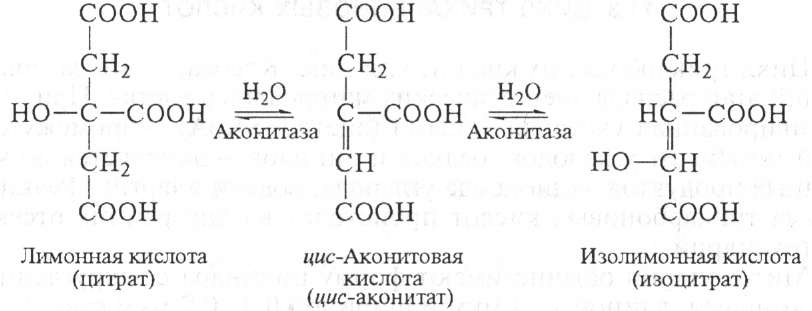
Фермент аконитаза осуществляет отнятие молекулы воды от лимонной кислоты, присоединение молекулы воды к цис-аконитовой кислоте и изомерное превращение цитрата в изоцитрат.
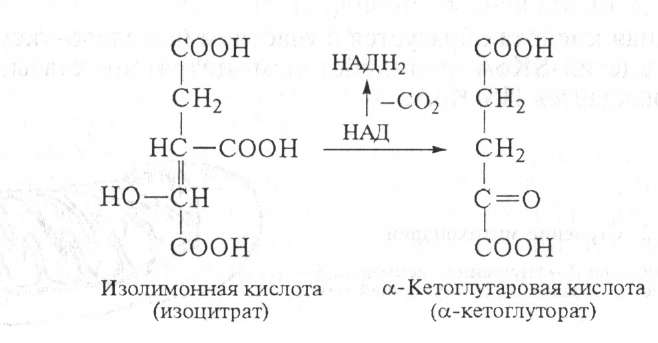
При отщеплении двух атомов водорода от изолимонной кислоты происходит восстановление НАД в НАДН2 (или в НАДФН2), который при окислении в дыхательной цепи обеспечивает синтез трех молекул АТФ.
4. а-Кетоглутаровая кислота под влиянием фермента а-кето- глутаратдегидрогеназы декарбоксилируется, в результате образуется активированная янтарная кислота — сукцинил-КоА, содержащая макроэргическую связь:
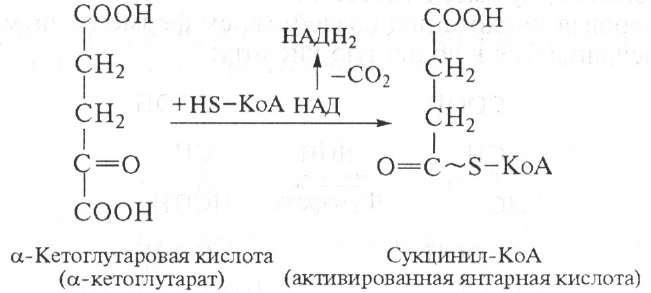
При этом НАД восстанавливается в НАДН2, который в дыхательной цепи обеспечивает синтез трех молекул АТФ.
Расщепление тиоэфирной связи сукцинил-КоА сопряжено с фосфорилированием гуанозиндифосфата (ГДФ):
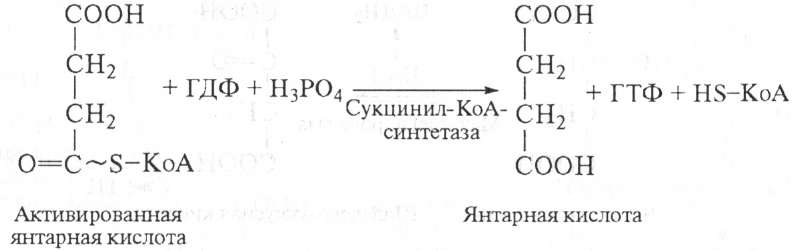
Образовавшийся при этом ГТФ вступает в реакцию перефосфорилирования с АДФ по следующей схеме:
![]()
5. Янтарная кислота под воздействием фермента сукцинатдегидрогеназы окисляется до фумаровой кислоты. Коферментом при этом служит ФАД:

ФАД • Н2 окисляется в дыхательной цепи митохондрий и обеспечивает синтез двух молекул АТФ.
6. Фумаровая кислота под воздействием фермента фумаратгидратазы превращается в яблочную кислоту:
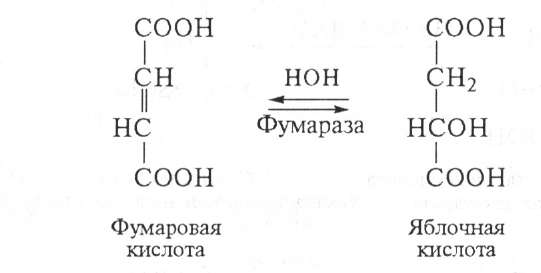
7. Яблочная кислота дегидрируется иод действием фермента малатдегидрогеназы, в результате образуется щавелево-уксусная кислота (ЩУК) и происходит восстановление НАД в НАДН2, последний в дыхательной цепи окисляется и обеспечивает образование трех молекул АТФ:
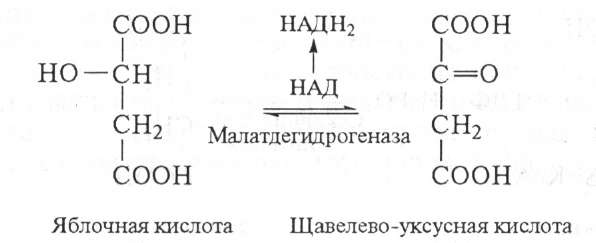
С момента образования щавелево-уксусной кислоты цикл три- карбоновых кислот замыкается и может повторяться в том же порядке: при наличии в системе ацетил-КоА ЩУК снова включается в цикл трикарбоновых кислот.
Суммарная реакция окисления ацетил-КоА в цикле трикарбоновых кислот выглядит следующим образом:
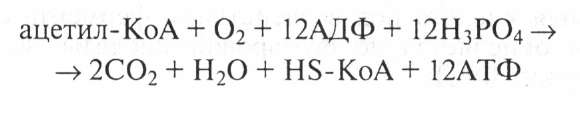
Таким образом, в одном цикле трикарбоновых кислот до конечных продуктов — СО, и Н20 — окисляется одна молекула активированной уксусной кислоты (ацетил-КоА), а энергия, высвобожденная при этом, аккумулируется в 12 молекулах АТФ.
![]()
Из них 24 молекулы АТФ синтезируются в цикле трикарбоновых кислот, 6 — при декарбоксилировании пировиноградной кислоты в ацетил-КоА, 2 — при анаэробном гликолизе, 6 — при окислении НАДН2, образующегося при субстратном окислении фосфоглицеринового альдегида в цитозоле.
