
- •Министерство образования Российской Федерации Московская Государственная Академия Тонкой Химической Технологии им. М.В.Ломоносова
- •Кафедра физической химии.
- •«Расчет химического равновесия»
- •Условия реакции:
- •1. Выбор термодинамических свойств веществ
- •3. Расчет изменения теплоемкости в ходе химической реакции
- •4. Расчет и построение графической зависимости стандартного теплового эффекта реакции от температуры
- •8. Расчет зависимости константы равновесия от температуры
- •9. Расчет изменения стандартной энергии Гиббса и стандартной энтропии реакции
- •10. Расчет парциальных давлений компонентов при заданном начальном составе смеси
- •11. Определение направления процесса при заданных условиях
- •12. Определение влияния давления на смещение равновесия Для определения влияния давления на смещение равновесия рассчитаем
- •13. Определение равновесных парциальных давлений
8. Расчет зависимости константы равновесия от температуры
Исходным уравнением для расчета константы равновесия при разных температурах является изобара Вант-Гоффа:
d lnKp = ΔrH°
dT RT²
Проинтегрируем уравнение Вант-Гоффа с учетом зависимости теплового эффекта реакции от температуры в виде степенного ряда:
lnKp = lnKj +∫(-180906,584-112,46*Т+0,18887*Т2+0,00006013*Т3 + 150000/T)dT/RT²
Полученное уравнение содержит lnKj – константу интегрирования, рассчитаем ее, используя для этого значение lnKp,298.
lnKj = (∫(-180906,584-112,46*Т+0,094435*Т2+0,00020043*Т3 – 150000/T)dT / RT²) –lnKp, где Т=298.15 К.
LnKj = 40,436419
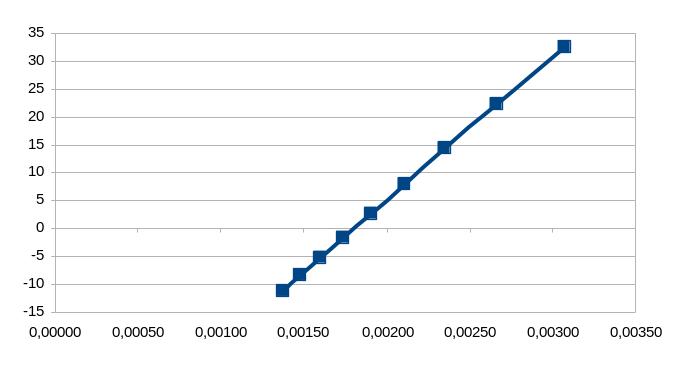
Вычислим значения lnKp и Kp в интервале температур (Т-200) ÷ (Т+200) с шагом 50 градусов и построим график в координатах lnKp от 1/Т. Полученный график используем для обсуждения влияния температуры на смещение равновесия в рассматриваемой реакции.
Т |
1/Т |
lnKp |
325 |
0,003077 |
32,63144 |
375 |
0,002667 |
22,31589 |
425 |
0,002353 |
14,33034 |
475 |
0,002105 |
7,96019 |
525 |
0,001905 |
2,75856 |
575 |
0,001739 |
-1,56893 |
625 |
0,001600 |
-5,22438 |
675 |
0,001481 |
-8,35140 |
725 |
0,001379 |
-11,05498 |
9. Расчет изменения стандартной энергии Гиббса и стандартной энтропии реакции
Воспользуемся уравнениями: ΔrG°т = -RTlnKp , ΔrG°т = ΔrH°т - TΔrS°т
и полученными значениями lnKp и ΔrH°т, рассчитанными для предложенного интервала температур (Табл.2). Рассчитаем значения ΔrG°т (Дж/моль) и ΔrS°т (Дж/моль·К) в том же интервале температур.
Таблица № 2
T |
1/T*10–3 |
rHT |
LnKp |
Kp |
rGT |
rST |
1100 |
0,00091 |
144170 |
0,45 |
1,58 |
-4158,5 |
134,84 |
1150 |
0,00087 |
144274 |
1,14 |
3,13 |
-10903,1 |
134,94 |
1200 |
0,00083 |
144367 |
1,77 |
5,87 |
-17651,9 |
135,02 |
1250 |
0,00080 |
144456 |
2,35 |
10,47 |
-24404,6 |
135,09 |
1300 |
0,00077 |
144544 |
2,88 |
17,87 |
-31160,7 |
135,16 |
1350 |
0,00074 |
144638 |
3,38 |
29,33 |
-37920,3 |
135,23 |
1400 |
0,00071 |
144741 |
3,84 |
46,48 |
-44683,6 |
135,30 |
1450 |
0,00069 |
144860 |
4,27 |
71,37 |
-51450,8 |
135,39 |
1500 |
0,00067 |
144998 |
4,67 |
106,55 |
-58222,4 |
135,48 |
Можно сделать вывод, что при увеличении температуры стандартный тепловой эффект, lnKp, константа равновесия (Кр) и стандартная энтропия увеличиваются, а стандартная энергия Гиббса реакции убывают.
