
- •Глава 5
- •5.1. Внутренняя энергия. Внутренняя энергия
- •5.2. Термодинамическое взаимодействие тел
- •5.2.1. Термодинамическая работа
- •5.2.2. Теплота
- •5.3. Первое начало термодинамики
- •5.4. Теплоемкость. Теплоемкость идеального газа
- •5.5. Адиабатный процесс
- •5.6. Распространение звуковой волны в газе
- •5.7. Круговые процессы. Тепловые машины
- •5.8. Цикл Карно. Идеальная тепловая машина
5.3. Первое начало термодинамики
Опыт показывает, что в общем случае при термодинамическом взаимодействии внутренняя энергия системы будет изменяться как за счет совершения работы над системой, так и за счет теплоты, получаемой системой. Тогда при бесконечно малом изменении состояния будем иметь
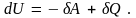 (5.8)
(5.8)
Это равенство выражает собой первое начало термодинамики в дифференциальной форме. Как уже было сказано, этот закон формулируется на основе обобщения опытных фактов. Однако к равенству (5.8) можно прийти и непосредственно из квантового статистического определения внутренней энергии, т.е. из равенства (5.1). Продифференцировав это равенство по переменным и , получим
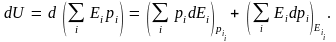
Индексы
у скобок здесь обозначают те переменные,
которые считаются постоянными при
взятии частной производной по другой
переменной. Как видим, элементарное
приращение внутренней энергии естественным
образом представилось в виде двух
слагаемых. Первое слагаемое, очевидно,
представляет собой элементарную работу,
совершаемую над системой,
 а второе – элементарную теплоту
,
полученную системой. Тем самым мы
приходим к равенству (5.8). Проведенные
рассуждения следует рассматривать ни
как вывод первого закона термодинамики
(он, как отмечалось выше, формулируется
на основе обобщения опытных фактов), а
как статистическое обоснование этого
закона. С точки зрения квантовой
статистической физики изменение
внутренней энергии происходит за счет
двух факторов - изменения уровней энергии
системы и изменения распределения
вероятностей состояний системы.
а второе – элементарную теплоту
,
полученную системой. Тем самым мы
приходим к равенству (5.8). Проведенные
рассуждения следует рассматривать ни
как вывод первого закона термодинамики
(он, как отмечалось выше, формулируется
на основе обобщения опытных фактов), а
как статистическое обоснование этого
закона. С точки зрения квантовой
статистической физики изменение
внутренней энергии происходит за счет
двух факторов - изменения уровней энергии
системы и изменения распределения
вероятностей состояний системы.
Если работа совершается самой системой, то в равенстве (5.8) элементарная работа должна стоять со знаком плюс. В интегральной форме (при конечном изменении состояния) первый закон термодинамики имеет вид
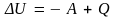 (5.9)
(5.9)
Соотношение (5.9) можно привести к виду
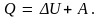 (5.10)
(5.10)
Соотношение (5.10) означает, что теплота, полученная системой, идет на увеличение ее внутренней энергии системы и на совершение системой работы против внешних сил.
Выразив
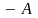 из (5.10), получим еще одну формулу первого
закона термодинамики:
из (5.10), получим еще одну формулу первого
закона термодинамики:
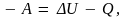 (5.11)
(5.11)
из которой следует, что в результате выполнения над системой работы увеличивается ее внутренняя энергия и выделяется вовне теплота.
Первое начало термодинамики можно записать также и в виде
 (5.12)
(5.12)
Это
равенство показывает, что система может
совершить работу только за счет
расходования своей внутренней энергии
и подвода к ней теплоты. И если
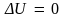 и
и
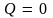 ,
то и
,
то и
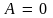 .
Если учесть также, что механическая
работа
.
Если учесть также, что механическая
работа
 где E
– полная механическая энергия, и
при
где E
– полная механическая энергия, и
при
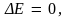 то можно сформулировать общее утверждение:
не возможно произвести работу, не
расходуя никакой энергии и не получая
извне теплоты. Поэтому первый закон
термодинамики можно сформулировать в
виде утверждения о невозможности вечного
двигателя первого рода – устройства,
которое совершало бы работу не расходуя
никакой энергии и не получая извне
тепла.
то можно сформулировать общее утверждение:
не возможно произвести работу, не
расходуя никакой энергии и не получая
извне теплоты. Поэтому первый закон
термодинамики можно сформулировать в
виде утверждения о невозможности вечного
двигателя первого рода – устройства,
которое совершало бы работу не расходуя
никакой энергии и не получая извне
тепла.
Уравнение (5.11) и эквивалентные ему уравнения (5.8) – (5.10) представляют собой закон сохранения и превращения энергии в общей форме. Действительно, выражение (5.8) определяет полное изменение энергии, которое может происходить как за счет тепловых воздействий, когда внешние параметры системы фиксированы, так и за счет работы, когда внешние параметры изменяются под действием так называемых обобщенных сил, которые могут иметь самую различную природу (силы механические, электрические и др.). Кроме того, из этого уравнения следует, что теплота и работа не только могут превращаться во внутреннюю энергию системы, но и друг в друга.
