
5. Рівняння адсорбції Гіббса
Джозеф Гіббс використав закони термодинаміки до повіерхневих явищ і, не виявляючи природи сил, що приводять до адсорбції речовин на границі розділу фаз і механізма явища, вивів рівняння залежності адсорбції від поверхневого натягу при зміні концентрації розчину.
Математичний вираз рівняння Гіббса такий:
Г
= –
![]() ,
,
де Г – надлишкова концентрація (адсорбція) розчиненої речовини, моль/м2; С – її молярна концентрація, моль/л, – поверхневий натяг розчину, Дж/м2.
Це рівняння використовується для ідеальних розчинів (дуже розбавлених розчинів неелектролітів). Для реальних розчинів замість концентрацій треба вживати активність:
Ррр
Для газів замість концентрацій підставляють рівноважні тиски:
Ррр
Рівняння Гіббса універсальне і справедливе для всіх адсорбційних процесів, але поверхневий натяг можна визначати тільки для рідин, тому воно використовується саме у випадках адсорбції на поверхні поділу рідина − рідина або рідина − газ.
Приклад 2. Знайти адсорбцію в моль/см2 пеларгонової кислоти С8Н17СООН при 10 °С, якщо початкова концентрація її в розчині 50 мг/л. Поверхневий натяг води при даній температурі дорівнює 74·10–3 Дж/м2, а розчину вказаної концентрації — 57,0 ·10–3 Дж/м2.
Розв’язання:
СМ – ?
М = 158 г/моль; СМ = 0,05:158 = 3,2·10–4 моль/л.
Г – ?
Використовуємо формулу рівння Гіббса
Г
=
–
![]() = –
= –
![]() = + 7,2
10−6
моль/м2.
= + 7,2
10−6
моль/м2.
[Г]
=
![]() Оскільки Г
> 0
і σ2
< σ1,
то адсорбція позитивна.
Оскільки Г
> 0
і σ2
< σ1,
то адсорбція позитивна.
Відповідь: Г = 7,2 10−6 моль/м2.
Приклад 3. При 293 К поверхневий натяг ртуті становить 0,4580, а амальгами калію (С = 0,11 моль/л) − 0,3926 Дж/м2. Визначити адсорбцію калію на поверхні ртуті.
Розв’язання:
1. Г − ?
В
рівнянні (2) можна замінити похідну
![]() на
на
![]() .
.
Г
=
–
= –
![]() = +
2,68
10−9
моль/м2.
= +
2,68
10−9
моль/м2.
[Г]
=
![]()
Відповідь: Г = 2,68 10−9 моль/м2.
За
рівнянням Гіббса можна обчислити
адсорбцію розчиненої речовини при
різних концентраціях. Для цього будують
графік залежності поверхневого
натягу від концентрації. Необхідні
значення
![]() знаходять
графічно. Для цього до точок, що
відповідають різним концентраціям С1,
С2,
С3
і т.д., проводять дотичні;
знаходять
графічно. Для цього до точок, що
відповідають різним концентраціям С1,
С2,
С3
і т.д., проводять дотичні;
з
 а
кутами нахилу їх до вісі абсцис визначають
тангенси кутів tg
=
.
Перемноживши одержані значення tg
на С/RT
одержують Г,
за якими можна побудувати повну
криву
Г=
f(C)
– ізотерму адсорбції,
з якої потім знайти адсорбцію за іншими
концентраціями
(рис. 1).
а
кутами нахилу їх до вісі абсцис визначають
тангенси кутів tg
=
.
Перемноживши одержані значення tg
на С/RT
одержують Г,
за якими можна побудувати повну
криву
Г=
f(C)
– ізотерму адсорбції,
з якої потім знайти адсорбцію за іншими
концентраціями
(рис. 1).
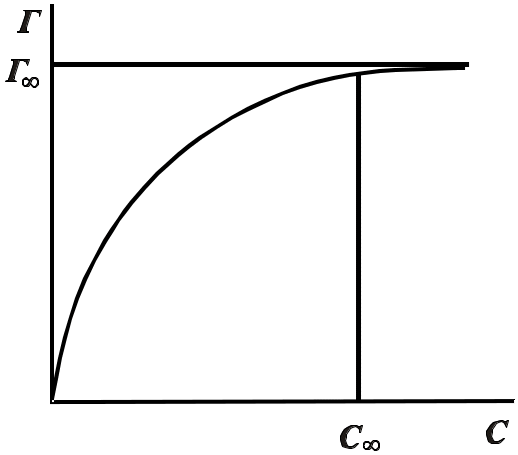
Рис. 1. Визначення надлишкової адсорбції
Зі збільшенням концентрації адсорбція зростає до певної межі, деякого максимального (граничного) значення Г. За величиною Г можна одержати відомості про будову адсорбційного шару.
З рівняння Гіббса випливає, що основною характеристикою адсорбата є величина , але вона змінюється при зміні концентрації. Звичайно використовують її граничне значення при С→ 0, яке називається поверхневою активністю.
g = –( )C→0 (Дж·м/моль).
Чим більше зменшується поверхневий натяг з зростанням концентрації адсорбата, тим більше його поверхнева активність.
Приклад 4. Побудувати ізотерму адсорбції масляної кислоти на поверхні розділу водний розчин − повітря при 283 K та концентрації С = 0,104 моль/л, використавши наступні експериментальні дані.
Сі, кмоль/м3 0,00 0,021 0,050 0,104 0,246 0,489
і103, Дж/м2 74,01 69,51 64,30 59,85 51,09 44,00
Задачу вирішити розрахунковим та графічним способом.
Розвۥязання:
Розрахунковий спосіб.
1. і −? DСі −? Сі/і−? Гі =?
Складемо таблицю розрахунків.
№ |
sі Дж/м2 |
і =s0 − sі Дж/м2 |
Сі кмоль/м3 |
Сі = С0 − Сі |
і/ Сі |
Сі/RT
|
Гі = – 103 |
1 |
69,51 |
4,5110−3 |
0,021 |
−0,021 |
−0,215 |
0,009 |
0,002 |
2 |
64,30 |
9,4710−3 |
0,050 |
−0,050 |
−0,19 |
0,021 |
0,004 |
3 |
59,85 |
14,1610−3 |
0,104 |
−0,104 |
−0,136 |
0,044 |
0,006 |
4 |
51,09 |
22,9210−3 |
0,246 |
−0,246 |
−0,093 |
0,104 |
0,01 |
5 |
44,00 |
30,0110−3 |
0,489 |
−0,489 |
−0,061 |
0,208 |
0,013 |
