
- •Методичні вказівки
- •Контрольна робота №1 Завдання №1
- •Завдання №2
- •Завдання №3
- •Завдання №4
- •Завдання №5
- •Завдання №6
- •Завдання №7
- •Завдання №8
- •Завдання №9
- •Завдання №10
- •Завдання №11
- •Завдання №12
- •Завдання №13
- •Завдання №14
- •Завдання №15
- •Завдання №16
- •Завдання №17
- •Завдання №18
- •Завдання №19
- •Завдання №20
- •Завдання №21
- •Завдання №22
- •Завдання №23
- •Завдання №24
- •Завдання №25
- •Завдання №26
- •Завдання №27
- •Завдання №28
- •Завдання №29
- •Завдання №30
- •Додаткові завдання Задача 1
- •Задача 2
- •Задача 3
- •Задачі 4, 5
- •Задачі 6 – 8
- •Задачі 9 – 11
- •Задачі 12, 13
- •Задачі 14 – 17
- •Задача 18
- •Задача 19
- •Задачі 20, 21
- •Задача 20
- •Задача 21
- •Завдання для варіантів 1-10
- •Завдання для варіантів 11-20
- •Завдання для варіантів 21-30
- •Контрольна робота №2 Завдання №1
- •Завдання №2
- •Завдання №3
- •Завдання №4
- •Завдання №5
- •Завдання №6
- •Завдання №7
- •Завдання №8
- •Завдання №9
- •Завдання №10
- •Завдання №11
- •Завдання №12
- •Завдання №13
- •Завдання №14
- •Завдання №15
- •Завдання №16
- •Завдання №17
- •Завдання №18
- •Завдання №19
- •Завдання №20
- •Завдання №21
- •Завдання №22
- •Завдання №23
- •Завдання №24
- •Завдання №25
- •Завдання №26
- •Завдання №27
- •Завдання №28
- •Завдання №29
- •Завдання №30
Завдання №15
Теоретичні основи та основні показники електрохімічних виробництв.
Технологічна схема синтезу карбаміду.
Негашене вапно містить 95% СаО, 1% СО2, 4% домішок. Утворюється вона випалом вапняку, що містить 89% СаСО3. Визначити витратний коефіцієнт по вапняку на 1 т вапна вказаного складу та ступінь випалу вапняку.
В одноступінчатому реакторі ідеального витіснення з фільтруючим шаром ванадієвого каталізатора проводиться каталітичне окислення SO2 в SO3. Продуктивність реактору 75 т/доба сірчаної кислоти (моногідрату). Вихідний газ містить в % (об): SO2 – 11 O2 – 10, N2 – 79. Задана ступінь окислення х = 0,75. Температура 570°С. Лінійна швидкість газу в робочих умовах w = 1 м/с; хр = 0,78.
Визначити:
А) час контакту газу з каталізатором τ і об‘єм каталізатору vкат, необхідних для забезпечення заданого х;
Б) діаметр реактору і висоту шару каталізатору Н;
В) за тих же умов визначити час контакту τ при режимі, близькому до повного змішування (киплячий шар).
Завдання №16
Електроліз розчину хлориду натрію у ваннах з твердим катодом.
Технологічна схема виробництва аміачної селітри з випарюванням розчинів.
Кокс має наступний склад, %: С – 84,53; Н – 0,9; S – 1,54; Н2О – 3,53; зола – 9,5. Підрахувати теоретичну кількість повітря, потрібного для згоряння 1 т коксу, якщо прийняти, що:
а) вуглець згорає з утворенням СО2, водень – Н2О;
б) горіння
сірки протікає за рівнянням
![]() .
.
Досліджується кінетика реакції 3Н2 + СО = СН4 + Н2О на нікелевому каталізаторі. Кінетичне рівняння, яке характеризує початкову швидкість реакції
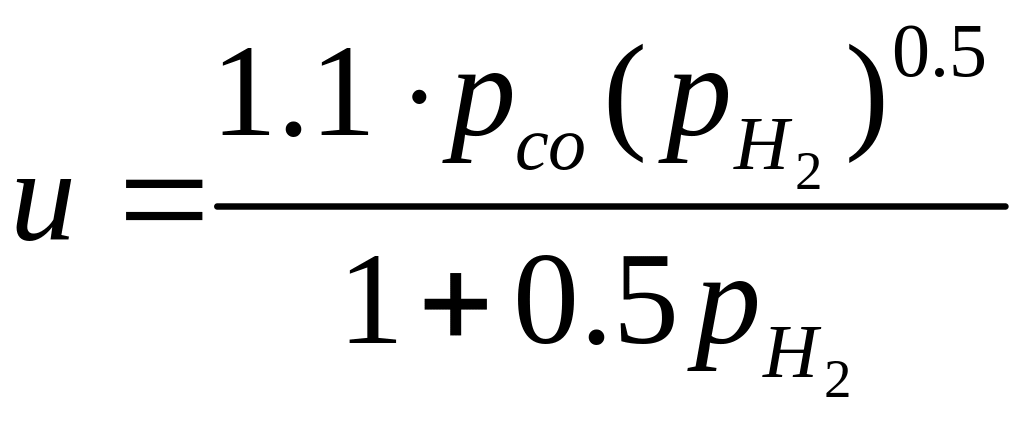
Задана ступінь перетворення, для якої справедливо наведене кінетичне рівняння, х = 0,3. Об‘ємна маса каталізатору Gкат = 480 кг/м3. Визначити об‘єм реактору для перетворення 4,536 кмоль/год СО, присутнього в еквімолекулярній суміші метану і водню.
Завдання №17
Мінеральні добрива, їх класифікація. Масштаби виробництва мінеральних добрив в Україні.
Технологічні стадії виробництва кальцинованої соди, їх фізико-хімічні основи та апаратурне оформлення.
Формальдегід отримують при контактному окисленні метанолу на срібному каталізаторі. Ступінь перетворення метанолу у формальдегід 0,7. Загальний ступінь перетворення метанолу – 0,8 (з урахуванням побічних реакцій). Вміст метанолу в спиртово-повітряній суміші 40 об.%. Визначити витрати метанолу та повітря для отримання 1 т формальдегіду.
Розрахувати тепловий ефект конверсії етилену (в кДж/моль):
С2Н4
+ 2Н2О
= 2СО + 4Н2
+
Q![]()
Завдання №18
Фосфорні добрива, їх класифікація. Технологічні схеми виробництва простого та подвійного суперфосфату.
Електроліз розчинів хлориду натрію у ваннах з твердим катодом.
При випалі 1 т вапняку утворюється 168 м3 діоксиду вуглецю. Вміст СаСО3 у вапняку 94%. Визначити ступінь випалу вапняку та його витрати на 1000 м3 СО2.
Підрахувати теоретичну температуру горіння пропану при надлишку повітря 20% (α = 1,2). Реакція горіння пропану:
С3Н8 + 5О2 = 3СО2 + 4Н2О + Q
