- •Методические указания по физиологии растений Клетка
- •1 Явление плазмолиза и деплазмолиза
- •2 Определение сосущей силы растительных тканей методом струек (по Шардакову)
- •3 Определение осмотического потенциала клеточного сока методом Уршпунга
- •4 Зависимость набухания семян от характера запасных веществ.
- •5 Определение интенсивности транспирации и относительной транспирации весовым методом.
- •6 Значение пробки для защиты растений от потери воды
- •7 Флюоресценция и химические свойства пигментов листа.
- •Флюоресценция
- •Химические свойства пигментов
- •8 Этиолированные растения. Обнаружение фотосинтеза методом крахмальной пробы (пробы Сакса). Путь с3
- •Путь с4 Хетча и Слэка
- •Фотосинтез по типу толстянковых (сам-метаболизм; «Crassulaceae acid metabolism»)
- •9 Методы определения площади листьев
- •10 Потеря сухого вещества при прорастании семян Гликолиз и брожение
- •11 Определение интенсивности дыхания по количеству выделенного со2 (методом Бойсен-Йенсена)
- •12 Определение дыхательного коэффициента прорастающих семян Электрон-транспортная цепь на мембранах митохондрий, переводящая энергию наd-н, наd(p)-н и янтарной кислоты (сукцината) в энергию атф
- •13 Озоление растительных материалов.
- •14 Влияние солей тяжелых металлов на всхожесть и рост проростков
- •15 Антагонизм ионов
- •16 Значение листа в процессе корнеобразования
- •17 Определение зоны геотропического изгиба у корня и стебля
- •18 Задерживающее и стимулирующее действие гетероауксина на рост корней в зависимости от его концентрации
- •19 Задерживающее влияние света на рост растений
- •20 Развитие проростков пшеницы при выращивании в синем и красном спектре 2 Фоторецепция
- •Действие красного света
- •Фотопериодизм
- •Действие синего света
- •21 Определение жизнеспособности семян
- •22 Влияние высокой температуры на проницаемость цитоплазмы
- •23 Защитное действие сахара на цитоплазму при замораживании
- •24 Определение активности амилаз в прорастающих семенах (по Вольгемуту)
- •25 Обнаружение нитратов в продукции растениеводства Азот
3 Определение осмотического потенциала клеточного сока методом Уршпунга
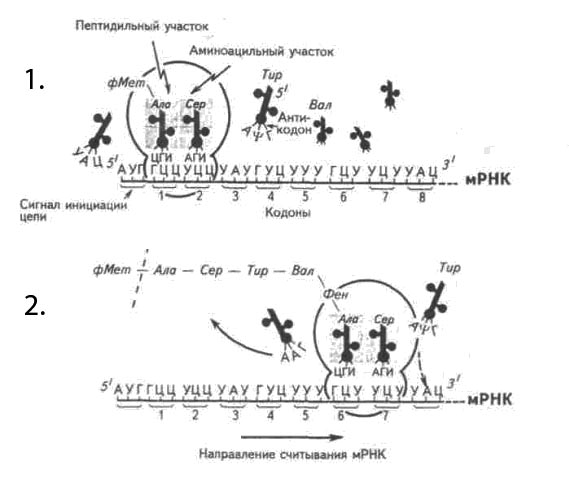
рис. 6 Синтез белка на рибосоме
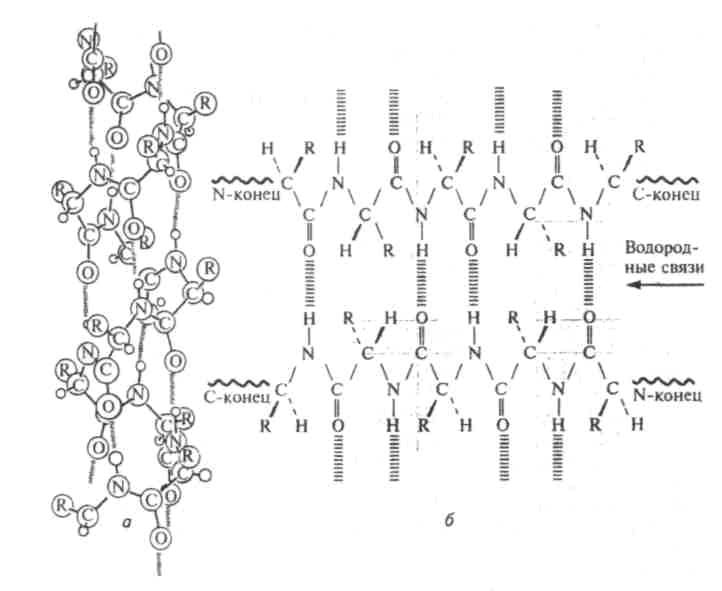
Рис. 7. Вторичная структура белка: в — а-спираль; б —складчатая структура (по Р. Бохински, 1987)
8.
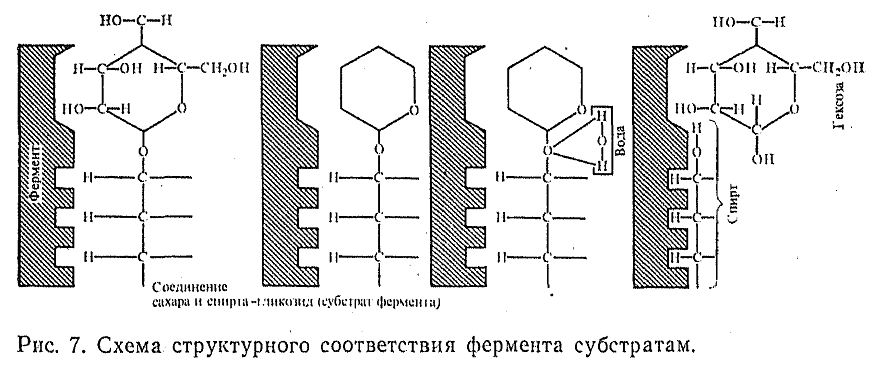
9.
Материалы и оборудование: растительные объекты (листья, корнеплоды), 1 н раствор NaCl или 1 н раствор сахарозы, дистил. вода, 2 бюретки с воронками, 2 химических стаканчика, штатив, 10 пробирок на 15-20 мл, мерные пробирки, пинцет, пробочное сверло d=5 мм, карандаш по стеклу.
Ход работы
1. Пронумеровать 10 пробирок на 15-20 мл. (1-10).
Заполнить бюретки: 1 - Н20; 2 - 1 н раствором NaCl (или сахарозы).
Приготовить растворы по 10 мл в пробирках объемом 15-20 мл (см. табл. в работе 2).
Приготовить растительный материал:
из корнеплодов вырезать пробочным сверлом высечь 10 одинаковых цилиндров d=5 мм и длиной 40-70 мм;
из листьев вырезать 10 полосок шириной около 5 мм и длиной 40 - 70 мм. Длина всех цилиндров и полосок для одного опыта должна быть строго одинаковая.
Поместить по одному цилиндрику корнеплодов или по одной полоске листьев в пробирки, выдерживать в течение 30-60 минут (время должно быть строго одинаковым для всего опыта).
Длину каждого бруска точно измеряют с помощью линейки перед экспозицией и после нее.
Результаты занести в таблицу.
Рассчитать осмотический потенциал по формуле: P=RTiC, где Р - осмотический потенциал;
R - газовая постоянная = 0,0821;
Т - температура в Кельвинах (T=273+t°C);
С - найденная концентрация клеточного сока;
i - изотонический коэффициент (NaCl - 1,5; сахароза - 1,0).
Сделать выводы.
Таблица
Концентрация растворов, н |
Длина растительных объектов до экспозиции, мм |
Длина растительных объектов после экспозиции, мм |
Изменение длины, мм |
0,1 |
|
|
. |
0,2 |
|
|
|
0,3 |
|
|
|
0,4 |
|
|
|
0,5 |
|
|
|
4 Зависимость набухания семян от характера запасных веществ.
|
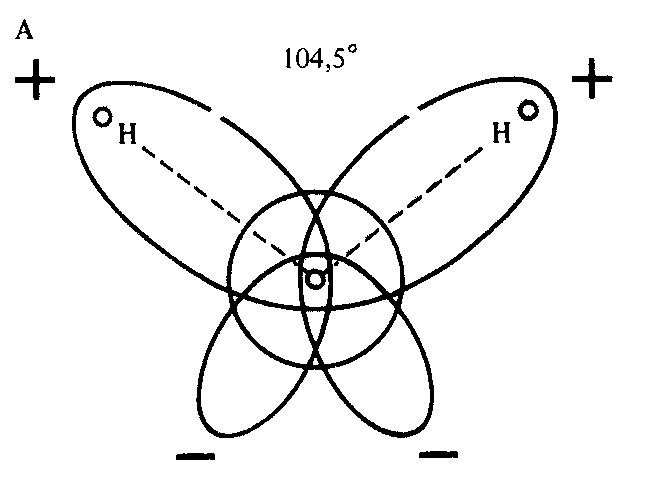
Вследствие того что орбиты с неподеленными электронами атома кислорода лежат в плоскости, перпендикулярной плоскости молекулы, а угол между ядрами водорода составляет 104,5° (109,5° для льда), возникает структура тетраэдра с четырьмя полюсами электрических зарядов: двумя положительными и двумя отрицательными. |
Каждая молекула воды, являясь диполем с тетраэдрическим распределением электронов вокруг атома кислорода, может взаимодействовать с четырьмя другими молекулами воды за счет электростатического взаимодействия атомов Н и О соседних молекул.
|
|
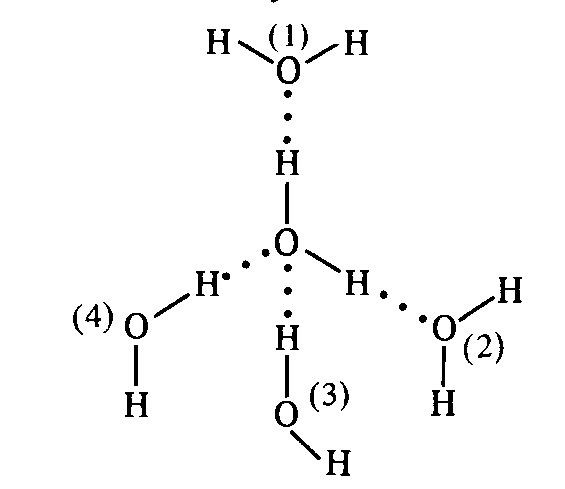
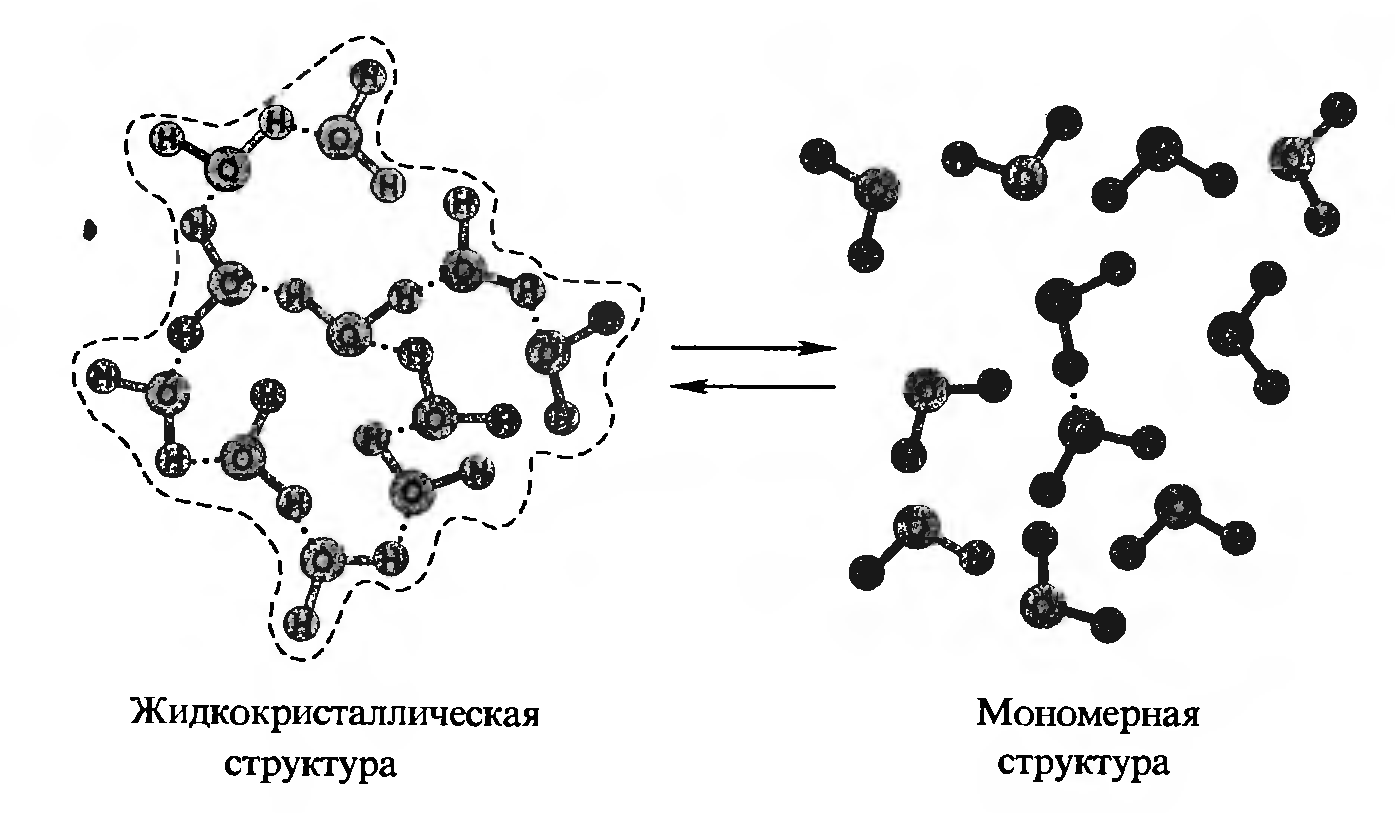
Молекулы 1 и 2 находятся в плоскости чертежа; 3 — над плоскостью; 4 — под ней. Жидкая вода в зависимости от температуры может находиться либо в жидко-кристаллической форме, либо в свободном состоянии.

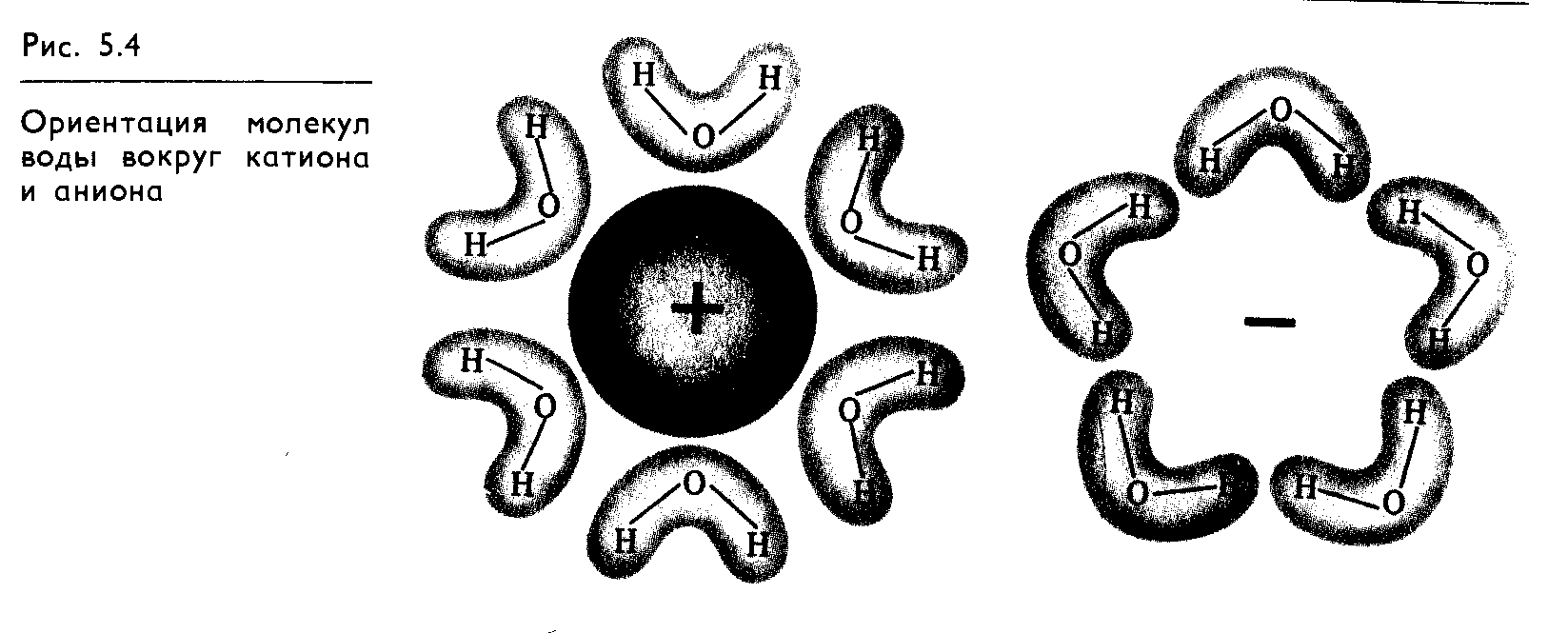
В электрическом поле катиона все ближайшие молекулы воды ориентируются отрицательными полюсами внутрь (рис. 5.4), а вокруг аниона внутрь направлены положительные полюсы молекул воды. Этот внутренний, прочно связанный с ионом слой молекул воды называют первичной, или ближней, гидратацией (сольватацией).
Однако ион, связывая определенное число молекул воды из своего непосредственного окружения, в результате иондипольного взаимодействия ориентирует также более далеко расположенные диполи воды. Эту гидратацию называют вторичной или дальней.
Цель занятия: установить зависимость набухания семян от характера запасных веществ.
Материалы и оборудование: семена гороха и пшеницы; весы; чашки Петри; водопроводная вода; фильтровальная бумага.
Вводные пояснения
При соприкосновении с влажным субстратом сухие семена поглощают воду и увеличиваются в объеме благодаря набуханию белков, крахмала и других гидрофильных коллоидов, при этом у некоторых семян возникает большое давление (до 100 МПа). В основе набухания лежит гидратация коллоидов – взаимодействие веществ с водой, приводящее к уменьшению ее подвижности. Главную роль в процессе набухания семян играют наиболее гидрофильные вещества – белки. Набухание белков имеет большое значение для биохимической активности клетки.
Гидратация белков включает три процесса:
1) электронейтральную гидратацию путем образования водородных связей между атомами О и N полярных групп (карбоксильной, спиртовой, аминной, амидной и др.) и водородом воды (наиболее важный процесс, приводящий к значительному увеличению объема и повышению температуры);
2) ионную гидратацию – притяжение диполей воды ионизированными группами белка – СОО – и – NH3+;
3) иммобилизацию молекул воды, попадающих в замкнутые полости белковых глобул.
Ход работы
Поместить в чашки Петри навески (2-5 г) семян пшеницы и гороха и залить водопроводной водой, обратив внимание на полное смачивание семян. Через 2-3 ч извлечь семена из чашек, быстро обсушить фильтровальной бумагой и взвесить. Увеличение массы выразить в процентах от исходной.
Задание 1. Результаты опыта записать в таблицу
Растение |
Масса семян, г |
Прибавка к массе |
||
исходная |
после набухания |
г |
% |
|
Пшеница |
|
|
|
|
Горох |
|
|
|
|
Задание 2. По результатам работы сделать вывод с учетом того, что семена отличаются разным содержанием основных запасных веществ – крахмала и белка (в семенах пшеницы содержится в среднем около 16 % белка и 70 % крахмала, в семенах гороха – до 34 % белка и 48 % крахмала).