
11 Раздел
Получение рентгеновского излучения.
Рентге́новская тру́бка — электровакуумный прибор, предназначенный для генерации рентгеновского излучения.
Рентгеновские лучи возникают при сильном ускорении заряженных частиц (тормозное излучение), либо при высокоэнергетических переходах в электронных оболочках атомов (характеристическое излучение). Оба эффекта используются в рентгеновских трубках.
Рентгеновская трубка.
Излучающий элемент представляет собой вакуумный сосуд с тремя электродами: катодом, накал катода и анодом.
Основными конструктивными элементами таких трубок являются металлические катод и анод.
В
рентгеновских трубках электроны,
испущенные катодом,
ускоряются под действием разности
электрических потенциалов между анодом
и катодом (при этом рентгеновские лучи
не испускаются, так как ускорение слишком
мало) и ударяются об анод, где происходит
их резкое торможение. При этом за
счёт тормозного
излучения происходит
генерация излучения рентгеновского
диапазона, и одновременно выбиваются
электроны из внутренних электронных
оболочек атомов
анода. Пустые места в оболочках занимаются
другими электронами атома. При этом
испускается рентгеновское излучение
с характерным для материала анода
спектром энергий (характеристическое
излучение,
частоты определяются законом
Мозли: ![]() где Z — атомный
номер элемента
анода, A и B —
константы для определённого значения
главного квантового числа n электронной
оболочки).
где Z — атомный
номер элемента
анода, A и B —
константы для определённого значения
главного квантового числа n электронной
оболочки).
рисунок
Тормозное излучение и его спектр.
Тормозное излучение — электромагнитное излучение, испускаемое заряженной частицей при её рассеянии (торможении) в электрическом поле.
Спектр фотонов тормозного излучения непрерывен и обрывается при максимально возможной энергии, равной начальной энергии электрона.
Характеристическое излучение и его спектр.
Характеристический спектр рентгеновского излучения, в противоположность непрерывному его спектру, состоит из отдельных спектральных линий. Он состоит из нескольких групп (серий) линий, отличающихся друг от друга длиной волны.
Исходя из планетарной модели атома, возбуждение характеристического спектра можно представить следующим образом. Когда движущийся в рентгеновской трубке от катода к аноду электрон при столкновении его с электроном какого-либо атома вещества анода сорвет его с его орбиты и выбросит за пределы атома, то на освободившееся место упадет другой электрон с одной из расположенных выше орбит, обладающей большей энергией, чем та орбита, на которую он упадет. При таком переходе освободится часть внутриатомной энергии, которая и излучается в виде одного кванта характеристического излучения.
Так как строение электронной оболочки меняется от одного химического элемента к другому, то каждый элемент даст свой особый характеристический спектр. Отсюда его название — характеристическое излучение.
Природа химической связи.
Химическая связь между атомами имеет электростатическую природу. Под химической связью понимают электрические силы притяжения, удерживающие частицы друг около друга.
По своей природе она представляет собой электростатическую силу притяжения между отрицательно заряженными электронами и положительно заряженными ядрами. Величина этой силы притяжения зависит главным образом от электронной конфигурации внешней оболочки атомов.
Частицы, которые принимают участие в образовании химических связей, могут быть атомами, молекулами или ионами.
Молекулярные спектры.
МОЛЕКУЛЯРНЫЕ СПЕКТРЫ - оптические спектры испускания, поглощения и рассеяния света, принадлежащие свободным или слабо связанным молекулам.
По сравнению с линейчатыми атомными спектрами молекулярные имеют более сложную структуру. Они состоят из совокупности полос, которые в свою очередь, распадаются на ряд тесно расположенных линий. Причина такого усложнения спектров заключается в том, что наряду с движением электронов вокруг ядер в молекуле происходит колебание самих ядер относительно положения равновесия и вращение молекул как целого.
Водородоподобный атом в квантовой механике
Атомные системы являются важнейшими объектами физики, для описания которых следует обязательно использовать законы квантовой механики.
Задача об атоме водорода - одна из фундаментальных проблем квантовой механики, успешное решение которой способствовало дальнейшему развитию теории.
ВОДОРОДОПОДОБНЫЙ
АТОМ - квантовомеханическая система,
состоящая из ядра массы М с зарядом
+Ze и
одного электрона
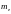 - массы
m
с зарядом - е, взаимодействующих
по закону Кулона, т. е. притягивающихся
друг к другу с силой, обратно пропорциональной
квадрату расстояния между ядром и
электроном. В частном случае при Z=1,
когда ядром является протон, В. а. -
обычный атом водорода.
- массы
m
с зарядом - е, взаимодействующих
по закону Кулона, т. е. притягивающихся
друг к другу с силой, обратно пропорциональной
квадрату расстояния между ядром и
электроном. В частном случае при Z=1,
когда ядром является протон, В. а. -
обычный атом водорода.
